
| A、O2和O3 |
| B、CH2=CHCH2CH3和CH3CH=CHCH3 |
| C、CH3CH2CH3和CH3(CH2)2CH3 |
| D、乙醇和乙醚 |


科目:高中化学 来源: 题型:
| A、食物中的主要成分能与酸反应的是碱性食物 |
| B、食物中的主要成分能与碱反应的是酸性食物 |
| C、食物在遇到甲基橙变红的是酸性食物,遇到酚酞变红的是碱性食物 |
| D、食物的酸碱性应当看食物在体内代谢完全后剩余物质的酸碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v (A)=0.3 mol?L-1?min-1 |
| B、v (B)=0.6 mol?L-1?min-1 |
| C、v (C)=0.5 mol?L-1?min-1 |
| D、v (A)=0.01 mol?L-1?s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
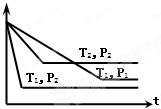 已知某可逆反应:mA(g)+nB(g)?xC(g),在密闭容器中进行,右图表示反应在不同时间t、温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则正确的是( )
已知某可逆反应:mA(g)+nB(g)?xC(g),在密闭容器中进行,右图表示反应在不同时间t、温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则正确的是( )| A、T1>T2,P1>P2,m+n>x,正反应放热 |
| B、T1<T2,P1<P2,m+n<x,正反应吸热 |
| C、T1>T2,P1<P2,m+n<x,正反应放热 |
| D、T1<T2,P1>P2,m+n>x,正反应吸热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N放出942KJ,根据以上信息和数据,下列说法正确的是( )
最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N放出942KJ,根据以上信息和数据,下列说法正确的是( )| A、N4属于一种新型的化合物 |
| B、N4与N2互为同位素 |
| C、N4与N2互为同素异形体 |
| D、1mol N4气体转变为N2将吸收882kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向燃料煤中加入生石灰,可以减少对大气的污染 |
| B、用双氧水清洗伤口,可以杀菌消毒 |
| C、只用淀粉溶液就能检验出食盐中是否加碘 |
| D、随意丢弃废旧电池,会对环境造成污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:
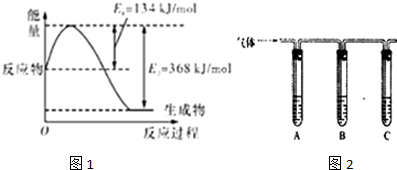
| 所加试剂 | 预期现象和结论 |
| 试管A中加足量 试管B中加1%品红溶液; 试管C中加 | 若 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、XYZ |
| B、X3YZ |
| C、XYZ2 |
| D、X2YZ3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、所含分子数和质量均不相同 |
| B、含有相同的分子数和电子数 |
| C、含有相同的质子数和中子数 |
| D、含有相同数目的中子、原子和分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com