
【题目】如图为原电池装置示意图。
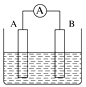
(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,作负极的分别是__(填字母)。
A 铝片、铜片 B 铜片、铝片
C 铝片、铝片 D 铜片、铜片
写出插入烧碱溶液中形成的原电池的负极反应式:____。
(2)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O。写出B电极反应式:___;该电池在工作时,A电极的质量将_(填“增加”“减小”或“不变”)。若该电池反应消耗了0.1 mol H2SO4,则转移电子的数目为__。
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池,写出B电极反应式:_________;该电池在工作一段时间后,溶液的碱性将___(填“增强”“减弱”或“不变”)。
(4)若A、B均为铂片,电解质为H2SO4溶液,分别从A、B两极通入CH4和O2,该电池即为甲烷燃料电池,写出A电极反应式:________;若该电池反应消耗了6.4克CH4,则转移电子的数目为__。
【答案】B Al-3e-+4OH-=AlO2-+2H2O PbO2+2 e-+4H++SO42-=PbSO4+2H2O 增加 6.021022 O2+4e-+2H2O=2H2O 减弱 CH4+8e-+2H2O=CO2+8H+ 3.26.021023
【解析】
根据原电池原理进行分析。
(1)将铝片和铜片用导线相连,一组插入浓硝酸中,由于铝遇浓硫酸发生钝化,而铜可以被浓硝酸溶解,故铜为负极、铝为正极;另一组插入烧碱溶液中,由于铝可以被其溶解,而铜不能,故铝为负极、铜为正极。综上所述,在这两个原电池中,作负极的分别是铜片、铝片,故选B 。
插入烧碱溶液中形成的原电池,负极上铝被氧化为偏铝酸根离子,电极反应式为:Al-3e-+4OH-=AlO2-+2H2O。
(2)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O。B电极为正极,其被还原为硫酸铅,电极反应式为PbO2+2 e-+4H++SO42-=PbSO4+2H2O;该电池在工作时,A电极被氧化为硫酸铅,故其质量将增加;由总反应可知,该反应若转移2mol电子可以消耗2mol H2SO4,若该电池反应消耗了0.1 mol H2SO4,则转移电子的数目为6.021022。
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池, B电极为正极,其电极反应式为:O2+4e-+2H2O=2H2O;该电池在工作一段时间后,虽然总反应中不消耗KOH,但是由于电池总反应的产物是水,故溶液的碱性将减弱。
(4)若A、B均为铂片,电解质为H2SO4溶液,分别从A、B两极通入CH4和O2,该电池即为甲烷燃料电池, A电极为负极,甲烷被氧化为二氧化碳,其电极反应式为:CH4+8e-+2H2O=CO2+8H+;由负极的电极反应可知,16g CH4参加反应时,可以转移8mol e-,因此,若该电池反应消耗了6.4克CH4(其物质的量为0.4mol),则转移电子的数目为3.26.021023。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 1.00mol NaCl中含有6.02×1023个NaCl分子
B. 1.00mol NaCl中,所有Na+的最外层电子总数为8×6.02×1023
C. 欲配置1.00L ,1.00mol.L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中
D. 电解58.5g熔融的NaCl,能产生22.4L氯气(标准状况)、23.0g金属钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C在周期表中所处的位置如图所示。A、B、C三种元素原子的质子数和为32。D元素原子的最外层电子数是其次外层电子数的2倍。则下列说法正确的是( )
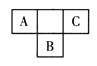
A.四种元素形成的气态氢化物中,C元素的氢化物的稳定性最强
B.元素D的某种同位素质量数为14,则其中子数为6
C.B、C两种元素可形成BC6型化合物,该化合物属于离子化合物
D.A、B两种元素的气态氢化物均能与它们对应的最高价氧化物对应的水化物发生反应,且都属于氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯酚和丙酮都是重要的化工原料,工业上可用异丙苯氧化法生产苯酚和丙酮,其反应和工艺流程示意图如下:
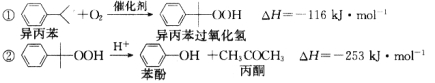
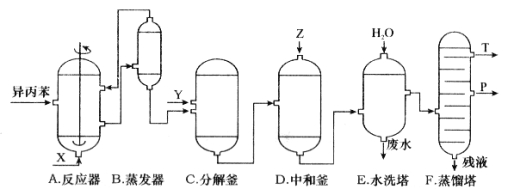
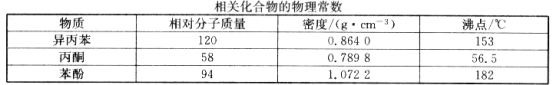
回答下列问题:
(1)在反应器 A 中通入的 X 是 。
(2)反应①和②分别在装置 和 中进行。(填装置符号)
(3)在分解釜 C中加入的Y为少量浓硫酸,其作用是 ,优点是用量少,缺点是 。
(4)反应②为 (填“放热”或“吸热”)反应。反应温度应控制在 50~60℃,温度过高的安全隐患是 。
(5)中和釜 D 中加入的 Z 最适宜的是 (填序号。已知苯酚是一种弱酸)。
A.NaOH B.CaCO3 C.NaHCO3 D.CaO
(6)蒸馏塔 F 中的馏出物 T 和 P 分别为 和 ,判断的依据是 。
(7)用该方法合成苯酚和丙酮的优点是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能影响水的电离平衡,并使溶液中c(H+)>c(OH-)的措施是( )
A. 将水加热煮沸,测得pH=6 B. 向水中加入FeCl3固体
C. 向纯水中投入一小块金属钠 D. 向水中加入Na2CO3固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用电石制备的乙炔气体中常混有少量H2S气体。请用图中仪器和药品组成一套制备、净化乙炔的装置,并可通过测定乙炔的量,从而计算电石纯度。

(1)电石制备乙炔气体的化学方程式____________;
(2)进行实验时,所制气体从左向右流,仪器的正确连接顺序是____________(填接口字母);
(3)为了使实验中气流平稳,甲中分液漏斗里的液体通常用_______________;
(4)若在标准状况下溴水与乙炔完全反应生成C2H2Br4,已知称取电石m g,测得量筒内液体体积V mL,则电石纯度可表示为____________;
(5)若没有装置戊,测定结果将会______(填“偏高”、“偏低”或“不变”) ,理由是(方程式表示)____;
(6)干燥乙炔可用_____________(填选项);
A. 
B.
C.
D.
(7)为了探究乙炔与HBr发生加成反应后的有关产物,进行以下实验:纯净乙炔气 ![]() 混合液
混合液 ![]() 有机混合物Ⅰ
有机混合物Ⅰ ![]() 混合液
混合液 ![]() 有机混合物Ⅱ
有机混合物Ⅱ
①操作b的名称是________;
②有机混合物Ⅰ可能含有的物质是________(写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在硫酸铜晶体结晶水含量测定的实验中,会造成实验结果偏低的是( )
A. 加热时间过长,固体部分变黑B. 坩埚内附有不挥发杂质
C. 晶体不纯,含有不挥发杂质D. 加热过程中有少量晶体溅出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲使1.6 g Fe2O3完全被还原,事先应准备的CO气体的标准状况下的体积为( )
A. 672 mLB. 336 mLC. 大于672 mLD. 小于336 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.完成下列制备物质的化学方程式:以电石、水、食盐为原料制备PVC____________________
II.由丁炔二醇制取1,3-丁二烯,请根据下面的合成路线图填空:
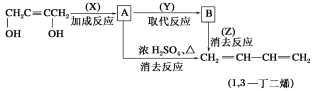
(1)写出各反应的反应条件及试剂名称:X________;Y________;Z________。
(2)写出A、B的结构简式:A____________;B____________。
III.下列物质在水中可能存在化合物甲、乙、丙有如下转化关系:
甲(C4H10O)条件条件①→乙(C4H8)![]() 丙(C4H8Br2)回答:
丙(C4H8Br2)回答:
(1)甲中官能团的名称是________,甲属________类物质,甲可能结构有________种,其中可催化氧化为醛的有________种。
(2)反应条件①为______________,条件②为______________。
(3)甲→乙的反应类型为____________,乙→丙的反应类型为____________。
(4)丙的结构简式不可能是________。
A.CH3CH2CHBrCH2Br B.CH3CH(CH2Br)2
C.CH3CHBrCHBrCH3 D.(CH3)2CBrCH2Br
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com