
【题目】锰及其化合物在工农业生产和科技领域具有广泛的应用。
Ⅰ.溶液中的Mn2+可被酸性(NH4)2S2O8溶液氧化为MnO4-,同时(NH4)2S2O8被还原为SO42-,该方法可用于检验Mn2+。
(1)用酸性(NH4)2S2O8溶液检验Mn2+时的实验现象为____。
(2)该反应的离子方程式为____。
(3)已知H2S2O8中硫的化合价为+6,若硫酸的结构简式为![]() ,则H2S2O8的结构简式为____。
,则H2S2O8的结构简式为____。
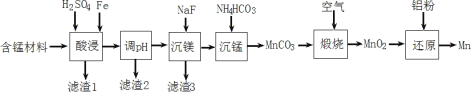
Ⅱ.实验室用含锰废料(主要成分为MnO2,还含有少量Al2O3、MgO、SiO2)为原料制备Mn的工艺流程如图所示。
已知:①部分难溶物的溶度积常数如下表所示。
难溶物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 | Mn(OH)2 |
溶度积常数 | 4.0×10-38 | 1.0×10-33 | 1.8×10-11 | 1.8×10-13 |
②当溶液中离子浓度≤1.0×10-5molL-1时,可认为该离子沉淀完全。
(1)“酸浸”时,MnO2将Fe氧化为Fe3+,该反应的离子方程式为____;该过程中浸出时间和液固比对锰浸出率的影响分别如图所示。
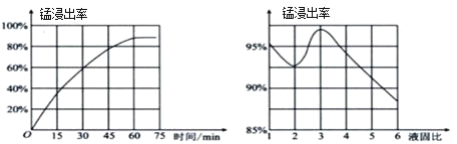
则适宜的浸出时间和液固比分别为____、____。
(2)若“酸浸”后所得滤液中c(Mn2+)=0.18molL-1,则应“调pH”的范围为____。
(3)“煅烧”反应中氧化剂与还原剂的物质的量之比为____。“还原”时发生的置换反应在化学上又叫作____。
【答案】溶液由无色变为紫红色 5S2O82-+2Mn2++8H2O=2MnO4-+10SO42-+16H+ 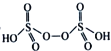 3MnO2+2Fe+12H+=3Mn2++2Fe3++6H2O 60min 3:1(或3)
3MnO2+2Fe+12H+=3Mn2++2Fe3++6H2O 60min 3:1(或3) ![]() ≤pH<8(或4.7≤pH<8) 1:2 铝热反应
≤pH<8(或4.7≤pH<8) 1:2 铝热反应
【解析】
Ⅰ.⑴高锰酸根是紫红色,Mn2+是无色。
⑵根据S2O82与Mn2+反应生成MnO4-、SO42原理书写离子方程式。
⑶硫酸的结构简式为![]() ,H2S2O8中含有过氧根,书写其结构简式。
,H2S2O8中含有过氧根,书写其结构简式。
Ⅱ “酸浸”时,MnO2将Fe氧化为Fe3+,自身变为Mn2+,氧化铝、氧化镁变为溶液,二氧化硅是滤渣1,调节pH将铁离子和铝离子沉淀完全得到滤渣2,加入NaF沉淀镁离子得到滤渣3,加入碳酸氢铵与锰离子反应生成碳酸锰,过滤后与氧气煅烧生成二氧化锰,再经铝热反应生成锰。
Ⅰ⑴Mn2+是无色,高锰酸根是紫红色,因此酸性(NH4)2S2O8溶液检验Mn2+时的实验现象为溶液由无色变为紫红色;故答案为:溶液由无色变为紫红色。
⑵该反应的离子方程式为5S2O82+2Mn2++8H2O=2MnO4-+10SO42+16H+;故答案为:5S2O82+2Mn2++8H2O=2MnO4-+10SO42+16H+。
⑶已知H2S2O8中硫的化合价为+6,若硫酸的结构简式为![]() ,则H2S2O8中含有过氧根,其结构简式为
,则H2S2O8中含有过氧根,其结构简式为 ;故答案为:
;故答案为: 。
。
Ⅱ⑴“酸浸”时,MnO2将Fe氧化为Fe3+,自身变为Mn2+,其反应的离子方程式为3MnO2+ 2Fe + 12H+=3Mn2++2Fe3++6H2O;该过程中浸出时间60min达到80%,以后浸出率不再上升,液固比等于3时锰浸出率最大,因此适宜的浸出时间和液固比分别为60min、3:1(或3);故答案为:60min;3:1(或3)。
⑵若“酸浸”后所得滤液中c(Mn2+)=0.18molL-1,铁离子先沉淀,再是铝离子沉淀,则应“调pH”的范围在铝离子沉淀完全,而锰离子刚沉淀时,![]() ,
, ,pH =
,pH =![]() ,
,![]() ,则
,则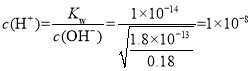 ,pH = 8,因此应“调pH”的范围为
,pH = 8,因此应“调pH”的范围为![]() ≤pH<8;故答案为:
≤pH<8;故答案为:![]() ≤pH<8。
≤pH<8。
⑶“煅烧”反应是碳酸锰和空气中氧气反应,碳酸锰中锰化合价/span>+2价变为二氧化锰+4价的锰,氧气中氧化合价降低到-2价,根据得到电子守恒得到氧化剂与还原剂的物质的量之比为1:2;“还原”时发生的置换反应是铝和二氧化锰高温反应生成锰和氧化铝,在化学上又叫作铝热反应;故答案为:1:2;铝热反应。


 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】工业上可采用丙烯氨氧化法制丙烯脂,回答下列问题:
I.丙烯的制备反应方程式为C3H8(g)=C3H6(g)+H2(g)。
已知:部分共价键的键能如下:
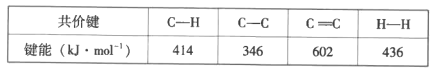
(1)制备丙烯反应的△H=__。该反应在__(“高温”或“低温”)下有利于自发进行。
(2)提高丙烯产率可以选择__(填序号)。
A.升温 B.减小压强 C.充入H2(恒容) D.加入催化剂
(3)已知:CO2(g)+H2(g)=CO(g)+H2O(g) H=-41kJ·mol-1,工业上选择向反应体系中加入CO2,提高丙烷的转化率,从化学平衡原理角度说明原因:__。
II.利用丙烯制备丙烯腈,反应方程式如下:2C3H6(g)+2NH3(g)+3O2(g)![]() 2CH2=CHCN(g)+6H2O(l) H=-1294kJ·mol-1。
2CH2=CHCN(g)+6H2O(l) H=-1294kJ·mol-1。
(4)主要的反应机理如下:
CH3-CH=CH2→[CH2![]() CH
CH![]() CH2]+H 慢 H>0
CH2]+H 慢 H>0
[CH2![]() CH
CH![]() CH2]+[NH]→CH2=CH-CN+3H 快
CH2]+[NH]→CH2=CH-CN+3H 快
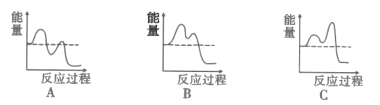
如图能表示反应历程的是__(填序号)。.
(5)一定温度下,IL恒容密闭容器中充人等物质的量的C3H6、NH3、O2制备丙烯腈,c(C3H6)与v正随时间变化的数据如下表:
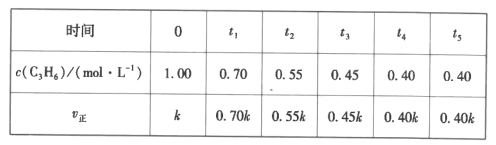
①判断t4时刻反应是否已经达到平衡状态并说明理由:__。
②列式并计算制备丙烯腈反应的平衡常数K=__(mol·L-1)-5。
③已知:正反应速率v正=kca(C3H6),根据表中数据,a=__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值,下列说法正确的是( )
为阿伏加德罗常数的值,下列说法正确的是( )
A.常温常压下,![]() 中所含中子数为
中所含中子数为![]()
B.![]() 溶液中含有
溶液中含有![]() 数目小于
数目小于![]()
C.熔融状态下,![]() 中所含阳离子数目为2
中所含阳离子数目为2![]()
D.25°C时,![]() 的碳酸钠溶液中,由水电离出的
的碳酸钠溶液中,由水电离出的![]() 数目为
数目为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工发展水平。请回答下列问题。
(1)乙烯的电子式为____,结构简式为____。
(2)鉴别甲烷和乙烯可用的试剂是____(填字母)。
A 稀硫酸 B 溴的四氯化碳溶液
C 水 D 酸性高锰酸钾溶液
(3)已知2CH3CHO+O2![]() 2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如图所示。
2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如图所示。
乙烯![]() A
A![]() B
B![]() 乙酸
乙酸
反应②的化学方程式为________。
工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方程式为____,反应类型是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组利用以下装置制取并探究氨气的性质。在A装置中发生反应的化学方程式为2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O。
CaCl2+2NH3↑+2H2O。

(1)B装置中的干燥剂是_____(填“碱石灰”或“浓硫酸”)。
(2)C、D装置中试纸颜色会发生变化的是_____(填”C”或“D”)。
(3)当实验进行段时间后,挤压E装置中的胶头滴管,滴入1--2滴浓盐酸,可观察到E装置中的现象是产生______(填”烟”或“白雾”)。
(4)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是_____(填“F”或“G”)。
(5)生石灰与水反应生成Ca(OH)2并放出热量。实验室利用此原理,向生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用的气体发生装置是____(填“a”“b”或“c”)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的短周期元素,且X、Z原子序数之和是Y、W原子序数之和的1/2。甲、乙、丙、丁是由这些元素组成的二元化合物,M是某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下)。上述物质间的转化关系如图所示(部分反应物和生成物省略)。下列说法正确的是
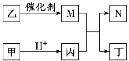
A. 原子半径:r(Y)>r(Z)>r(W)
B. 化合物N与乙烯均能使溴水褪色,且原理相同
C. 含W元素的盐溶液可能显酸性、中性或碱性
D. Z与X、Y、W形成的化合物中,各元素均满足8电子结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是(假设金属的摩尔质量为Mg·mol-1金属原子半径为r cm,用NA表示阿伏加德罗常数的值)

A.金属Zn采用②堆积方式
B.①和③中原子的配位数分别为:6、8
C.对于采用②堆积方式的金属的晶胞质量为![]()
D.金属锻压时,会破坏密堆积的排列方式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备乙酸丁酯的环境温度(反应温度)是115﹣125℃,其它有关数据如下表,则以下关于实验室制备乙酸丁酯的叙述错误的是( )
物质 | 乙酸 | 1-丁醇 | 乙酸丁酯 | 98%浓硫酸 |
沸点 | 117.9℃ | 117.2℃ | 126.3℃ | 338.0℃ |
溶解性 | 溶液水和有机物 | 溶液水和有机物 | 微溶于水,溶液有机物 | 与水混合 |
A.相对价廉的乙酸与1﹣丁醇的物质的量之比应大于1:1
B.不用水浴加热是因为乙酸丁酯的沸点高于100℃
C.从反应后混合物分离出粗品的方法:用Na2CO3溶液洗涤后分液
D.由粗品制精品需要进行的一步操作:加吸水剂蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】十九大报告指出:“坚持全民共治、源头防治,持续实施大气污染防治行动,打赢蓝天保卫战!”以NOx为主要成分的雾霾的综合治理是当前重要的研究课题。
汽车的排气管上安装“催化转化器”,发生反应①:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) △H=-746.5 kJ·mol-1。
2CO2(g)+N2(g) △H=-746.5 kJ·mol-1。
(1)T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中,若温度和体积不变,反应过程中(0~15min)NO的物质的量随时间变化如图。
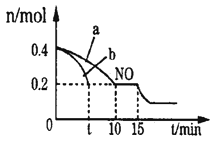
①图中a,b分别表示在相同温度下,使用质量相同但表面积不同的催化剂时,达到平衡过程中n(NO)的变化曲线,其中表示催化剂表面积较大的曲线是__。(填“a”或“b”)
②T℃时,该反应的化学平衡常数K=__;平衡时若保持温度不变,再向容器中充入CO、CO2各0.2 mol,则平衡将__移动。(填“向左”、“向右”或“不”)
③15min时,若改变外界反应条件,导致n(NO)发生图中所示变化,则改变的条件可能是___(任答一条即可)。
④又已知:反应②N2(g)+O2(g)![]() 2NO(g) △H2=+180.5 kJ·mol-1,则CO的燃烧热△H=__。
2NO(g) △H2=+180.5 kJ·mol-1,则CO的燃烧热△H=__。
(2)在密闭容器中充入5 mol CO和4 mol NO,发生上述反应①,如图为平衡时NO的体积分数与温度、压强的关系。

①温度:T1__T2(填“<”或“>”)。
②若在D点对反应容器升温的同时扩大体积使体系压强减小,重新达到的平衡状态可能是图中A~G点中的____点。
(3)目前,科学家正在研究一种以乙烯作为还原剂的脱硝原理,其脱硝率(脱硝率即NO的转化率)与温度、负载率(分子筛中催化剂的质量分数)的关系如图所示。
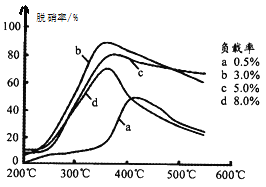
为达到最佳脱硝效果,应采取的条件是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com