
【题目】利用碳酸钠晶体(Na2CO3·10H2O)来配制1.0 mol·L-1Na2CO3溶液500 mL,假如其他操作均准确无误,下列情况会引起所配溶液浓度偏高的是( )
A. 称取碳酸钠晶体53.0 g
B. 定容时,俯视观察刻度线
C. 移液时,对用于溶解碳酸钠晶体的烧杯没有进行冲洗
D. 定容后,将容量瓶振荡摇匀,静置时发现液面低于刻度线,于是又加入少量水至刻度线
【答案】B
【解析】
根据![]() 可得,一定物质的量浓度溶液配制的误差都是由溶质的物质的量nB和溶液的体积V引起的。误差分析时,关键要看配制过程中引起n和V怎样的变化。
可得,一定物质的量浓度溶液配制的误差都是由溶质的物质的量nB和溶液的体积V引起的。误差分析时,关键要看配制过程中引起n和V怎样的变化。
A、1.0 mol/L的碳酸钠溶液500 mL需称取Na2CO3·10H2O的质量是1.0mol/L×0.5L×286g/mol=143g,称取碳酸钠晶体53.0 g会导致浓度偏低,A错误;
B、定容时俯视刻度线,会造成所配溶液的体积偏小,浓度偏高,B正确;
C、未冲洗溶解碳酸钠晶体的烧杯,会造成碳酸钠损失,浓度偏低,C错误;
D、定容后,将容量瓶振荡摇匀,静置时发现液面低于刻度线,于是又加入少量水至刻度线,溶液体积增加,会造成所配溶液的浓度偏低,D错误。
答案选B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】能源是现代社会发展的支柱之一。
(1)化学反应中的能量变化,主要表现为热量的变化。
①下列反应中,属于放热反应的是_________(填字母)。
a.Ba(OH)2·8H2O与NH4Cl混合搅拌
b.高温煅烧石灰石
c.铝与盐酸反应
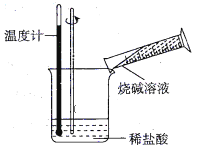
②某同学进行如图所示实验,测量稀盐酸与烧碱溶液中和反应的能量变化。实验表明,反应温度升高;由此判断该反应是_____________(填“吸热”或“放热”)反应,其离子方程式是__________________________。
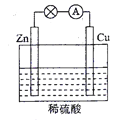
(2)电能是现代社会应用最广泛的能源之一。如图所示的原电池装置中,负极是____,正极上能够观察到的现象是________,正极的电极反应式是____________。原电池工作一段时间后,若消耗锌6.5 g,则放出气体_______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10mL0.1mol/LNaOH溶液中加入0.1mol/L的一元酸HA,溶液pH的变化曲线如图所示。下列说法正确的是

A. a点所示溶液中c(A-)+c(HA)=0.1mol/L
B. a、b两点所示溶液中水的电离程度不同
C. pH=7时,c(Na+)=c(A-)
D. b点所示溶液中c(HA)>c(A-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组微粒,在溶液中能大量共存的是( )
A.Ca2+、Cl﹣、CO32﹣、K+
B.Cu2+、Cl﹣、SO42﹣、OH﹣
C.K+、Cl﹣、NO3﹣、H+
D.H +、Cl﹣、CO32﹣、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是

A. X→Y反应类型为酯化反应
B. X、Y、Z均能使溴的四氯化碳溶液褪色
C. Y和Z互为同分异构体
D. 等物质的量的X、Z分别与足量Na反应,消耗Na的物质的量之比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氯水的说法正确的( )
A.新制氯水呈浅黄绿色,是因为氯水中含有HClO
B.新制氯水在光照的条件下,可以产生气体,该气体是氯气
C.新制氯水中滴加硝酸银溶液,没有任何现象
D.新制氯水中滴加石蕊试液,变红后褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com