
【题目】下图为实验室制取纯净、干燥的Cl2,并进行检验Cl2性质实验的装置。其中E瓶中放有干燥红色布条;F中为铜网,F右端出气管口附近放有脱脂棉。
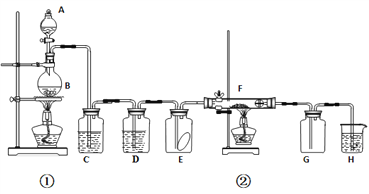
(1)A中所放试剂为________,B中所放试剂为________,二者反应的化学方程式为________,该反应中的氧化剂是______。
(2)C中试剂是_______;D中试剂的作用是_________。
(3)E中现象是_____________; F中现象是________,其反应的化学方程式为________。
(4)F管中脱脂棉的作用是________,H中试剂为______________。
(5)整套装置中有两处用酒精灯加热,两处酒精灯点燃的先后顺序是________。(用①或②填写)。
【答案】 浓盐酸 MnO2 MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O MnO2 饱和食盐水 吸收氯气中的水蒸气 干燥的红色布条不褪色 有棕黄色的烟产生 Cu+Cl2
MnCl2+Cl2↑+2H2O MnO2 饱和食盐水 吸收氯气中的水蒸气 干燥的红色布条不褪色 有棕黄色的烟产生 Cu+Cl2![]() CuCl2 防止CuCl2固体小颗粒被气体鼓入导管中,堵塞导管 NaOH溶液 ①②
CuCl2 防止CuCl2固体小颗粒被气体鼓入导管中,堵塞导管 NaOH溶液 ①②
【解析】本题考查实验方案设计与评价,(1)根据实验目的,装置①是制备氯气,制备氯气反应方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,因此分液漏斗中盛放浓盐酸,圆底烧瓶中盛放MnO2,氧化剂是化合价降低的物质,即MnO2为氧化剂;(2)制备的氯气中混有HCl和H2O(g),根据实验目的,需要制备纯净、干燥的氯气,因此装置C的作用是除去氯气中HCl,一般用饱和食盐水,装置D的作用是干燥氯气,或吸收氯气中的水镇通过其,盛放的是浓硫酸;(3)干燥的氯气不能使干燥的有色布条褪色,即E的现象是干燥的红色布条不褪色;F中发生Cu+Cl2
MnCl2+Cl2↑+2H2O,因此分液漏斗中盛放浓盐酸,圆底烧瓶中盛放MnO2,氧化剂是化合价降低的物质,即MnO2为氧化剂;(2)制备的氯气中混有HCl和H2O(g),根据实验目的,需要制备纯净、干燥的氯气,因此装置C的作用是除去氯气中HCl,一般用饱和食盐水,装置D的作用是干燥氯气,或吸收氯气中的水镇通过其,盛放的是浓硫酸;(3)干燥的氯气不能使干燥的有色布条褪色,即E的现象是干燥的红色布条不褪色;F中发生Cu+Cl2![]() CuCl2,铜和氯气反应产生棕黄色的烟;(4)E中产生棕黄色的烟,容易阻塞导管,因此脱脂棉的作用是防止CuCl2固体小颗粒被气体鼓入导管中,堵塞导管;氯气有毒,需要尾气处理,即装置H的作用是吸收过量的氯气,即H中盛放NaOH溶液;(5)装置中有空气,如果先加热②,铜和空气中氧气发生反应,生成CuO,因此先加热①,产生的氯气排尽装置中的空气,当装置中充满黄绿色气体,再点燃②,即先后顺序是①②。
CuCl2,铜和氯气反应产生棕黄色的烟;(4)E中产生棕黄色的烟,容易阻塞导管,因此脱脂棉的作用是防止CuCl2固体小颗粒被气体鼓入导管中,堵塞导管;氯气有毒,需要尾气处理,即装置H的作用是吸收过量的氯气,即H中盛放NaOH溶液;(5)装置中有空气,如果先加热②,铜和空气中氧气发生反应,生成CuO,因此先加热①,产生的氯气排尽装置中的空气,当装置中充满黄绿色气体,再点燃②,即先后顺序是①②。


科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种常见的金属单质,A元素在地壳中含量位列第6,A的密度为0.97 g/cm3;B为紫红色固体,锈蚀时变为绿色;C在空气中加热熔化但不滴落;D在氧气中燃烧,火星四射。根据以上信息回答下列问题:
(1)写出对应化学式:A________,B________,C________,D________。
(2)A在室温下与氧气反应时生成________,D在空气中锈蚀生成的氧化物为________。
(3)写出下列化学方程式:
①A在空气中燃烧_______________________________________________________;
②B长期置于空气中变为绿色物质______________________________________________。
(4)将5 g钠铝合金投入到200 mL的水中,固体完全溶解,产生4.48 L标准状况下的气体,溶液中只有一种溶质。经过分析得出钠铝合金中两种金属的物质的量之比为________,所得溶液中溶质的物质的量浓度为____________(假设溶液体积变化忽略不计)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式为 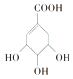 ,关于它的叙述中不正确的是( )
,关于它的叙述中不正确的是( )
A.该有机物能使溴的四氯化碳溶液褪色
B.该有机物发生消去反应可得到芳香烃
C.该有机物在一定条件下可发生氧化反应
D.1 mol该有机物最多可与1 mol NaHCO3反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )
选项 | 叙述Ⅰ | 叙述Ⅱ |
A | 纯碱是强碱弱酸盐 | 用纯碱溶液可清洗油污 |
B | 不锈钢是合金 | 不锈钢在潮湿环境中容易被腐蚀 |
C | Fe2O3是碱性氧化物 | Fe2O3可用作红色油漆和涂料 |
D | NO2是红棕色气体 | 常温下可用铜与浓硝酸制取NO2 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法正确的是

A.该硫酸试剂的物质的量浓度为18.4 mol/L
B.稀释该硫酸时应把水倒入硫酸中,边倒边搅拌
C.50 mL该H2SO4中加入足量的铜片并加热,被还原的H2SO4的物质的量为0.46 mol
D.标准状况下2.7 g Al与足量的该硫酸反应可得到H2 3.36 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组的同学为了探究SO2和氯水的漂白性,设计了如图所示实验装置。

(1)写出A中反应的化学方程式:___________, 浓硫酸表现出_____性。
(2)实验室用装置E制备Cl2,离子方程式为____________。该反应中的还原剂是_______(填化学式)。
(3)①装置A和E中,常用于萃取操作的仪器是__________(填名称)。
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为B.______,D._____。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1:1同时通入品红溶液中,结果发现品红溶液未褪色,并且生成了两种常见的强酸,请你分析该现象的原因:__________(用化学方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方法能达到实验目的是( )
A.用KMnO4溶液鉴别甲烷和乙烯
B.用焰色反应鉴别KNO3和KCl
C.用BaCl2溶液鉴别Na2CO3和Na2SO4
D.用NaOH溶液除去Cl2中含有的少量HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com