
【题目】(1)曲酸是一种非常有潜力的食品添加剂,经测定曲酸的分子式为C6H6O4,结构简式为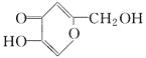 ,其所含有的官能团有(写结构简式) __________。
,其所含有的官能团有(写结构简式) __________。
(2)L­多巴用于帕金森综合症的治疗,其结构简式为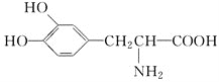 。这种药物的研制是基于获得2000年诺贝尔生理学和医学奖的研究成果。L­多巴分子中所含的官能团的名称是__________。
。这种药物的研制是基于获得2000年诺贝尔生理学和医学奖的研究成果。L­多巴分子中所含的官能团的名称是__________。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
Ⅰ.(1)将钠、钾、镁、铝各1 mol分别投入到足量的同浓度的盐酸中,试预测实验结果:___与盐酸反应最剧烈,_____与盐酸反应产生的气体最多。(填元素符号)
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为:__。
Ⅱ.利用图装置可验证同主族元素非金属性的变化规律
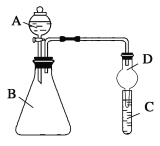
(3)仪器A的名称为____。
(4)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉—碘化钾混合溶液,观察到C中溶液____现象,即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用____溶液吸收尾气。
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液观察到C中溶液_____的现象,反应的离子方程为: _____。有同学认为实验无法证明C非金属性大于Si,请指出实验设计的不足之处,并进行改进: ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1mol/L醋酸溶液加水稀释,下列说法正确的是
A. 溶液中c(OH+)和c(OH-)都减小B. 溶液中c(OH+)增大
C. 醋酸电离平衡向左移动D. 溶液的pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)(题文)钨是我国丰产元素,是熔点最高的金属,广泛用于拉制灯泡的灯丝,有“光明使者”的美誉。
(1)T℃时,WO3经如下的四步反应生成W。每一步反应的焓变和平衡常数如下:
WO3(s)+0.1H2(g)![]() WO2.9(s)+0.1H2O(g) △H1 K1
WO2.9(s)+0.1H2O(g) △H1 K1
WO2.9(s)+0.18H2(g)![]() WO2.72(s)+0.18H2O(g) △H2 K2
WO2.72(s)+0.18H2O(g) △H2 K2
WO2.72(s)+0.72H2(g)![]() WO2(s)+0.72H2O(g) △H3 K3
WO2(s)+0.72H2O(g) △H3 K3
WO2(s)+2H2(g)![]() W(s)+2H2O(g) △H4 K4
W(s)+2H2O(g) △H4 K4
则该温度下,WO3(s)+3H2(g)![]() W(s)+3H2O(g) K=__________。
W(s)+3H2O(g) K=__________。
(2)T1℃时,将4molH2和足量WO3置于2 L密闭容器中,发生反应:WO3(s)+3H2(g)![]() W(s)+3H2O(g),混合气体各组分物质的量之比随时间变化的关系如图所示:
W(s)+3H2O(g),混合气体各组分物质的量之比随时间变化的关系如图所示:

①下列选项中能说明反应已经达到平衡的是_________。(填字母)
a.反应速率ν(H2)=ν(H2O)
b.每断裂3molH-H键的同时断裂3molO-H键
c.反应热不变
d.混合气体的密度不再改变
e.体系的压强不再改变
②反应在2min时达到平衡,此时H2的平衡转化率a=_________%。
③若在4min时升高并维持温度为T2℃,变化如图所示,则该反应的△H_______0,若在8min时缩小容器容积,则![]() ________1.3。(填“>”“ <”或“=”)
________1.3。(填“>”“ <”或“=”)
(3)利用电解法可以从合金碳化钨(WC)废料中回收钨元素(合金中钨、碳均为单质)。电解时,用合金碳化钨做阳极,不锈钢做阴极,盐酸溶液为电解液,阳极析出钨酸(H2WO4)并放出CO2。该阳极的电极反应式为___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100mL MgCl2和AlCl3的混和溶液中,逐滴加入NaOH溶液直至过量,经测定,加入NaOH物质的量和所得沉淀的物质的量的关系如图所示。回答下列问题。
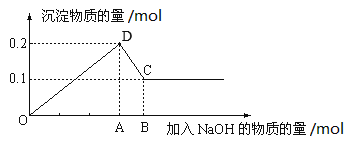
(1)图中CD段反应的化学方程式为___________;C点存在的固体物质为________。
(2)A点的数据为_______;混合液中,MgCl2的浓度为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物。某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究。
实验操作Ⅰ:在试管中加入5 mL 1 mol/L NaOH溶液和5 mL溴乙烷,振荡。
实验操作Ⅱ:将试管如图固定后,水浴加热。

(1)用水浴加热而不直接用酒精灯加热的原因是_________;试管口安装一长导管的作用是________________________。
(2)观察到________________现象时,表明溴乙烷与NaOH溶液已完全反应。
(3)鉴定生成物中乙醇的结构,可用的波谱是_____________________。
(4)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验的是________________,检验的方法是______________________________说明所用的试剂、简单的实验操作及预测产生的实验现象)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.2 mol某烃A在氧气中充分燃烧后,生成化合物B,C各1.2 mol。试回答:
(1)烃A的分子式为________。
(2)若取一定量的烃A完全燃烧后,生成B、C各3 mol,则有________g烃A参加了反应,燃烧时消耗标准状况下的氧气________L。
(3)若烃A不能使溴水褪色,但在一定条件下,能与氯气发生取代反应,其一氯代物只有一种,则烃A的结构简式为________________________________。
(4)若烃A能使溴水褪色,在催化剂作用下,与H2加成,其加成产物经测定分子中含有4个甲基,烃A可能有的结构简式为____________________________________;比烃A少2个碳原子的同系物有________种同分异构体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化不可能通过一步反应直接完成的是
A. Al(OH)3 → Al2O3 B. Al2O3 → Al(OH)3
C. Al → AlO2- D. Al3+ → Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下向20 mL 0.1 mol/L HA溶液中逐滴加入0.1 mol/L NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。下列说法中不正确的是

A. 由题可知HA为弱酸
B. 滴定终点位于c和d之间
C. 滴定到b点时:n(Na+)+ n(H+)-n(OH-)+ n(HA)=0.002 mol
D. 滴定到d点时:c(OH-)>c(Na+)>c(A-) >c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com