
【题目】下列变化中,需要加入还原剂的是( )
A.H2→HClB.Na2CO3→NaHCO3
C.FeCl3→FeCl2D.SO2→SO3
科目:高中化学 来源: 题型:
【题目】某溶液X中仅可能含有K+、Na+、Fe2+、Fe3+、SO42-、CO32-、I-、Cl-中的一种或多种,且溶液中各离子浓度相同。现进行下列实验,下列说法正确的是( )
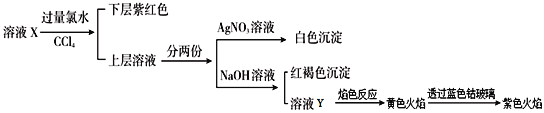
A. 该溶液X中Na+、Cl-一定有
B. 溶液Y中加入氯化钡溶液没有沉淀
C. 该溶液可能是硫酸亚铁、碘化钾和氯化钠溶于水后得到的
D. 原溶液X中滴加几滴KSCN溶液后,再滴加少量的次氯酸钠溶液后溶液呈血红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧化钠固体在实验室保存中容易变质。现取一定量的久存氢氧化钠固体样品溶于水,向所得溶液中逐滴加入稀盐酸至过量,生成的CO2(标准状况)与加入的盐酸体积有如图关系

(不考虑CO2在水中的溶解)。试计算:
(1)盐酸的物质的量浓度为________mol/L。
(2)该样品中NaOH与Na2CO3物质的量之比为________。
(3)若该氢氧化钠固体样品溶于水后用于吸收CO2,最多能吸收CO2的体积(标况下)是________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中,能大量共存且形成无色透明溶液的是
A.Mg2+、H+、C1-、OH-B.Na+、Ba2+、C1-、NO3-
C.Na+、H+、Cl-、CO32-D.K+、Cu2+、NO3-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下图中两极加以必要的连接并填空:

(1)在图A中,使铜片上产生氢气。
①若加以导线连接,则锌片发生____________(填“氧化”或“还原”);铜片上的电极反应式:____________________________。
②若外加电源,则铜片作为该装置的______极,连接电源的_______极;锌片上发生的电极反应式为________________________。
(2)在图B中,使a极析出铜。

①若a、b电极均为石墨电极并加以必要的连接,则连接后的装置应为____________(填“原电池”或“电解池”);该装置工作时,溶液中阴离子向________极作定向移动(填“a”或“b”); 经过一段时间后,停止反应并搅匀溶液,溶液的酸性__________ (填“增强”、“降低”或“不变”)。
②若a、b电极加以导线连接,且a极为铜电极,则b极可以为________电极(填序号)。
A.铂 B.铁 C.石墨 D.银 E.锌
该装置工作时,溶液中阴离子向________极作定向移动(填“a”或“b”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二次污染是排入环境中的一次污染物在物理、化学或生物因素的作用下发生变化,或与环境中的其他物质发生反应,生成新的污染物。下列物质①SO2、②NO、③NO2、④HCl、⑤CO2,不易导致二次污染的是( )
A.①②③④⑤B.①③⑤C.④⑤D.④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲醛在医药、染料、香料等行业中都有着广泛的应用。实验室通过下图所示的流程由Mn2O3氧化甲苯制备苯甲醛,试回答下列问题。
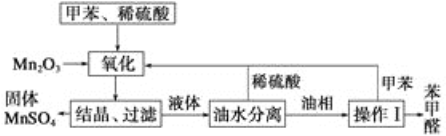
(1)Mn2O3氧化甲苯的反应需要不断搅拌,搅拌的作用是________。
(2)甲苯经氧化后得到的混合物通过结晶、过滤进行分离,该过程中需将混合物冷却,其目的是______。
(3)实验过程中,可循环使用的物质有__________。
(4)实验中分离甲苯和苯甲醛采用的操作Ⅰ是___,其原理是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com