
【题目】四个电解装置都以Pt作电极,它们分别装着如下电解质溶液进行电解,电解一段时间后,测定其pH变化,所记录的结果正确的是
选项 | A | B | C | D |
电解质溶液pH 变化 | HCl | AgNO3 | KOH | BaCl2 |
pH变化 | 减小 | 增大 | 增大 | 不变 |
A. A B. B C. C D. D
科目:高中化学 来源: 题型:
【题目】50mL0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液在如下图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。
回答下列问题:

(1)烧杯间填满碎纸条的作用是_____________________,大烧杯上如不盖硬纸板,求得的中和热数值_________(填“偏大”、“偏小”、“无影响”)。
(2)若用浓硫酸与NaOH溶液反应,则测得的中和热的数值会 ________(填“偏大”、“偏小”、“无影响”)。
(3)实验时所用盐酸及NaOH溶液的密度均为1g·cm3,生成溶液的比热容为:c=4.18 kJ·kg-1·℃-1,实验起始温度为t1℃,终止温度为t2℃。试计算生成1mol水时的焓变:△H=________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物在氧气中充分燃烧,生成水蒸气和二氧化碳的物质的量之比为1︰1,由此可得到结论( )
A.有机物分子中n(C):n(H):n(O)=1:2:3
B.分子中只含碳氢原子且个数比为1:2
C.有机物中必定含有氧元素
D.无法判断有机物中是否含有氧元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组的同学在学习了电化学相关知识后,用如图装置进行实验,请回答下列问题:

(1)实验一:将开关K与a连接,则乙的电极反应式为___。
(2)实验二:开关K与b连接,则总反应的离子方程式为_______。
(3)对于实验二,下列说法正确的是___(填字母)。
A.溶液中Na+向甲极移动
B.从甲极处逸出的气体能使湿润的KI淀粉试纸变蓝
C.反应一段时间后加适量HCl可恢复到电解前电解质的浓度
D.反应在结束后,甲电极和乙电极上收集到的气体体积一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个密闭容器中盛有N2和H2 , 它们的起始浓度分别是1.8mol/L和5.4mol/L,在一定的条件下它们反应生成NH3 , 10min后测得N2的浓度是0.8mol/L,则在这10min内NH3的平均反应速率是( )
A.0.1 mol/(Lmin)
B.0.2 mol/(Lmin)
C.0.3 mol/(Lmin)
D.0.6 mol/(Lmin)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组的同学对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定。回答下列问题:
(1)甲同学运用沉淀法测定样品中NaOH的含量。他选用的药品除样品外,还应有____。
(2)乙同学运用滴定法测定样品中NaOH的含量。
①用分析天平准确称取该样品12.00 g,全部溶于水配制成250.0 mL的溶液。用碱式滴定管取其中25.00 mL放在锥形瓶中,滴加几滴指示剂,待测。滴定管在使用前除洗涤外,还应_____________。
②用浓度为1.00 0 mol·L-1的盐酸标准溶液进行滴定。开始滴定前的一步操作是_________。
③滴定过程中用pH计测定锥形瓶中溶液的pH,临近滴定终点时测定pH应每滴一滴测一次。
④滴定过程中,锥形瓶中溶液的pH变化如下
V(HCl/mL | 0.00 | 12.00 | 18.00 | 22.00 | 23.00 | 23.96 | 25.00 | 25.02 | 26.00 | 27.00 | 30.00 |
pH | 13.1 | 12.6 | 12.2 | 11.7 | 11.4 | 9.9 | 7.0 | 4.0 | 2.7 | 2.4 | 1.9 |
请在右边坐标图中绘制出上述中和滴定的曲线。____________

⑤下表是几种酸碱指示剂的变色范围,根据你作出的中和滴定曲线分析,上述中和滴定中应选用的指示剂是______。
指示剂 | 变色范围(pH) | 颜色 | |
酸色 | 碱色 | ||
甲基橙 | 3.1~4.4 | 红 | 黄 |
石蕊 | 5.0~8.0 | 红 | 蓝 |
酚酞 | 8.2~10.0 | 无 | 红 |
⑥样品中,NaOH的质量百分含量为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫、铁的化合物有广泛的应用。
(1)过二硫酸铵(NH4)2S2O8可以看成双氧水的衍生物,H2O2分子中的两个H原子被—SO3H基取代后即为过二硫酸。
①(NH4)2S2O8中硫元素的化合价为_________;
②用过二硫酸铵溶液检测废水中的Mn2+,配平下面的离子反应:
__S2O82-+__Mn2++__=___MnO4-+__SO42-+____。
(2)大苏打的成分是Na2S2O3·5H2O,常用于防毒面具中吸收氯气。若1 mol Na2S2O3完全反应,失去8mol电子。写出其水溶液吸收氯气的离子方程式______________。
(3)磁性材料A是由两种元素组成的化合物,某研究小组按如图所示流程探究其组成:
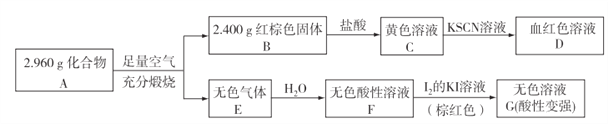
①A的化学式为____________;
②已知化合物A能与盐酸反应,生成一种淡黄色不溶物和一种气体(标准状况下密度为1.518g/L),写出该反应的离子方程式:_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com