
| A、乙醇和浓硫酸混合加热,制乙烯 |
| B、从石油中提炼汽油 |
| C、用蒸馏方法提纯水 |
| D、实验室制取溴苯 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
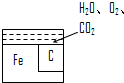 (1)维生素C的结构简式是
(1)维生素C的结构简式是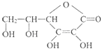 ,维生素C的分子式是
,维生素C的分子式是查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水的电离度α(25℃)>α(35℃) |
| B、c(H+)随着温度的降低而升高 |
| C、在35℃时,纯水中c(H+)>c(OH-) |
| D、水的电离过程是吸热过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、υ(D)=0.4 mol/(L?s) |
| B、υ(C)=0.6mol/(L?s) |
| C、υ(B)=0.5mol/(L?s) |
| D、υ(A)=0.15 mol/(L?s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
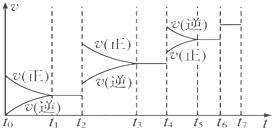
查看答案和解析>>
科目:高中化学 来源: 题型:
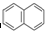 ②
② ③
③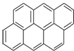 ④
④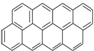 …该系列化合物中所含碳的质量分数最大值是( )
…该系列化合物中所含碳的质量分数最大值是( )| A、93.8% | B、95.7% |
| C、97.3% | D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、光化学烟雾是氮氧化物受紫外线照射后与空气中的…些碳氢化合物作用后生成的一种有毒烟雾 |
| B、“煤改气”、“煤改电”等清洁燃料改造工程有利于减少雾霾天气 |
| C、绿色化学的核心是应用化学原理对环境污染进行治理 |
| D、航天飞机上使用的隔热陶瓷瓦,大多是以碳纤维做增强体的新型复合材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com