
| A. | C2H4和C3H6的混合物的质量为ag,所含碳氢键数目为aNA/7 | |
| B. | 标准状况下,2.24L 2H35Cl中所含中子数为1.8NA | |
| C. | 50mL 12mol•L-1盐酸与足量MnO2共热,转移的电子数为0.3NA | |
| D. | 1L 0.1mol•L-1的NaHCO3溶液中$HC{{O}_{3}}^{-}$和$C{{O}_{3}}^{2-}$的离子数之和为0.1NA |
分析 A.C2H4和C3H6的最简式为CH2,所以ag混合物中含有最简式CH2的物质的量为:$\frac{a}{14}$mol,ag混合物中含有$\frac{a}{14}$molC原子、$\frac{a}{7}$molH原子,每个氢原子形成1个碳氢键;
B.2H35Cl中含有中子数为19;
C.二氧化锰只能与浓盐酸反应,和稀盐酸不反应;
D.碳酸氢根离子水解生成碳酸,电离生成碳酸根离子.
解答 解:A.每个氢原子形成1个碳氢键,ag混合物中总共含有$\frac{a}{7}$molH原子,所以含有$\frac{a}{7}$molH原子碳氢键,所含碳氢键数目为$\frac{a}{7}$NA,故A正确;
B.标准状况下,2.24L 2H35Cl物质的量为0.1mol,中所含中子数为1.9NA,故B错误;
C.二氧化锰只能与浓盐酸反应,和稀盐酸不反应,即盐酸不能反应完全,故转移的电子数小于0.3NA个,故C错误;
D.碳酸氢根离子水解生成碳酸,电离生成碳酸根离子,依据碳原子个数守恒可知:1L 0.1mol•L-1的NaHCO3溶液中$HC{{O}_{3}}^{-}$和$C{{O}_{3}}^{2-}$的离子数之和小于0.1NA,故D错误;
故选:A.
点评 本题考查了阿伏伽德罗常数的应用,熟悉以物质的量为核心的有关计算公式、明确盐类水解规律及物质所含原子、分子、质子、电子、中子数目关系是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 用水鉴别1-丙醇、甲苯和硝基苯 | |
| B. | 用燃烧法鉴别甲醇、苯和四氯化碳 | |
| C. | 用酸性高锰酸钾溶液鉴别苯和甲苯 | |
| D. | 用溴水鉴别乙苯、苯酚、环己烷和乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


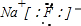 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O是一种非常稳定的化合物,这是由于氢键所致 | |
| B. | 原子晶体中,共价键的键长越短,键能越大,熔点就越高 | |
| C. | 分子晶体中,共价键键能越大,该分子的熔沸点就越高 | |
| D. | 分子晶体中,分子间作用力越大,则分子越稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用钢瓶储存液氯或浓硫酸 | |
| B. | 通过灼热的铜网以除去H2中混有的O2 | |
| C. | Cu与浓硫酸反应终止后,冷却,向试管中加适量蒸馏水以观察水合铜离子的颜色 | |
| D. | 用广泛pH试纸测得某溶液的pH为3.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铯的密度比钠大,熔点比钠高 | |
| B. | 氢氧化铯易溶于水 | |
| C. | 铯能与热水反应放出氢气,但与冷水不反应 | |
| D. | 铯与氯形成共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14组 | B. | 20组 | C. | 26组 | D. | 32组 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2和 盐酸; Ba(OH)2 和 H2SO4 | |
| B. | BaCl2 和 Na2SO4; Ba(OH)2 和 (NH4)2SO4 | |
| C. | NaHCO3和 H2SO4; Ca(HCO3)2 和 HNO3 | |
| D. | Ba(OH)2 和 HNO3; Cu(OH)2 和 H2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com