
【题目】实验室利用如图所示的装置及药品制取氨气。

(1)A中发生反应的化学方程式为__________________。
(2)B中盛放的试剂名称为___________________。
(3)C为用集气瓶收集氨气的装置,请绘出完装置图___________________。
(4)证明氨气已收集满的操作和现象为_____________。
【答案】Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O 碱石灰
CaCl2+2NH3↑+2H2O 碱石灰  将湿润的红色石蕊试纸靠近C右侧的导管口,试纸变蓝色
将湿润的红色石蕊试纸靠近C右侧的导管口,试纸变蓝色
【解析】
实验室制氨气用Ca(OH)2和NH4Cl固体加热制取,由于NH3遇水显碱性,干燥NH3需要使用碱石灰;由于NH3密度比空气小,且极易溶于水,所以用向下排空气法收集。
(1)A中是实验室制取氨气的反应,反应方程式为: Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
(2)根据分析,干燥氨气一般使用碱石灰,所以B里面的试剂为碱石灰。
(3)根据分析,氨气的密度比空气小,且极易溶于水,不能使用排水法收集,可以用向下
排空气法收集,因此C中的装置图需要用一个正立的集气瓶,导管要短进长出,图像为: 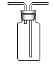
(4)氨气溶于水显碱性:NH3+H2O ![]() NH3·H2O
NH3·H2O ![]() NH4++OH-,可使湿润的石蕊试纸变蓝。因此操作为:将湿润的红色石蕊试纸靠近C右侧的导管口,试纸变成蓝色。
NH4++OH-,可使湿润的石蕊试纸变蓝。因此操作为:将湿润的红色石蕊试纸靠近C右侧的导管口,试纸变成蓝色。


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:
【题目】几种无机物之间转化关系如下图(反应条件省略。部分产物省略)。下列推断不正确的是
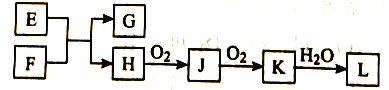
A. 若L为强碱,则E可能为NaCl溶液、F为钾
B. 若L为强酸,则E可能为NaHS、F为HNO3
C. 若L为弱酸,则E可能为Mg、F为CO2
D. 若L为强酸,则E可能为NH4Cl、F为Ca(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】解释下列事实的方程式不正确的是
A. 次氯酸钙溶液中通入过量二氧化硫:Ca2+ + 2ClO-+ H2O + SO2=CaSO3↓+ 2HClO
B. 硫酸型酸雨放置一段时间溶液的pH下降:2H2SO3+O2=2H2SO4
C. 纯碱液可以清洗油污的原因:CO32+H2O![]() HCO3+OH
HCO3+OH
D. 向K2Cr2O7溶液中加入少量NaOH浓溶液,溶液由橙色变为黄色:Cr2O72—+H2O![]() 2CrO42—+2H+
2CrO42—+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组同学对乙醛与新制的Cu(OH)2反应的实验进行探究。
实验Ⅰ:取2mL 10%的氢氧化钠溶液于试管中,加入5滴2%的CuSO4溶液和5滴5%的乙醛溶液,加热时蓝色悬浊液变黑,静置后未发现红色沉淀。
实验小组对影响实验Ⅰ成败的因素进行探究:
(1)探究乙醛溶液浓度对该反应的影响。
编号 | 实验Ⅱ | 实验Ⅲ |
实验方案 |
|
|
实验现象 | 加热,蓝色悬浊液变红棕色,静置后底部有大量红色沉淀 | 加热,蓝色悬浊液变红棕色,静置后上层为棕黄色油状液体,底部有少量红色沉淀 |
已知:乙醛在碱性条件下发生缩合反应:CH3CHO+CH3CHO![]() CH3CH=CHCHO+H2O ,生成亮黄色物质,加热条件下进一步缩合成棕黄色的油状物质。
CH3CH=CHCHO+H2O ,生成亮黄色物质,加热条件下进一步缩合成棕黄色的油状物质。
① 能证明乙醛被新制的Cu(OH)2 氧化的实验现象是______。
② 乙醛与新制的Cu(OH)2 发生反应的化学方程式是______。
③ 分析实验Ⅲ产生的红色沉淀少于实验Ⅱ的可能原因:______。
(2)探究NaOH溶液浓度对该反应的影响。
编号 | 实验Ⅳ | 实验Ⅴ |
实验方案 |
|
|
实验现象 | 加热,蓝色悬浊液变黑 | 加热,蓝色悬浊液变红棕色, 静置后底部有红色沉淀 |
依据实验Ⅰ→Ⅴ,得出如下结论:
ⅰ. NaOH溶液浓度一定时,适当增大乙醛溶液浓度有利于生成Cu2O。
ⅱ. 乙醛溶液浓度一定时,______。
(3)探究NaOH溶液浓度与乙醛溶液浓度对该反应影响程度的差异。
编号 | 实验Ⅵ | 实验Ⅶ |
实验方案 |
|
|
实验现象 | 加热,蓝色悬浊液变黑 | 加热,静置后底部有红色沉淀 |
由以上实验得出推论: ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某NaCl溶液样品中含有Na2SO4、CaCl2杂质(该溶液用X表示),除去杂质的实验方案如图所示。

请回答:
(1)溶液B中存在的阳离子为____________,阴离子为___________。
(2)固体C中所含物质的化学式为__________。
(3)溶液D中加入适量盐酸后,大量减少的微粒为__________。
(4)①和②不能调换顺序的理由为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某物质X能发生如下转化,下列有关上述转化关系中物质及其反应的叙述不正确的是

A. 若X为N2或NH3,则A为硝酸
B. 若X为S或H2S,则A为硫酸
C. 若X为非金属单质或非金属氢化物,则A不一定能与金属铜反应生成Y
D. 反应①和②一定为氧化还原反应,反应③一定为非氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用废镀锌铁皮制备磁性Fe3O4胶体粒子及副产物ZnSO4晶体的实验流程如下:

已知:Zn及其化合物的性质与Al及其化合物的性质相似。
(1)用NaOH溶液处理废镀锌铁皮除溶解锌外,另一个作用是_______________。为缩短用NaOH溶液处理废镀锌铁皮的时间,可采取的措施是_____________(答两条)。
(2)加入适量H2O2溶液的主要作用是______________。溶液B中n(Fe2+):n(Fe3+)=______。
(3)在由溶液B制得Fe3O4胶体粒子的过程中,须缓慢滴加稀NaOH溶液并持续通入N2,持续通入N2的原因是_____________________。
(4)请补充完整下列由溶液A获得副产品ZnSO4晶体的实验步骤:
①向溶液A中通入CO2气体,得到Zn (OH)2沉淀;
②______________、洗涤得到沉淀;
③______________;
④将溶液加热浓缩、冷却结晶、过滤、洗涤、干燥即可得到产品。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作及现象能够达成相应实验结论的是( )
选项 | 实验操作及现象 | 结论 |
A | 向某溶液中加入BaCl2溶液,有白色沉淀生成 | 溶液中一定含有 |
B | 向某溶液中加入盐酸,产生能使澄清石灰水变浑浊的无色气体 | 溶液中一定含有 |
C | 向某溶液中先加入盐酸酸化,没有明显现象,再加入BaCl2溶液,有白色沉淀产生 | 溶液中一定含有SO42- |
D | 向5mL饱和氯水中滴加少量0.1 mol/L NaBr溶液,溶液由无色变为橙黄色,再滴加足量0.1 mol/L淀粉-KI溶液,溶液变蓝 | 氧化性强弱:Cl2>Br2>I2 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国是世界上最早制得和使用金属锌的国家。一种以闪锌矿(主要成份是ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:

相关金属离子[c(Mn+)=0.10mol·L–1]形成氢氧化物沉淀的pH范围如下:
金属离子 | Fe3+ | Fe2+ | Zn2+ | Cd2+ |
开始沉淀的pH | 1.5 | 6.3 | 6.3 | 7.4 |
沉淀完全的pH | 2.8 | 8.3 | 8.2 | 9.4 |
回答下列问题:
(1)写出ZnS的电子式__________________________;
焙烧过程中主要反应的化学方程式为__________________________。
(2)滤渣1的成分为:___________________;
(3)试剂Y是_________(只要求填写一种), 调PH值的范围是___________________。
(4)电解硫酸锌溶液制备单质锌时,电解的总反应离子方程式为:___________________。
(5)为将溶液中的Fe2+氧化,试剂X可选用的是_______。(填序号)
A.H2O2 B.H2S C.HNO3 D.O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com