
【题目】研究者设计利用芳香族化合物的特殊性质合成某药物,其合成路线如下(部分反应试剂和条件已省略):

已知:Ⅰ. 
Ⅱ. 
回答下列问题:
(1)B的名称是____________________。
(2)反应②和⑤所属的反应类型分别为____________、_____________。
(3)反应④所需的条件为___________,E分子中官能团的名称为_________________。
(4)反应⑥的化学方程式为________________________________。
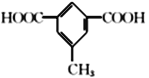
(5)芳香族化合物X是C的同分异构体,X只含一种官能团且1mol X与足量NaHCO3溶液发生反应生成2 molCO2,则X的结构有__________种。其中核磁共振氢谱显示有4组峰,且峰面积之比为3 :2 : 2 :1的结构简式为____________、_____________。
【答案】 )对苯二甲酸 取代反应(或酯化反应) 加成反应 浓硫酸、加热 碳碳双键 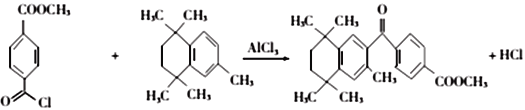 10
10 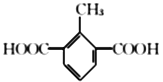
【解析】(1)根据合成流程可知,A被酸性高锰酸钾溶液氧化生成对苯二甲酸,则A为对二甲苯, B为对苯二甲酸;正确答案:对苯二甲酸。
(2)根据对苯二甲酸和D的结构简式可以知道C为![]() ,所以由B到C的反应为酯化反应;对比B与反应(5)的产物结构可以知道,B发生消去反应生成E为
,所以由B到C的反应为酯化反应;对比B与反应(5)的产物结构可以知道,B发生消去反应生成E为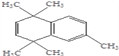 ,反应⑥是E与
,反应⑥是E与![]() 发生加成反应;正确答案:取代反应(或酯化反应); 加成反应。
发生加成反应;正确答案:取代反应(或酯化反应); 加成反应。
(3)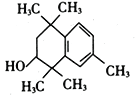 在浓硫酸加热作用下,醇发生消去反应生成E,结构简式为:
在浓硫酸加热作用下,醇发生消去反应生成E,结构简式为: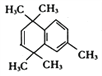 ;分子中含有官能团碳碳双键;正确答案:浓硫酸、加热;碳碳双键。
;分子中含有官能团碳碳双键;正确答案:浓硫酸、加热;碳碳双键。
(4)有机物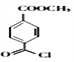 与有机物
与有机物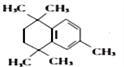 在氯化铝的作用下发生取代反应,化学方程式为:
在氯化铝的作用下发生取代反应,化学方程式为: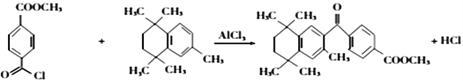 ;正确答案:
;正确答案: 。
。
(5)有机物C为![]() ,芳香族化合物X只含一种官能团,且1mol X与足量NaHCO3溶液发生反应生成2 molCO2,结构中含有2个羧基,满足这样条件的有机物结构有:2个-COOH、1个-CH3分别连在苯环上,结构有6种;1个–COOH、1个-CH2COOH分别连在苯环上,结构有3种;苯环上连有
,芳香族化合物X只含一种官能团,且1mol X与足量NaHCO3溶液发生反应生成2 molCO2,结构中含有2个羧基,满足这样条件的有机物结构有:2个-COOH、1个-CH3分别连在苯环上,结构有6种;1个–COOH、1个-CH2COOH分别连在苯环上,结构有3种;苯环上连有![]() 的结构有1种;共计有10种;其中核磁共振氢谱显示有4组峰,且峰面积之比为3 :2 : 2 :1的结构简式为
的结构有1种;共计有10种;其中核磁共振氢谱显示有4组峰,且峰面积之比为3 :2 : 2 :1的结构简式为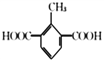 和
和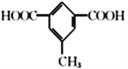 ;正确答案:10;
;正确答案:10; 和
和 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知在25 ℃、101 kPa下,0.5 mol辛烷C8H8燃烧生成二氧化碳和液态水时放出2 759 kJ热量。表示上述反应的热化学方程式正确的是( )
A.C8H18(l)+ ![]() O2(g)=8CO2(g)+9H2O(g) ΔH=-48.40 kJ·mol-1
O2(g)=8CO2(g)+9H2O(g) ΔH=-48.40 kJ·mol-1
B.C8H18(l)+ ![]() O2(g)=8CO2(g)+9H2O(l) ΔH=-5 518 kJ·mol-1
O2(g)=8CO2(g)+9H2O(l) ΔH=-5 518 kJ·mol-1
C.C8H18(l)+ ![]() O2(g)=8CO2(g)+9H2O(l) ΔH=+5 518 kJ·mol-1
O2(g)=8CO2(g)+9H2O(l) ΔH=+5 518 kJ·mol-1
D.2C8H18(l)+25O2(g)=16CO2(g)+18H2O(l) ΔH=+11 036 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,体积一定的密闭容器中进行如下反应:X(g)+Y(g) ![]() Z(g)+W(s), △H>0下列叙述正确的是( )
Z(g)+W(s), △H>0下列叙述正确的是( )
A.加入少量W,逆反应速度增大
B.当容器中气体压强不变时,反应达到平衡
C.升高温度,平衡逆向移动
D.平衡后加入X,上述反应的△H增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是最重要的氮肥,是产量最大的化工产品之一.德国人哈伯在1905年发明了合成氨的方法,其合成原理为:N2(g)+3H2(g) ![]() 2NH3(g) ΔH=-92.4 kJ·mol-1 , 他因此获得了1918年诺贝尔化学奖.在密闭容器中,将2 mol N2和6 mol H2混合发生下列反应:N2(g)+3H2(g)
2NH3(g) ΔH=-92.4 kJ·mol-1 , 他因此获得了1918年诺贝尔化学奖.在密闭容器中,将2 mol N2和6 mol H2混合发生下列反应:N2(g)+3H2(g) ![]() 2NH3(g) ΔH=-92.4 kJ·mol-1。
2NH3(g) ΔH=-92.4 kJ·mol-1。
(1)当反应达到平衡时,N2和H2的浓度比是;N2和H2的转化率比是 . 反应放出的热量(填“大于”“小于”或“等于”)184.8 kJ。
(2)降低平衡体系的温度(保持体积不变),混合气体的平均相对分子质量 , 密度 . 平衡常数K(填“增大”“减小”或“不变”).
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将(填“正向”“逆向”或“不”)移动.
(4)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将(填“向左移动”“向右移动”或“不移动”).达到新平衡后,容器内温度(填“大于”“小于”或“等于”)原来的2倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜的相关化合物在生产生活中具有重要的作用。回答下列问题:
(1)铜元素在周期表中的位置是______________,基态铜原子中,核外电子占据最高能层的符号是_________________,占据该最高能层的电子数为__________________。
(2)在一定条件下,金属相互化合形成的化合物称为金属互化物,如Cu9Al4、Cu5Zn8等。某金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于__________(填“晶体”或“非晶体”)。
(3)铜能与类卤素[(SCN)2]反应生成Cu(SCN)2,1mol(SCN)2分子中含有σ键的数目为______________。 (SCN)2对应的酸有硫氰酸(H-S-C![]() N)、异硫氰酸(H-N=C=S)两种。理论上前者沸点低于后者,其原因是____________________________。
N)、异硫氰酸(H-N=C=S)两种。理论上前者沸点低于后者,其原因是____________________________。
(4)铜晶体中铜原子的堆积方式为面心立方堆积,每个铜原子周围距离最近的铜原子个数为________。
(5)铜与金形成的金属互化物的晶胞结构如图所示,其晶胞边长为a nm,该金属互化物的密度为____________(用含a、NA的代数式表示)g·cm-3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是恒温下H2(g)+I2(g)![]() 2HI(g)+Q(Q>0)的化学反应速率随反应时间变化的示意图,t1时刻改变的外界条件是
2HI(g)+Q(Q>0)的化学反应速率随反应时间变化的示意图,t1时刻改变的外界条件是

A. 升高温度
B. 增大压强
C. 增大反应物浓度
D. 加入催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com