
【题目】X、Y、Z均为短周期主族元素,已知它们的原子序数的关系为X+Z=2Y,且Z的最高价氧化物对应的水化物是强酸。则下列有关说法正确的是
A. 若X是Na,则Z的最高价一定为偶数
B. 若X是O,则YX一定是离子化合物
C. 若Y是O,则非金属性Z>Y>X
D. 若Y是Na,则X、Z不可能是同一主族元素
【答案】B
【解析】
A.X是Na,则Z可为Cl,最高价是奇数,故A错误;B.X是O,因为O原子序数是8,偶数,则Z只能是S,Y的原子序数为![]() 2=12,Y是Mg,MgO是离子化合物,故B正确;C.Y是O,则X+Z=16,只有Z为N,X为F满足,非金属性:F>O>N,即:X>Y>Z,故C错误;D.Y是Na,则X+Z=22,Z可为N,Y为P元素,N和P是同一主族元素,7+15=22满足前述条件,故D错误;故选B。
2=12,Y是Mg,MgO是离子化合物,故B正确;C.Y是O,则X+Z=16,只有Z为N,X为F满足,非金属性:F>O>N,即:X>Y>Z,故C错误;D.Y是Na,则X+Z=22,Z可为N,Y为P元素,N和P是同一主族元素,7+15=22满足前述条件,故D错误;故选B。
点晴:高频考点,注意根据原子序数的关系判断元素的种类是解答该题的关键,原子序数X+Z=2Y,则X和Z的原子序数只能同时为奇数或者同时为偶数,Z的最高价氧化物对应水化物是强酸,Z只能是N,S,Cl(短周期)等元素,以此解答该题。


科目:高中化学 来源: 题型:
【题目】以下过滤操作中,不正确的是( )
A. 滤纸应紧贴漏斗内壁并用少量水润湿,使滤纸与漏斗壁之间没有气泡
B. 漏斗下端管口应紧靠烧杯内壁
C. 倒入漏斗的过滤液的液面应高于滤纸边缘
D. 要沿着玻璃棒慢慢向漏斗中倾倒过滤液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列鉴别方法正确的是( )
A.用澄清石灰水鉴别CO2和SO2
B.用湿润的碘化钾淀粉试纸鉴别Br2(g)和NO2
C.用CO2鉴别NaAlO2溶液和NaClO溶液
D.用Ba(OH)2溶液鉴别Na2CO3溶液和NaHCO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.化学反应不一定都有能量变化
B.增大反应物浓度,活化分子百分数增大,化学反应速率一定增大
C.升高温度,活化分子百分数增大,化学反应速率一定增大
D.一般使用催化剂可以降低反应的活化能,增大活化分子百分数,从而提高反应物的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 干冰、盐酸都是电解质
B. Na2O2、Fe2O3、CaO既属于碱性氧化物,又属于离子化合物
C. 有单质参加或有单质生成的反应不一定属于氧化还原反应
D. 根据是否具有丁达尔效应,可将分散系分为溶液、浊液和胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电影《闪闪的红星》中,为让被困的红军战士吃上食盐,潘冬子将浸透食盐水的棉袄裹在身上,带进山中。假如潘冬子在实验室中,欲从食盐水中提取出食盐,采用的最好方法是:
A.过滤 B.萃取 C.蒸发 D.蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴及其化合物在工业中运用广泛,从某工业废料中制备草酸钴的工业流程如图:
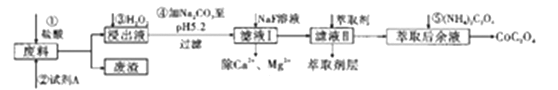
已知:①废料中主要含有三氧化二钴。含少量F2O3、Al2O3、MnO、CaO、SiO2等;
②浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
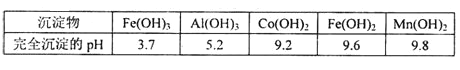
(1)在浸出过程中加入Co2O3与盐酸反应生成气体,此反应的离子方程式为___________________ ;实验室中检验该气体的方法是________________。
(2)加入试剂A的目的是_________________,废渣的主要成分是_______________,在浸出液中先加入双氧水反应,再加入碳酸钠的原因是(试用离子方程式和必要的文字简述其理)___________。
(3)萃取后余液中加入(NH4)2C2O4沉淀Co2+,判断Co2+沉淀完全的操作是____________________。
(4)萃取剂对金属离子的萃取率与pH的关系如下图所示,在滤液II中适宜萃取的pH为_____(填序号)
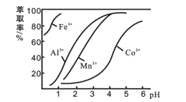
A.接近2.0 B. 接近3.0 C. 接近5.0
(5)在空气中加热CoC2O4固体,经测定,210℃~290℃的过程中只产生CO2和一种化合物,该化合物中钴元素的质量分数为73.44%。此过程发生反应的化学方程式是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3 分子的空间构型是三角锥形,而不是正三角形的平面结构,解释该事实的充分理由是
A.NH3分子是极性分子
B.分子内3个N—H键的键长相等,键角相等
C.NH3分子内3个N—H键的键长相等,3个键角都等于107°
D.NH3分子内3个N—H键的键长相等,3个键角都等于120°
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NOx、CO等大气污染物的测量及处理具有重要意义。
(1)在汽车尾气系统中装置催化转化器,可有效降低NOx的排放。NOx在催化转化器中被CO还原成N2排除。写出NO被CO还原的化学方程式:________________。
(2)选择性催化还原技术(SCR)是目前最成熟的烟气脱硝技术,即在金属催化剂作用下,用还原剂(如NH3)选择性地与NOx反应生成N2和H2O。
①已知:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)△H=-905.5kJmol-1
4NO(g)+6H2O(g)△H=-905.5kJmol-1
N2(g)+O2(g)![]() 2NO(g)△H=+180kJmol-1
2NO(g)△H=+180kJmol-1
完成该方法中主要反应的热化学方程式
4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g)△H=_________________。
4N2(g)+6H2O(g)△H=_________________。
②该方法应控制反应温度在315~400℃之间,反应温度过低会影响反应速率,但温度也不宜过高,原因是___________________。
③氨氮比[n(NH3)/n(NO)]会直接影响该方法的脱硝率。350℃时,只改变氨气的投放量,反应物x的转化率与氨氮比的关系如右图所示,则X是________________ (填化学式)。当n(NH3)/n(NO)>1.0时,烟气中NO浓度反而增大,主要原因是________________ 。

(3)通过NOx传感器可监测NOx的含量,其工作原理示意图如下:

①Pt电极上发生的是______________反应(填“氧化”或“还原”)。
②写出NiO电极的电极反应式:___________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com