
����Ŀ���ܼ��仯�����ڹ�ҵ�����ù㷺����ij��ҵ�������Ʊ������ܵĹ�ҵ������ͼ��
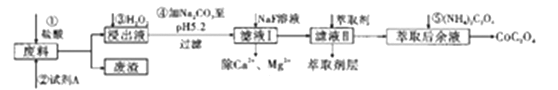
��֪���ٷ�������Ҫ�������������ܡ�������F2O3��Al2O3��MnO��CaO��SiO2�ȣ�
�ڽ���Һ���е���������Ҫ��H+��Co2+��Fe2+��Mn2+��Ca2+��Mg2+��Al3+�ȣ�
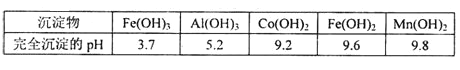
�۲���������������������ʽ����ʱ��Һ��pH���±���
(1)�ڽ��������м���Co2O3�����ᷴӦ�������壬�˷�Ӧ�����ӷ���ʽΪ___________________ ��ʵ�����м��������ķ�����________________��
(2)�����Լ�A��Ŀ����_________________����������Ҫ�ɷ���_______________���ڽ���Һ���ȼ���˫��ˮ��Ӧ���ټ���̼���Ƶ�ԭ����(�������ӷ���ʽ�ͱ�Ҫ�����ּ�������)___________��
(3)��ȡ����Һ�м���(NH4)2C2O4����Co2+���ж�Co2+������ȫ�IJ�����____________________��
(4)��ȡ���Խ������ӵ���ȡ����pH�Ĺ�ϵ����ͼ��ʾ������ҺII��������ȡ��pHΪ_____(�����)
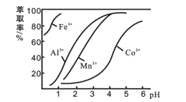
A.�ӽ�2.0 B. �ӽ�3.0 C. �ӽ�5.0
(5)�ڿ����м���CoC2O4���壬���ⶨ��210�桫290��Ĺ�����ֻ����CO2��һ�ֻ�����û���������Ԫ�ص���������Ϊ73.44%���˹��̷�����Ӧ�Ļ�ѧ����ʽ��________________________��
���𰸡�Co2O3+6H++2Cl��=2Co2++Cl2��+3H2O��ʪ��ĵ��۵⻯����ֽ����ȷ��Co3+��ȫ����ԭ��Co2+SiO2��Fe2+����ΪFe3+���ټ����̼���ƣ���![]() ����H+��Ӧ��
����H+��Ӧ��![]() ���ͣ�ʹFe3+��Al3+����R3+���棩��ˮ��ƽ��R3++3H2O
���ͣ�ʹFe3+��Al3+����R3+���棩��ˮ��ƽ��R3++3H2O![]() R(OH)3+3H+�����ƶ�����������������������ú����ϲ���Һ������(NH4)2C2O4�������������B3CoC2O4+2O2
R(OH)3+3H+�����ƶ�����������������������ú����ϲ���Һ������(NH4)2C2O4�������������B3CoC2O4+2O2![]() Co3O4+6CO2
Co3O4+6CO2
��������
(1)�ڽ��������м���Co2O3�����ᷴӦ����CoCl2��Cl2��������Ӧ�����ӷ���ʽΪCo2O3+6H++2Cl��=2Co2++Cl2��+3H2O��ʵ����ͨ����ʪ��ĵ��۵⻯����ֽ���飬����ֽ����ɫ����֤��������Ϊ������
(2)������Լ�AӦ����Fe����Ŀ����Ϊ��ȷ��Co3+��ȫ����ԭ��Co2+�������к���SiO2������ϡ���ᣬ���÷�������Ҫ�ɷ���SiO2���ڽ���Һ���ȼ���˫��ˮ��Ӧ��ʹ��Һ�е�Fe2+��ȫ����ΪFe3+���ټ����̼���ƣ���CO32-����H+��Ӧ�� c(H+)���ͣ�ʹFe3+��Al3+����R3+���棩��ˮ��ƽ��R3++3H2O![]() R(OH)3+3H+�����ƶ����������������������
R(OH)3+3H+�����ƶ����������������������
(3)��ȡ����Һ�м���(NH4)2C2O4����Co2+�������ú����ϲ���Һ������(NH4)2C2O4������������ֿ��ж�Co2+������
(4)��ͼʾ��֪����ҺpH=3����ʱ��Fe3+��Al3+��Mn2+����ȡ����ߣ���Co2+����ȡ�ʽϵͣ��ʴ�ΪB��
��5���û�������Co����������Ϊ73.44%����Co�UO��ԭ�Ӹ�����Ϊ![]() =3�U4����û�����Ļ�ѧʽΪCo3O4���ʷ���ʽΪ3CoC2O4+2O2_
=3�U4����û�����Ļ�ѧʽΪCo3O4���ʷ���ʽΪ3CoC2O4+2O2_![]() Co3O4+6CO2��
Co3O4+6CO2��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͭ��һ����Ũ���ᷴӦ���õ�����ͭ��Һ��NO2��N2O4��NO�Ļ�����壬��Щ������1.68 L O2����״������Ϻ�ͨ��ˮ�У�����������ȫ��ˮ�����������ᡣ������������ͭ��Һ�м���5 mol/L NaOH��Һ��Cu2+ǡ����ȫ������������NaOH��Һ�������
A��60 mL B��45 mL C��30 mL D��15 mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
�Թ�����Ϊ�����������������V2O5���ǽӴ�����������Ĵ������ӷϷ������л���V2O5�ȱ�����Ⱦ��������������Դ�ۺ����á��Ϸ���������Ҫ�ɷ�Ϊ��
���� | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
��������/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
������һ�ַϷ��������չ���·�ߣ�
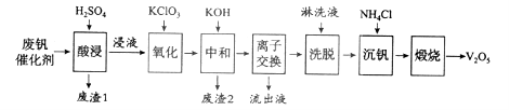
�ش��������⣺
��1���������ʱV2O5ת��ΪVO2+����Ӧ�����ӷ���ʽΪ___________��ͬʱV2O4ת��VO2+��������1������Ҫ�ɷ���__________________��
��2��������������ʹ3 mol��VO2+��ΪVO2+������Ҫ������KClO3����Ϊ______mol��
��3�����к�������֮һ��ʹ����V4O124��ʽ��������Һ�С�������2���к���_______��
��4�������ӽ���������ϴ�����ɼ�ʾΪ��4ROH+ V4O124![]() R4V4O12+4OH��ROHΪǿ���������ӽ�����֬����Ϊ�����ϴ��Ч�ʣ���ϴҺӦ�ó�_____�ԣ���������������������������
R4V4O12+4OH��ROHΪǿ���������ӽ�����֬����Ϊ�����ϴ��Ч�ʣ���ϴҺӦ�ó�_____�ԣ���������������������������
��5��������Һ����������������________��
��6�����������õ�ƫ����泥�NH4VO3��������д�����������з�����Ӧ�Ļ�ѧ����ʽ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��Ϊ����������Ԫ�أ���֪���ǵ�ԭ�������Ĺ�ϵΪX+Z=2Y����Z������������Ӧ��ˮ������ǿ�ᡣ�������й�˵����ȷ����
A. ��X��Na����Z�����һ��Ϊż��
B. ��X��O����YXһ�������ӻ�����
C. ��Y��O����ǽ�����Z��Y��X
D. ��Y��Na����X��Z��������ͬһ����Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����ʵ����ʺ�Ӧ����ȷ���ǣ�������
A. �������ֿ����ڱ��溣�ʲ�Ʒ
B. ��֬�����������¿�ˮ�����ɸ�֬�������
C. �Ҵ�������͵����ʶ�����������Ӫ������
D. �ϳ�������ά�������л��߷��Ӳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧѡ��5���л���ѧ����]
����������һ����Ҫ��ʳ���㾫����ͼ��ϳ����ķ�Ӧ·�ߣ�
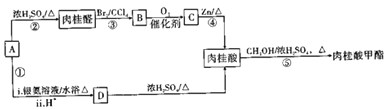
��֪��I.�����廯����A�ķ���ʽΪC9H10O2����ֻ��-������������ÿ��C�����ֻ��һ�������ţ�
��. lmol A��ȫ�������IJ���ֻ����1molNaOH��ȫ��Ӧ
(1) A�Ľṹ��ʽΪ_______________�����ȩ�ķ���ʽΪ_______________��
(2)�����ϳ�·����ʹ�âڢ۲���Ӧ��Ŀ����_________________��
(3)�ڢݲ���Ӧ�Ļ�ѧ����ʽΪ___________________________��
(4)д��A��������Һ��Ӧ�Ļ�ѧ����ʽ��_______________________��
(5)D�����к��ж��ֹ����ţ����ܷ����ķ�Ӧ������__________������ţ���
a.������Ӧ b.ȡ����Ӧ c.�Ӿ۷�Ӧ
d.ˮ�ⷴӦ e.��ȥ��Ӧ f.������Ӧ
(6) д�������������������ȩ��ͬ���칹�壺_________________(����3��)��
��.��������
��.����̼ԭ��һ����ͬһƽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йػ��������������ȷ����
A. ��֬������Ԫ�أ��������Ǻ������Ԫ��
B. ά����D����֬�ʣ��ܴٽ������Լغ�������
C. ����˫�����Լ�������ɫ��Ӧ��ֻ�е�����
D. ����DNA��RNA��ϸ�������У�DNA���Ŵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I����ҵ����һ����C02�������״�ȼ�ϵķ�����
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ��H=-49.0kJmol-1
CH3OH(g)+H2O(g) ��H=-49.0kJmol-1
��6 mol CO2��8 mol H2����2 L���ܱ������У����H2�����ʵ�����ʱ��仯����ͼ��ʾ(ʵ��)��ͼ������a(1��6)��ʾ����1 minʱH2�����ʵ�����6 mol��
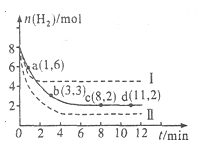
��1��a������Ӧ���� (����ڡ������ڡ���С�ڡ�)�淴Ӧ���ʡ�
��2������ʱ���ƽ����Ӧ���������� ��
A��O��1 min B��1��3 min C��3��8 min D��8��11 min
��3�����ı�ijһʵ�������ٽ�������ʵ����H2�����ʵ�����ʱ��仯��ͼ����ʾ�����ߣ�������I��Ӧ��ʵ�������ı��� �����ߢ��Ӧ��ʵ�������ı��� ����������ٳ���3molCO2��4 mol H2,H2O(g)��������� ����������䡱��С������
��4������1molCO2��3molH2����������У���ַ�Ӧ�ﵽƽ�����CO2ת����Ϊa,�������ڵ�ѹǿ����ʼѹǿ֮��Ϊ ��
��.��ҵ�ϻ����ں����ܱ������в������з�Ӧ�ϳɼ״���CO��g��+2H2��g��![]() CH3OH��g�� ��H
CH3OH��g�� ��H
��1���жϷ�Ӧ�ﵽƽ��״̬�������� ��
A��2v(H2)(��)=v(CO)(��)
B�����������ܶȲ���
C����������ƽ����Է�����������
D��CH3OH��CO��H2��Ũ�ȶ����ٷ����仯
E��������CO��H2��CH3OH��Ũ��֮��Ϊ1:2:1
��2����һ���¶��£�����4a mol H2��2amol CO����2L���ܱ������У���ַ�Ӧ����CO��ת����Ϊ50������÷�Ӧ��ƽ�ⳣ��Ϊ ������ʱ�����������Ͷ��a mol CO��2amol H2��amol CH3OH���ж�ƽ���ƶ��ķ����� ���������ƶ����������ƶ������ƶ���������ԭƽ����ȣ�CO�����ʵ���Ũ�� ������������䡱��С������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ�������ɺ����������ʹ������
A��AlCI3 B��KHCO3 C��Fe2(SO4)3 D��NH4HCO3
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com