
����Ŀ���л���A��G�Ľṹ��ʽ�ֱ�Ϊ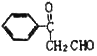 ��
��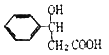 ��������һ����Ҫ���л��ϳ��м��壬D��FΪ�߷��ӻ����
��������һ����Ҫ���л��ϳ��м��壬D��FΪ�߷��ӻ����
��1��д���л���G���������ֺ��������ŵ�����_______________��
��2���л���G���Է�������ͼ��ת������ش��������⣺

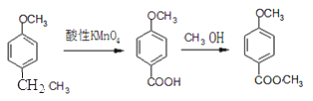
��ɷ�Ӧ��ѡ�õ��Լ�����Ϊ___________________________________________����Ӧ�ܵķ�Ӧ������___________________________________________��
д�����з�Ӧ�Ļ�ѧ����ʽ��
��Ӧ��____________________________________��
��Ӧ��____________________________________��
��Ӧ��____________________________________��
��3��G��һ��ͬ���칹��![]() ��һ��ҽҩ�м��塣����ƺ���������
��һ��ҽҩ�м��塣����ƺ���������![]() �ϳ�
�ϳ�![]() ������ԭ����ѡ���÷�Ӧ����ͼ��ʾ����ע����Ҫ�ķ�Ӧ������������:
������ԭ����ѡ���÷�Ӧ����ͼ��ʾ����ע����Ҫ�ķ�Ӧ������������: ![]()
__________________________________________________��
���𰸡� �������ǻ����Ȼ� �������ƻ�̼���ƻ�̼��������Һ�� ��ȥ��Ӧ ![]()
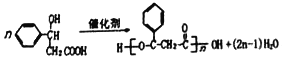
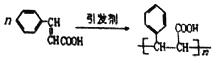
��������(1)�л���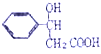 ���������ֺ��������ŵ�����(��)�ǻ����Ȼ���
���������ֺ��������ŵ�����(��)�ǻ����Ȼ���
(2)���ǻ����Ȼ�������Na��Ӧ�����Ȼ�������NaOH��Na2CO3��Ӧ����Ӧ��ѡ�õ��Լ�����Ϊ �������ƻ�̼���ƻ�̼��������Һ�ȣ���Ӧ���� ������ȥ��Ӧ���ɱ���ϩ����
������ȥ��Ӧ���ɱ���ϩ����
��Ӧ����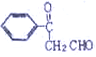 ������������ͭ���ã��䷴Ӧ����ʽΪ
������������ͭ���ã��䷴Ӧ����ʽΪ![]() ��
��
��Ӧ���� �������۷�Ӧ���䷴Ӧ����ʽΪ
�������۷�Ӧ���䷴Ӧ����ʽΪ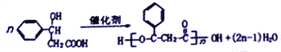 ��
��
��Ӧ���DZ���ϩ�ᷢ���Ӿ۷�Ӧ���䷴Ӧ����ʽΪ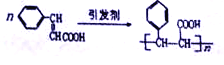 ��
��
(3)��![]() Ϊԭ�Ϻϳ�
Ϊԭ�Ϻϳ�![]() ������ͼΪ
������ͼΪ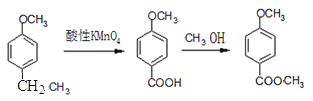 ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������1mol ���ڿ�������ȫȼ�գ�����Һ̬ˮ���ų�����Q���÷�Ӧ���Ȼ�ѧ����ʽ�ǣ� ��
A. C6H6+15/2O2��6CO2+3H2O+Q
B. C6H6(l)+15/2O2(g)��6CO2(g)+3H2O(l)-Q
C. C6H6(g)+15/2O2(g)��6CO2(g)+3H2O(g)+Q
D. 2C6H6(l)+15O2(g)��12CO2(g)+6H2O(l)+2Q
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ȼ���г���CaF2����ʽ���ڡ�
(1)�����й�CaF2�ı�����ȷ����________��
a��Ca2����F��������ھ�����������
b��F�������Ӱ뾶С��Cl������CaF2���۵����CaCl2
c���������ӱ�Ϊ2��1�����ʣ�����CaF2���幹����ͬ
d��CaF2�еĻ�ѧ��Ϊ���Ӽ������CaF2������״̬���ܵ���
(2)CaF2������ˮ���������ں�Al3������Һ�У�ԭ����_________________________________(�����ӷ���ʽ��ʾ)��
��֪��AlF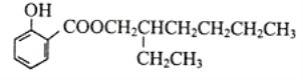 ����Һ�п��ȶ����ڡ�
����Һ�п��ȶ����ڡ�
(3)F2ͨ��ϡNaOH��Һ�п�����OF2��OF2�����д��ڵĻ�ѧ������________��OF2�ĵ���ʽ________��
(4)F2������±�ص��ʷ�Ӧ�����γ�±�ػ��������ClF3��BrF3�ȡ���֪��ӦCl2(g)��3F2(g)===2ClF3(g)����H����313 kJ��mol��1��F��F���ļ���Ϊ159 kJ��mol��1��Cl��Cl���ļ���Ϊ242 kJ��mol��1����ClF3��Cl��F����ƽ������Ϊ________kJ��mol��1 ��ClF3���ۡ��е��BrF3��________(����������������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ᴿ��������Ba(NO3)2���ʵ�KNO3��Һ����ʹ�õķ���Ϊ
A���������Na2CO3��Һ�����ˣ���ȥ��������Һ�в�����������
B���������K2SO4��Һ�����ˣ���ȥ��������Һ�в�����������
C���������Na2SO4��Һ�����ˣ���ȥ��������Һ�в�����������
D���������K2CO3��Һ�����ˣ���ȥ��������Һ�в�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ɫ���ļ�����Һ�У��ܴ����������������
A�� Na+��K+��CO32����NO3�� B��Cu2+��Al3+��SO42����NO3��
C�� K+��Fe2+��NH4+��NO3�� D��NH4+��Na+��NO3����Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��![]()
ˮ������EΪ�������ռ������������Ʒ�ɹ˪��E��һ�ֺϳ�·�����£�
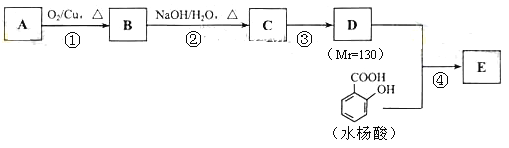
��ش��������⣺
��1��һԪ��A��������������ԼΪ21.6%����A�ķ���ʽΪ ���ṹ������ʾAֻ��һ������A������Ϊ ��
��2��B�������Ƶ�Cu(OH)2������Ӧ���÷�Ӧ�Ļ�ѧ����ʽΪ ��
��3��C�� �ֽṹ����һ��ȡ��������C�����������ţ���ʹ�õ��Ⱥ�˳��д�������Լ� ��
��4�������ķ�Ӧ����Ϊ ��D���������ŵ�����Ϊ ��
��5��д��ͬʱ��������������ˮ��������ͬ���칹��Ľṹ��ʽ�� ��
A�������к���6��̼ԭ����һ������
B�����������������Ű���ˮ������еĹ�����
��6���������ķ�Ӧ����Ϊ ��д��E�Ľṹ��ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ȲΪԭ�ϣ�ͨ����ͼ��ʾ�����ܺϳ�һ�ָ߷��ӵ���G��ת�������еIJ��ַ�Ӧ���������ֲ�������ȥ����

����A��B��C��D�ֱ����һ���л��B����������
��֪��-C��CH+ 
![]()
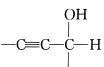

��ش��������⣺
��1��A��B�Ļ�ѧ��Ӧ������______��
д��B��C�Ļ�ѧ��Ӧ����ʽ��____________��
��2��E ��H2��ȫ�ӳɵõ������ʵĽṹ��ʽ��____________��
��3��д����������������E��ͬ���칹��________��
�ٺ��б��� ���������� �ۿɷ���������Ӧ �ܱ����������ֲ�ͬ������H��
��4������˵����ȷ����______������ĸ���ţ���
A�����������У���Ȳ���л���B���л���E���ɷ����ۺϷ�Ӧ
B.�л���E��ʹ����KMnO4��Һ��ɫ����˵��E��̼̼˫��
C.�л���C������Ϊ����ȩ�����л�ԭ��
D. 35%��40%�ļ�ȩ��HCHO����Һ�׳Ƹ���������Һ����ʹ�����ʱ���
��5����Ȼ��ά����ʪ�����ںϳ���ά�����кϳ���ά����ʪ�ԽϺõ���____������ĸ���ţ���
A����������ά�����ڣ� B.������ά�����ڣ�
C������ϩ������ȩ��ά��ά�ڣ� D���۱�ϩ��ά�����ڣ�
��6����д��F����G�Ļ�ѧ��Ӧ����ʽ_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ԭ�ӹ������������ȷ��
A. ��ԭ�ӵ�2s���������3p�ܼ���
B. �ԭ�ӵ�2s��5s �����Ϊ���ηֲ�
C. p�ܼ���ԭ�ӹ���ʷĴ��Σ������ܲ����������ӣ�p�ܼ�ԭ�ӹ��Ҳ������
D. �ܲ�n��4��ԭ�ӹ����������16������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������и������������̷���FeSO4��7H2O��,��������ȴ���Ƶ�һ����ɫճ����Һ�塰�̷��͡���������ʣ��Ĺ���Ϊ����ɫ��������и���:
��1���̷��������ʵĻ�ѧʽΪ________________________��
��2������ͼװ��ģ�������з�Ӧ�������������̷�һ��ʱ�����D��U�ܳ�����ɫճ����Һ�壬b��Ʒ����Һ��ɫ��

����װ����ȷ������˳��A��_________________________���ô�д��ĸ��ʾ)
��д�������̷��Ļ�ѧ����ʽ________________________________________��
��ʵ������в��˼�������̷�����Ҫԭ����__________________________________
��3����������ʵ�����ɱȽ�ijЩ���ӵĻ�ԭ�ԡ�������ϡ���ὫA��ʣ��Ĺ����ܽ⣬�քeȡ2mL����Һ��2֧�Թ��н�������ʵ�飺
�ٵ�һ֧�Թ��м����������Ը��������Һ�������������Һ��ɫ����ȥ��˵����������в�����____________��
�ڵڶ�֧�Թ��м�������C����Һ�����������ɣ�
�ۼ�����ڶ�֧�Թ��м�������____________��Һ��������ɫ������
����ʵ�������֤�����ӵĻ�ԭ��____________>____________���������ӷ��ţ�
��4���̷��ڿ����в��ֱ�����Ϊ����������ȡ3.66g�̷���Ʒ����ϡ���ᣬ����������BaCl2��Һ�����˵ó���4.66g������Һ��ͨ��56mL����״��������ǡ�ý�Fe2+��ȫ�������Ʋ⾧����n(Fe2+)��n(Fe3+)��n(H2O)=��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com