
ЁОЬтФПЁПЛиД№ЯТСаЮЪЬтЃК
1LКЃЫЎдкж№НЅХЈЫѕЙ§ГЬжаЮіГібЮЕФжжРрКЭжЪСПЃЈЕЅЮЛЃКgЃЉЕФЙиЯЕШчЯТБэЫљЪОЃК
КЃЫЎУмЖШ(gmL-1) | CaSO4 | NaCl | MgCl2 | MgSO4 | NaBr |
1.21 | 0.05 | 3.26 | 0.004 | 0.008 | ЁЊ |
1.22 | 0.015 | 9.65 | 0.01 | 0.012 | ЁЊ |
1.26 | 0.01 | 2.64 | 0.02 | 0.02 | 0.04 |
1.31 | ЁЊ | 1.40 | 0.54 | 0.03 | 0.06 |
зЂЃКЛЁАЁЊЁБЕФЪ§ОнЩйгк10-4ЃЌПЩвдКіТдВЛМЦЁЃ
(1)ДгКЃЫЎжаЛёЕУДжбЮЃЌвЛАуВЩгУЕФЗНЗЈЪЧ___ЁЃ
(2)ИљОнЩЯБэЃЌвЊЛёЕУдгжЪНЯЩйЕФЪГбЮЃЌгІПижЦКЃЫЎЕФзюМбУмЖШЮЊ___gmL-1ЃЈЬюзжФИЃЉЁЃ
AЃЎ1.21 BЃЎ1.22 CЃЎ1.26 DЃЎ1.31
(3)ДжбЮжаГЃКЌгаMgCl2ЁЂMgSO4ЁЂCaCl2ЕШдгжЪЃЌвЊГ§ШЅетаЉдгжЪЃЌАДЫГађМгШыЕФЪдМСвРДЮЮЊNaOHЁЂBaCl2ЁЂ___ЁЂ___ЕШЃЈЬюЛЏбЇЪНЃЉЁЃ
(4)ЙЄвЕЩЯЕчНтШлШкТШЛЏФЦжЦШЁН№ЪєФЦЕФЛЏбЇЗНГЬЪНЮЊ___ЁЃ
(5)ФЦдЊЫиЕФвЛжжГЃМћбѕЛЏЮяПЩзїЮЊКєЮќУцОпЕФЙЉбѕМСЃЌаДГіИУбѕЛЏЮяКЭCO2ЗДгІЕФЛЏбЇЗНГЬЪН___ЁЃ
ЁОД№АИЁПеєЗЂЛђШеЩЙ B Na2CO3 HCl 2NaCl(ШлШк)![]() 2NaЃЋCl2Ёќ 2Na2O2+2CO2=2Na2CO3+O2
2NaЃЋCl2Ёќ 2Na2O2+2CO2=2Na2CO3+O2
ЁОНтЮіЁП
(1)дкКЃЫЎж№НЅХЈЫѕЙ§ГЬжаЃЌКЃЫЎжаЕФФГаЉбЮЕФХЈЖШЛсЗЂЩњвЛЖЈЕФИФБфЃЌБэжаЪ§жЕЮЊЮіГібЮЕФжЪСПЃЌЫљвдвЊЛёШЁФГжжбЮЃЌгІбЁдёЦфЮіГіСПЖрЕФЕуЁЃ
(2)Г§ШЅДжбЮжаЕФдгжЪЃЌФГаЉЪдМСЕФМгШыДцдквЛЖЈЕФЫГађЃЌвВОЭЪЧЯШМгШыЕФЪдМСЃЌЙ§СПВПЗжашвЊКѓМгШыЪдМСШЅГ§ЁЃЖдДжбЮЬсДПРДЫЕЃЌгыДЫЯрЙиЕФЪдМСЮЊNa2CO3КЭHClЃЌЫљвдNa2CO3БиаыдкМгШыBaCl2жЎКѓМгШыЃЌHClБиаыдкЙ§ТЫжЎКѓМгШыЁЃ
(1)ДгКЃЫЎжаЛёЕУДжбЮЃЌГЃашдіДѓХЈЖШЃЌШУбЮЫЎБфЕУБЅКЭЃЌЫљвдвЛАуВЩгУЕФЗНЗЈЪЧеєЗЂЛђШеЩЙЁЃД№АИЮЊЃКеєЗЂЛђШеЩЙЃЛ
(2)ИљОнБэжааХЯЂЃЌвЊЛёЕУдгжЪНЯЩйЕФЪГбЮЃЌгІПижЦКЃЫЎЕФзюМбУмЖШЮЊ1.22gmLЃ1ЃЌетЪБЮіГіЪГбЮзюЖрЃЌдгжЪзюЩйЃЌвђДЫбЁBЁЃД№АИЮЊЃКBЃЛ
(3)ДжбЮжаГЃКЌгаMgCl2ЁЂMgSO4ЁЂCaCl2ЕШдгжЪЃЌМгNaOHгУРДГ§ШЅMg2+ЃЌМгШыBaCl2Г§ШЅSO42-ЃЌгІМгШыNa2CO3Г§ШЅЙ§СПЕФBa2+КЭдгаЕФCa2+ЃЌзюКѓМгШыбЮЫсГ§ШЅЙ§СПЕФCO32-ЃЌвЊГ§ШЅетаЉдгжЪЃЌАДЫГађМгШыЕФЪдМСвРДЮЮЊNaOHЁЂBaCl2ЁЂNa2CO3ЁЂHClЁЃД№АИЮЊЃКNa2CO3ЃЛHClЃЛ
(4)ЙЄвЕЩЯЕчНтШлШкТШЛЏФЦжЦШЁН№ЪєФЦЃЌЛЏбЇЗНГЬЪНЮЊ2NaCl(ШлШк)![]() 2NaЃЋCl2ЁќЁЃД№АИЮЊЃК2NaCl(ШлШк)
2NaЃЋCl2ЁќЁЃД№АИЮЊЃК2NaCl(ШлШк)![]() 2NaЃЋCl2ЁќЃЛ
2NaЃЋCl2ЁќЃЛ
(5)Й§бѕЛЏФЦПЩзїЮЊКєЮќУцОпЕФЙЉбѕМСЃЌЫќКЭCO2ЗДгІЕФЛЏбЇЗНГЬЪН2Na2O2 + 2CO2 == 2Na2CO3 + O2ЁЃД№АИЮЊЃК2Na2O2 + 2CO2 == 2Na2CO3 + O2ЁЃ


 ЬьЬьЯђЩЯвЛБОКУОэЯЕСаД№АИ
ЬьЬьЯђЩЯвЛБОКУОэЯЕСаД№АИ аЁбЇЩњ10ЗжжггІгУЬтЯЕСаД№АИ
аЁбЇЩњ10ЗжжггІгУЬтЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПШєЦјЬЌЬўDЕФУмЖШЮЊ1.25 g/L(БъзМзДПі)ЃЌИїжжЮяжЪМфзЊЛЏЙиЯЕШчЯТЃК
A![]() B
B![]() CЃЛA
CЃЛA![]() D
D![]() EЁЃ
EЁЃ
(1)аДГіAЁЋEЕФНсЙЙМђЪНЃК
A_______ЃЌB_________ЃЌC_________ЃЌD_______ЃЌE________ЁЃ
(2)аДГіЯТСаЗДгІЕФЛЏбЇЗНГЬЪНЃК
AЁњBЃК__________________ЃЛ
BЁњCЃК__________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊЯТСаЪ§ОнЃК
ЮяжЪ | ШлЕу/Ёц | ЗаЕу/Ёц | УмЖШ/ |
ввДМ |
| 78.3 | 0.79 |
ввЫс | 16.6 | 117.9 | 1.05 |
ввЫсввѕЅ |
| 77 | 0.90 |
ФГбЇЩњдкЪЕбщЪвжЦШЁввЫсввѕЅЕФжївЊВНжшШчЯТЃК
ЂйХфжЦ![]() ХЈСђЫсЁЂ
ХЈСђЫсЁЂ![]() ввДМЃЈКЌ
ввДМЃЈКЌ![]() ЃЉКЭ
ЃЉКЭ![]() ввЫсЕФЛьКЯШмвКЁЃ
ввЫсЕФЛьКЯШмвКЁЃ
ЂкАДШчЭМСЌНгКУзАжУЃЈзАжУЦјУмадСМКУЃЉВЂМгШыЛьКЯвКЃЌгУаЁЛ№ОљдШМгШШ![]() ЁЃ
ЁЃ
ЂлД§ЪдЙмввЪеМЏЕНвЛЖЈСПВњЮяКѓЭЃжЙМгШШЃЌГЗГіЪдЙмввВЂгУСІеёЕДЃЌШЛКѓОВжУД§ЗжВуЁЃ
ЂмЗжРыГіввЫсввѕЅЃЌЯДЕгЁЂИЩдяЁЃ
(1)ХфжЦЂйжаЛьКЯШмвКЕФЗНЗЈЮЊ_______________________________ЃЛЗДгІжаХЈСђЫсЕФзїгУЪЧ____________________________ЃЛаДГіжЦШЁввЫсввѕЅЕФЗДгІЕФЛЏбЇЗНГЬЪНЃК____________________________ЃЈБъГі![]() ЃЉЁЃ
ЃЉЁЃ
(2)ЩЯЪіЪЕбщжаБЅКЭЬМЫсФЦШмвКЕФзїгУЪЧ________ЃЈЬюзжФИЃЉЁЃ
A.жаКЭввЫсКЭввДМ B.жаКЭввЫсВЂЮќЪеввДМ
C.МѕЩйввЫсввѕЅЕФШмНт D.МгЫйѕЅЕФЩњГЩЃЌЬсИпЦфВњТЪ
(3)ВНжшЂкжаашвЊаЁЛ№ОљдШМгШШЃЌЦфжївЊдвђЪЧ____________________________ЃЛВНжшЂлЫљЙлВьЕНЕФЯжЯѓЪЧ_______________________________________ЃЛгћНЋввЪдЙмжаЕФЮяжЪЗжРывдЕУЕНввЫсввѕЅЃЌБиаыЪЙгУЕФвЧЦїга___________ЃЛЗжРыЪБЃЌввЫсввѕЅгІДгвЧЦї_____________ЃЈЬюЁАЯТПкЗХЁБЛђЁАЩЯПкЕЙЁБЃЉГіЁЃ
(4)ИУЭЌбЇЗДИДЪЕбщЃЌЕУГіввДМгыввЫсЕФгУСПКЭЕУЕНЕФввЫсввѕЅЩњГЩСПШчЯТБэЃК
ЪЕбщ | ввДМ/ | ввЫс/ | ввЫсввѕЅ/ |
Ђй | 2 | 2 | 1.33 |
Ђк | 3 | 2 | 1.57 |
Ђл | 4 | 2 | x |
Ђм | 5 | 2 | 1.76 |
Ђн | 2 | 3 | 1.55 |
БэжаЪ§ОнxЕФЗЖЮЇЪЧ__________________ЃЛЪЕбщЂйЂкЂнЬНОПЕФЪЧ_____________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЖдгкБНввЯЉЃЈ![]() )ЕФЯТСаа№ЪіЂйФмЪЙЫсадKMnO4ШмвКЭЪЩЋЁЂЂкПЩЗЂЩњМгОлЗДгІЁЂЂлПЩШмгкЫЎЁЂЂмПЩШмгкБНжаЁЂЂнФмгыХЈЯѕЫсЗЂЩњШЁДњЗДгІЁЂЂоЫљгаЕФдзгПЩФмЙВЦНУцЃЌЦфжае§ШЗЕФЪЧЃЈ ЃЉ
)ЕФЯТСаа№ЪіЂйФмЪЙЫсадKMnO4ШмвКЭЪЩЋЁЂЂкПЩЗЂЩњМгОлЗДгІЁЂЂлПЩШмгкЫЎЁЂЂмПЩШмгкБНжаЁЂЂнФмгыХЈЯѕЫсЗЂЩњШЁДњЗДгІЁЂЂоЫљгаЕФдзгПЩФмЙВЦНУцЃЌЦфжае§ШЗЕФЪЧЃЈ ЃЉ
A.НіЂйЂкЂмЂнB.НіЂйЂкЂнЂоC.НіЂйЂкЂмЂнЂоD.ШЋВПе§ШЗ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЛЊЗЈСж(Warfarin)гжУћЩБЪѓСщЃЌЮЊаФбЊЙмМВВЁЕФСйДВвЉЮяЁЃЦфКЯГЩТЗЯп(ВПЗжЗДгІЬѕМўТдШЅ)ШчЯТЫљЪОЃК
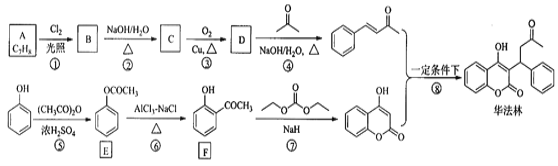
ЛиД№ЯТСаЮЪЬт:
(1)AЕФУћГЦЮЊ________ЃЌEжаЙйФмЭХУћГЦЮЊ________ЁЃ
(2)BЕФНсЙЙМђЪНЮЊ________ЁЃ
(3)гЩCЩњГЩDЕФЛЏбЇЗНГЬЪНЮЊ___________
(4)ЂнЕФЗДгІРраЭЮЊ_________ЃЌЂрЕФЗДгІРраЭЮЊ________ЁЃ
(5)FЕФЭЌЗжвьЙЙЬхжаЃЌЭЌЪБЗћКЯЯТСаЬѕМўЕФЭЌЗжвьЙЙЬхЙВга___________жжЁЃ
aЃЎФмгыFeCl3ШмвКЗЂЩњЯдЩЋЗДгІ bЃЎКЌга-CHO
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвЛЖЈЮТЖШЯТЃЌдкШ§ИіЬхЛ§ОљЮЊ2.0 LЕФКуШнУмБеШнЦїжаЗЂЩњЗДгІЃКPCl5(g)![]() PCl3(g)+Cl2(g)ЁЃ
PCl3(g)+Cl2(g)ЁЃ
БрКХ | ЮТЖШ /Ёц | Ц№ЪМЮяжЪ ЕФСП/mol | ЦНКтЮяжЪ ЕФСП/mol | ДяЕНЦНКт ЫљашЪБМф/s | |
PCl5(g) | PCl3(g) | Cl2(g) | |||
Ђё | 320 | 0.40 | 0.10 | 0.10 | t |
Ђђ | 320 | 0.80 | t1 | ||
Ђѓ | 410 | 0.40 | 0.15 | 0.15 | t2 |
ЯТСаЫЕЗЈе§ШЗЕФЪЧ
A.ЦНКтГЃЪ§KЃКШнЦїЂђ>ШнЦїЂѓ
B.ЗДгІЕНДяЦНКтЪБЃЌPCl5ЕФзЊЛЏТЪЃКШнЦїЂђ>ШнЦїЂё
C.ЗДгІЕНДяЦНКтЪБЃЌШнЦїЂёжаЕФЦНОљЫйТЪЮЊv(PCl5)=![]() molЁЄL-1ЁЄs-1
molЁЄL-1ЁЄs-1
D.Ц№ЪМЪБЯђШнЦїЂѓжаГфШыPCl5 0.30 molЁЂPCl3 0.45 molКЭCl2 0.10 molЃЌдђЗДгІНЋЯђФцЗДгІЗНЯђНјаа
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЖўдЊЫс(ЛЏбЇЪНгУH2XБэЪО)дкЫЎжаЕФЕчРыЗНГЬЪНЪЧЃКH2XЃНHЃЋЃЋHXЃ HXЃ![]() HЃЋЃЋX2Ѓ,ГЃЮТЯТЃЌЯђ10 mL 0.1000 mol/LЕФH2XШмвКжаж№ЕЮМгШы0.1000 mol/LЕФNaOHШмвКЃЌpHЫцNaOHШмвКЬхЛ§ЕФБфЛЏШчЭМЫљЪОЁЃЯТСаа№Ъіжае§ШЗЕФЪЧ
HЃЋЃЋX2Ѓ,ГЃЮТЯТЃЌЯђ10 mL 0.1000 mol/LЕФH2XШмвКжаж№ЕЮМгШы0.1000 mol/LЕФNaOHШмвКЃЌpHЫцNaOHШмвКЬхЛ§ЕФБфЛЏШчЭМЫљЪОЁЃЯТСаа№Ъіжае§ШЗЕФЪЧ
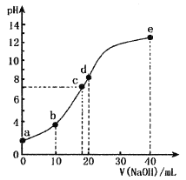
A.aЕуpH>1
B.bЕуШмвКжаЃКc(NaЃЋ)>c(HXЃ)>c(X2Ѓ)>c(H2X)>c(HЃЋ)>c(OHЃ)
C.dЕуШмвКжаЃКc(NaЃЋ)ЃН2c(X2Ѓ)ЃЋ2c(HXЃ)
D.ЫЎЕФЕчРыГЬЖШЃКc>a>e
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЬњЕФаэЖрЛЏКЯЮядкЩњВњЁЂЩњЛюжагазХЙуЗКЕФгІгУЃЌШчFeCl3ЪЧживЊЕФН№ЪєЪДПЬМСЁЂЫЎДІРэМСЃЛгАЪгзїЦЗХФЩужаГЃгУFe(SCN)3ШмвКФЃФтбЊвКЃЛFeSПЩгУгкЯћГ§ЫЎжажиН№ЪєЮлШОЕШЁЃ
ЃЈ1ЃЉвбжЊЃКЂй3Cl2(g)+2Fe(s)=2FeCl3(s) ІЄH1=akJЁЄmol-1
Ђк2FeCl2(s)+Cl2(g)=2FeCl3(s) ІЄH2=bkJЁЄmol-1
дђ2FeCl3(s)+Fe(s)=3FeCl2(s) ІЄH3=____ЁЃ
ЃЈ2ЃЉНЋc(FeCl3)=0.2molЁЄL-1ЕФШмвКгыc(KSCN)=0.5molЁЄL-1ЕФШмвКАДЕШЬхЛ§ЛьКЯгкФГУмБеШнЦїЗЂЩњЗДгІЃКFeCl3+3KSCN![]() Fe(SCN)3+3KClЃЌВтЕУГЃЮТЯТШмвКжаc(Fe3+)ЕФХЈЖШЫцзХЪБМфЕФБфЛЏШчЭМ1ЫљЪОЃЛВтЕУВЛЭЌЮТЖШЯТt1ЪБПЬЪБШмвКжаc[Fe(SCN)3]ШчЭМ2ЫљЪОЁЃ
Fe(SCN)3+3KClЃЌВтЕУГЃЮТЯТШмвКжаc(Fe3+)ЕФХЈЖШЫцзХЪБМфЕФБфЛЏШчЭМ1ЫљЪОЃЛВтЕУВЛЭЌЮТЖШЯТt1ЪБПЬЪБШмвКжаc[Fe(SCN)3]ШчЭМ2ЫљЪОЁЃ
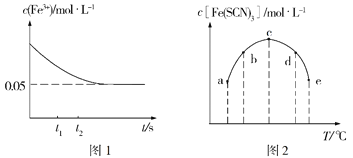
ЂйбаОПБэУїЃЌЩЯЪіЗДгІДяЕНЦНКтКѓЃЌЯђЬхЯЕжаМгШыЪЪСПKClЙЬЬхКѓЃЌШмвКбеЩЋЮоБфЛЏЃЌЦфдвђЪЧ___ЃЌИљОнЭМ1ЗжЮіЃЌдкt1ЁЂt2ЪБПЬЃЌЩњГЩFe3+ЕФЫйТЪНЯДѓЕФЪЧ____ЪБПЬЁЃ
ЂкГЃЮТЯТFe3++3SCN-![]() Fe(SCN)3ЕФЦНКтГЃЪ§ЕФжЕдМЮЊ___ЃЌЦфЫќЬѕМўВЛБфЪБЃЌШєЯђШнЦїжаМгЪЪСПеєСѓЫЎЃЌдђаТЦНКтНЈСЂЙ§ГЬжаv(е§)___v(Фц)ЃЈЬюЁАЃОЁБЁАЃМЁБЛђЁА=ЁБЃЉЁЃ
Fe(SCN)3ЕФЦНКтГЃЪ§ЕФжЕдМЮЊ___ЃЌЦфЫќЬѕМўВЛБфЪБЃЌШєЯђШнЦїжаМгЪЪСПеєСѓЫЎЃЌдђаТЦНКтНЈСЂЙ§ГЬжаv(е§)___v(Фц)ЃЈЬюЁАЃОЁБЁАЃМЁБЛђЁА=ЁБЃЉЁЃ
ЂлИљОнЭМ2ХаЖЯЃЌИУЗДгІЕФІЄH___0ЃЈЬюЁАЃОЁБЛђЁАЃМЁБЃЉЃЌЭМжаЮхИіЕуЖдгІЕФзДЬЌжаЃЌвЛЖЈДІгкЗЧЦНКтЬЌЕФЪЧ___ЃЈЬюЖдгІзжФИЃЉЁЃ
ЃЈ3ЃЉРћгУFeSПЩГ§ШЅЗЯЫЎжаЕФжиН№ЪєРызгЃЌШчгУFeSНЋPb2+зЊЛЏЮЊPbSПЩЯћГ§Pb2+дьГЩЕФЮлШОЃЌЕБзЊЛЏДяЕНЦНКтзДЬЌЪБЃЌЗЯЫЎжаc(Fe2+)=___c(Pb2+)[ЬюОпЬхЪ§ОнЃЌвбжЊKsp(PbS)=8ЁС10-28ЃЌKsp(FeS)=6ЁС10-18]ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊЗДгІЃКЂйCl2+2KBr=2KCl+Br2ЃЛЂкKClO3+6HCl=3Cl2Ёќ+KCl+3H2OЃЛЂл2KBrO3+Cl2=Br2+2KClO3ЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧЃК(ЁЁЁЁ)
A.ЂйжаKCl ЪЧбѕЛЏВњЮяЃЌKBrЗЂЩњЛЙдЗДгІ
B.бѕЛЏадгЩЧПЕНШѕЕФЫГађЮЊKBrO3>KClO3>Cl2>Br2
C.ЗДгІЂкжабѕЛЏМСгыЛЙдМСЕФЮяжЪЕФСПжЎБШЮЊ1ЃК6
D.Ђлжа1 molбѕЛЏМСВЮМгЗДгІЕУЕНЕчзгЕФЮяжЪЕФСПЮЊ2.5 mol
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com