
短周期元素A、B、C、D、E原子序数依次增大,A与C可形成A2C2和A2C两种化合物;B的最高价氧化物对应的水化物甲与其气态氢化物乙反应可生成盐丙;D与A位于同一主族;在同周期元素形成的简单离子中,E的离子半径最小。
(1)实验室中可用A2C2制取C单质,其化学方程式是
(2)由A、C、D三种元素组成的化合物的电子式是 ;B、C、E三种元素组成的常见盐的水溶液呈酸性,原因是 (用离子方程式表示)。
(3)反应乙+C2→B2+A2C(未配平)可设计为燃料电池,则通入乙的电极是 (填“正”或“负”)极,在碱性条件下其电极反应是
【知识点】元素周期律,电池
【答案解析】(每空2分)
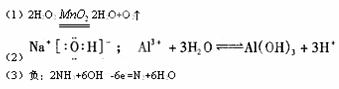
解析:(1)根据A与C可形成A2C2和A2C两种化合物,推断A为H,C为O,B的最高价氧化物对应的水化物甲与其气态氢化物乙反应可生成盐丙,推断B为N,丙为硝酸铵,D与A同一主族,原子序数大于C,所以D为Na,实验室用过氧化氢制取氧气的方程式为: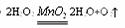
(2)A、C、D组成的物质为NaOH,其电子式为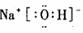
BCE形成的化合物为硝酸铝,铝离子水解使溶液显酸性,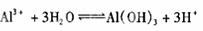
(3)燃料电池中,燃料作负极,因此氨气为负极,在碱性条件下其电极反应是: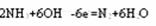
【思路点拨】本题考查元素周期律相关内容,推断出各元素是关键,再结合燃料电池正负极判断及电极反应式的书写,难度较大。


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物。某同学通过如下实验探究 反应原理并验证产物。
反应原理并验证产物。
实验I:用砂纸擦去镁条表面氧化膜,将其放入盛适量滴有酚酞的饱和碳酸氢钠溶液的烧杯中,迅速反应,产生大量气泡和白色不溶物,溶液的浅红色加深。
(1)该同学对反应中产生的白色不溶物做出如下猜测:
猜测1:白色不溶物可能为
猜测2:白色不溶物可能为MgCO3
猜测3:白色不溶物可能为碱式碳酸镁[yMg(OH )2•xMgCO3]
)2•xMgCO3]
(2)为了确定产物,进行以下定性实验:
| 实验序号 | 实 验 | 实验现象 | 结 论 |
| 实验Ⅱ | 将实验I中收集到的气体点燃 | 安静燃烧, 火焰呈淡蓝色 | 气体成分为 ① |
| 实验Ⅲ | 将实验I中的白色不溶物滤出、洗涤,取少量加入足量 ② |
③ | 白色不溶物中含有MgCO3 |
| 实验Ⅳ | 取实验Ⅲ中的滤液,向其中加入适 量 ④ 稀溶液 | 产生白色沉淀,溶液红色变浅 | 溶液中存在CO32- 离子 |
实验Ⅲ中洗涤的操作方法是  。
。
(3)为进一步确定实验I的白色不溶物的成分,进行以下定量实验,装置如图所示:
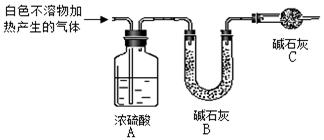
称取干燥、纯净的 白色不溶物 4.52 g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中。实验后装置A增重0.36 g,装置B增重1.76 g。
白色不溶物 4.52 g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中。实验后装置A增重0.36 g,装置B增重1.76 g。
装置C的作用是 ;
白色不溶物的化学式为 。
(4)写出镁与饱和碳酸氢钠溶液反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
从海带中提取碘的实验过程中,涉及到下列操作,其中正确的是(考察每一个操作时,假设其它操作均正确)( )
|
|
|
|
|
A.将海带灼烧成灰 B.过滤得合I—溶液 C.放出碘的苯溶液 D.分离碘并回收苯
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中微粒浓度关系一定正确的是( )
A.常温下,氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH4+)
B.常温下,pH=2的一元酸和pH=12的一元强碱等体积混合: c(OH-)=c(H+)
C.0.1 mol·L—1的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+)
D.0.1 mol·L—1的硫化钠溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S)
查看答案和解析>>
科目:高中化学 来源: 题型:
关于化学键的下列叙述中,不正确的是
A、含有共价键的化合物一定是共价化合物
B、共价化合物中一定含有共价键
C、含有离子键的化合物一定是离子化合物
D、双原子单质分子中的共价键一定是非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
反应 H2(g) + I2(g)  2HI(g)的平衡常数K1 ,反应 HI(g)
2HI(g)的平衡常数K1 ,反应 HI(g) 
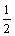 H2(g)+
H2(g)+ 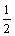 I2(g)的
I2(g)的
平衡常数K2 ,则K1、K2的关系为(平衡常数为同温度下的测定值)
A.K1=2K2 B.K1=K22 C.K1=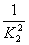 D.K1=
D.K1=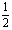 K2
K2
查看答案和解析>>
科目:高中化学 来源: 题型:
根据反应:①2C-+A2===2A-+C2;②2B-+D2===2D-+B2;③2A-+B2===2B-+A2。推断A-、B-、C-、D-的还原能力由强到弱的顺序是 ( )
A.A->B->C->D-
B.D->B->A->C-
C.D->A->B->C-
D.C->A->B->D-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com