
| A. | 苯使溴水褪色 | |
| B. | 长时间放置的KI溶液变棕色 | |
| C. | 将Na2CO3溶液点在红色石蕊试纸上,试纸变蓝 | |
| D. | 向KSCN与FeCl3的混合溶液中加入FeCl3晶体,溶液颜色加深 |
分析 A.苯能萃取溴水中的溴;
B.碘离子能被空气中的氧气氧化;
C.Na2CO3在溶液中水解显碱性;
D.KSCN与FeCl3反应生成Fe(SCN)3.
解答 解:A.苯能萃取溴水中的溴,属于物理变化,与氧化还原反应无关,故A错误;
B.长时间放置的KI溶液变棕色,是因为碘离子能被空气中的氧气氧化,所以与氧化还原反应有关,故B正确;
C.Na2CO3在溶液中水解显碱性,碱性溶液使红色石蕊试纸变蓝,没有发生氧化还原反应,故C错误;
D.KSCN与FeCl3反应生成Fe(SCN)3,属于复分解反应,与氧化还原反应无关,故D错误.
故选B.
点评 本题考查氧化还原反应,明确颜色变化涉及的化学反应是解答的关键,注意酸碱指示剂的变色和反应的实质,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用双缩脲试剂可区分蛋白质溶液和淀粉溶液 | |
| B. | 用水可区分苯,甲苯和溴苯 | |
| C. | 用高锰酸钾酸性溶液可区分乙烷和乙烯 | |
| D. | 用溴水可鉴别苯酚溶液,2-己烯和甲苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2的结构式:H-O-O-H | B. | C2H4的结构简式:CH2CH2 | ||
| C. | O2-结构示意图: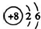 | D. | CCl4的结构式: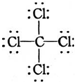 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气溶于水的离子方程式:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液,若溶液变成蓝色,则氧化性:Cl2>I2 | |
| C. | 为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可 | |
| D. | 漂白粉在空气中久置变质是因为漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
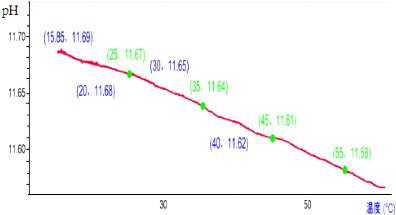
| A. | 随着温度升高溶液中c(OH-)不断减小 | |
| B. | 加热促进CO32-水解和水的电离,溶液中c(OH-)随温度升高而增大 | |
| C. | 溶液pH减小的原因是:加热促进水的电离,Kw随温度升高而增大 | |
| D. | 25℃时CO32-的水解程度约为100.67% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
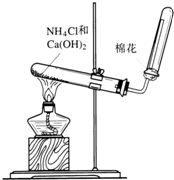 如图是实验室制取氨气的装置图.请回答:
如图是实验室制取氨气的装置图.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | H-Cl的键能为432 kJ/mol,H-F的键能明显高于432 kJ/mol | |
| B. | 0.1 mol/L氨水中NH3•H2O部分电离,一定温度下该氨水的电离度为55% | |
| C. | 某Ca(OH)2溶液的浓度为0.5 mol/L | |
| D. | 十六烷的裂化产物中不饱和烃的分子数超过50% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com