
| A.三种途径所消耗的铜的物质的量相等 |
| B.三种途径所消耗的硝酸的物质的量相等 |
| C.所消耗的铜的物质的量是:途径(3)>途径(1)>途径(2) |
| D.所消耗的硝酸的物质的量是:途径(1)>途径(2)>途径(3) |
科目:高中化学 来源:不详 题型:单选题
 调控。
调控。 装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。
装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。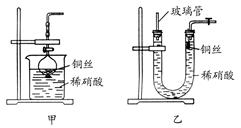
| A.铁 | B.铝 |
| C.铂 | D.玻璃 |
 状况下________mL O2才能使NO全部溶于水。
状况下________mL O2才能使NO全部溶于水。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.15mol | B.0.225mol | C.0.3mol | D.无法计算 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氨气可以用碱石灰干燥也可用无水CaCl2干燥 |
| B.氨水能导电,所以NH3是电解质 |
| C.沸点:NH3<PH3<AsH3 |
| D.用水吸收NH3用下图装置可防止倒吸: |

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ,则c(H2)= ,20min内,用N2浓度的变化表示的反应速率为 。
,则c(H2)= ,20min内,用N2浓度的变化表示的反应速率为 。 )∶n(NH3)=1∶3∶2
)∶n(NH3)=1∶3∶2 SO4+2NH3+CO2+H2O= CaCO3+(NH4)2SO4
SO4+2NH3+CO2+H2O= CaCO3+(NH4)2SO4查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.N2和H2在Pt作用下反应生成NH3 | B.NH4Cl和Ca(OH)2反应生成NH3 |
| C.NO2和水制硝酸 | D.由NH3制氮肥 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 求回答下列问题:
求回答下列问题:查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NH3中混有少量水蒸气:通过装有浓硫酸的洗气瓶 |
| B.NO中混有少量NO2气体:用水洗涤后再干燥 |
| C.食盐中混有少量NH4Cl:加过量烧碱溶液后加热蒸干 |
| D.硝酸混有少量硫酸:加适量BaCl2后再过滤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com