
【题目】W、M、X、Y、Z是周期表前36号元素中的五种常见元素,其原子序数依次增大。W的一种核素在考古时常用来鉴定一些文物的年代;M的氧化物是导致酸雨的主要物质之一。X的某一种单质是大气污染物监测物之一;Y的基态原子核外有6个原子轨道处于半充满状态;Z能形成红色的Z2O和黑色的ZO两种氧化物。
(1)Y3+基态的电子排布式可表示为___。
(2)MX![]() 的空间构型__(用文字描述)。
的空间构型__(用文字描述)。
(3)MH3极易溶于水的原因是___。
(4)根据等电子原理,WX分子的结构式为___。
(5)1molWX2中含有的σ键数目为__。
(6)H2X分子中X原子轨道的杂化类型为___。
(7)向Z2+的溶液中加入过量NaOH溶液,可生成Z的配位数为4的配位离子,该配位离子为___。
【答案】1s22s22p63s23p63d3(或[Ar]3d3) 平面三角形 NH3分子与H2O分子间形成氢键 C≡O 2×6.02×1023个(或2NA) sp3杂化 Cu(OH)![]()
【解析】
根据题干信息可知:W、M、X、Y、Z是周期表前36号元素,其原子序数依次增大,W的一种核素在考古时常用来鉴定一些文物的年代,故W为C;M的氧化物是导致酸雨的主要物质之一,M可能是N或者S,X的某一种单质是大气污染物监测物之一则X为O,故M只能是N;Y的基态原子核外有6个原子轨道处于半充满状态即3d54s1,故Y为Cr;Z能形成红色的Cu2O和黑色的CuO两种氧化物,故Z为Cu;综上所述:W、M、X、Y、Z分别是C、N、O、Cr、Cu五种元素。
(1)Y为Cr,故Y3+基态的电子排布式可表示为1s22s22p63s23p63d3(或[Ar]3d3),答案为:1s22s22p63s23p63d3(或[Ar]3d3);
(2)MX![]() 即NO
即NO![]() ,由于NO
,由于NO![]() 中N原子形成了三个σ键且没有孤对电子,其与三氟化硼是等电子体,故其的空间构型为平面三角形,答案为:平面三角形;
中N原子形成了三个σ键且没有孤对电子,其与三氟化硼是等电子体,故其的空间构型为平面三角形,答案为:平面三角形;
(3)MH3即NH3极易溶于水的原因是由于NH3与H2O均为极性分子,二者相似相溶,且NH3分子与H2O分子间形成氢键,故答案为:由于NH3与H2O均为极性分子,二者相似相溶,且NH3分子与H2O分子间形成氢键;
(4)根据等电子原理,WX即CO分子与N2互为等电子体,故CO的结构式为C≡O,答案为:C≡O;
(5)根据WX2即CO2的结构简式O=C=O可知,1mol中含有CO2的σ键数目为2mol,答案为:2×6.02×1023个(或2NA);
(6)H2X分子即H2O中O原子与H原子形成2个σ键,且O周围有2对孤对电子,故其杂化类型为sp3杂化,答案为:sp3;
(7)Cu2+与OH-之间形成配位键,又知生成Z的配位数为4的配位离子,故该配位离子为Cu(OH)![]() ,答案为:Cu(OH)
,答案为:Cu(OH)![]() 。
。


科目:高中化学 来源: 题型:
【题目】以辉铜矿(Cu2S)为原料冶炼铜,其反应原理可表示为Cu2S+O2![]() 2Cu+SO2。下列说法不正确的是( )
2Cu+SO2。下列说法不正确的是( )
A.化合价发生变化的元素有3种
B.Cu2S在该反应中既是氧化剂又是还原剂
C.1 mol O2参加反应时,上述反应转移电子总物质的量为4 mol
D.SO2被分离、回收后氧化生成SO3,作为制取硫酸的原料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于铝热反应的现象有如下描述:反应放出大量的热,并发出耀眼的光芒;纸漏斗的下部被烧穿,有熔融物落入沙中。已知![]() 、
、![]() 、
、![]() 、
、![]() 的熔点、沸点如表所示:
的熔点、沸点如表所示:
物质 |
|
|
|
|
熔点/℃ | 660 | 1565 | 2054 | 1535 |
沸点/℃ | 2467 | 3414 | 2980 | 2750 |
(1)某同学推测,铝热反应所得到的熔融物是铁铝合金,因为该反应放热能使铁熔化,而铝的熔点比铁的低,此时液态的铁和铝形成铁铝合金。你认为他的解释是否合理?________(填“合理”或“不合理”)。
(2)设计一个简单的实验,证明上述熔融物中含有金属铝,填写下列表格:
①所用试剂 | ______ |
②实验操作及现象 | ______ |
③有关反应的化学方程式 | ______ |
(3)欲在常温下溶解该熔融物,下列试剂中最好选用______(填序号),理由是_________________________。
a.浓硫酸 b.稀硫酸 c.硫酸锌溶液d. ![]() 溶液
溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制汞的过程是:焙烧辰砂(主要含HgS),发生反应:HgS+O2![]() Hg+SO2还原出的汞呈气态,冷凝得液态汞。其流程如图,下列说法不正确的是
Hg+SO2还原出的汞呈气态,冷凝得液态汞。其流程如图,下列说法不正确的是
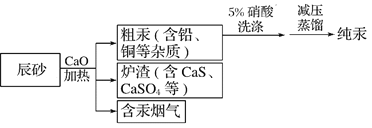
A. 洗涤粗汞时可用5%的盐酸代替5%的硝酸
B. HgS+O2![]() Hg+SO2属于置换反应
Hg+SO2属于置换反应
C. 含汞烟气必须处理达标后才能排放
D. 流程中加入氧化钙的目的是减少SO2的排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种元素的部分信息如下表所示。
元素 | X | Y | Z | W |
相关 信息 | 短周期元素,最高化合价为+7价 | 基态原子中,电子占据的最高能层符号为L,最高能级上只有两个自旋方向相同的电子 | 核外电子共有15种运动状态 | 能与X形成两种常见化合物WX2、WX3,酚遇WX3溶液能发生显色反应 |
回答下列问题:
(1)W的基态原子电子排布式为___,X、Y、Z三种元素电负性由大到小的顺序为___(用具体的元素符号填写)。
(2)化合物YX4、ZX3、ZX5(气态或液态时)中,中心原子的轨道类型不是sp3杂化的是___ (填化学式,下同),分子构型是正四面体的是___,ZX3属于___(极性分子、非极性分子)。
(3)已知WX3的熔点:306℃,沸点:319℃,则WX3的晶体类型为___。
(4)Z原子的价电子轨道表示式为___。
(5)W元素的单质晶体在不同温度下有两种堆积方式,晶胞分别如图所示。在面心立方晶胞中W原子的配位数为___;若W的原子半径为rcm,阿伏加德罗常数为NA,则其体心立方晶体的密度可表示为___gcm-3。
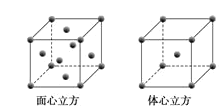
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】柠檬烯![]()
![]()
![]() 具有良好的镇咳、祛痰、抑菌作用。下列关于柠檬烯的说法正确的是( )
具有良好的镇咳、祛痰、抑菌作用。下列关于柠檬烯的说法正确的是( )
A.能使酸性高锰酸钾溶液褪色,其褪色原理与![]() 相同
相同
B.能发生氧化反应、加成反应、取代反应、缩聚反应
C.与乙烯互为同系物,其一氯代物有8种
D.分子中所有碳原子可能处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2NO(g)+Br2(g)![]() 2NOBr(g) △H=-a kJ·mol-1 (a>0),其反应机理如下
2NOBr(g) △H=-a kJ·mol-1 (a>0),其反应机理如下
①NO(g)+Br2(g)![]() NOBr2(g) 快 ②NO(g)+NOBr2(g)
NOBr2(g) 快 ②NO(g)+NOBr2(g)![]() 2NOBr(g) 慢
2NOBr(g) 慢
下列有关该反应的说法正确的是( )
A. 该反应的速率主要取决于①的快慢
B. NOBr2是该反应的催化剂
C. 正反应的活化能比逆反应的活化能小a kJ·mol-1
D. 增大Br2(g)浓度能增大活化分子百分数, 加快反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取部分物质的过程如下图所示,下列有关说法错误的是
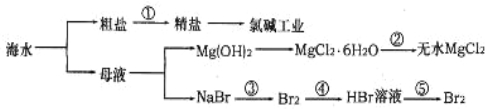
A.过程①需要加入化学试剂、沉淀、过滤等操作
B.由“母液→无水MgCl2”一系列变化中未涉及氧化还原反应
C.工业上一般用电解氯化镁溶液制取Mg单质
D.反应③和⑤均可由下列反应实现:2Br-+Cl2=Br2+2Cl-,该反应属于置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。下图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法正确的是( )
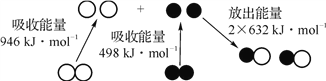
A. 放电条件下,N2(g)和O2(g)混合能直接化合生成NO(g)
B. NO是一种酸性氧化物,能用NaOH溶液处理含NO的尾气
C. N2(g)和O2(g)反应生成 NO(g),相当于N2(g)在O2(g)燃烧,该反应放热
D. 28 g N2(g)和32 g O2(g)完全反应生成 NO(g),放出的能量为180 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com