
【题目】四种短周期元素A、B、C、D,原子序数依次增大,A原子的最外电子层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上电子数之和。
(1)A元素最高价氧化物的电子式为_________,D元素的某种核素中质子数和中子数相等,该核素组成符号为_______。
(2)化合物E中存在的化学键类型为_________。
(3)A、B、C的原子半径从大到小的顺序__________________。(用对应原子符号表示);B、C、D 的简单离子的半径从大到小的顺序__________________。(用对应的离子符号表示)
【答案】 ![]()
![]() 离子键和(非极性)共价键 Na>C>O S2->O2->Na+
离子键和(非极性)共价键 Na>C>O S2->O2->Na+
【解析】四种短周期元素A、B、C、D的原子序数依次增大,B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,则B为O元素、C为Na元素,E为Na2O2,A原子的最外电子层上有4个电子且原子序数小于O元素,则A为C元素,D的L层电子数等于K、M两个电子层上电子数之和,D为S元素。
(1). C元素的最高价氧化物是CO2,电子式为![]() ,S是16号元素,质子数为16,质子数和中子数相等,则中子数也为16,质量数为32,该核素组成符号为
,S是16号元素,质子数为16,质子数和中子数相等,则中子数也为16,质量数为32,该核素组成符号为![]() ,故答案为:
,故答案为:![]() ;
;![]() ;
;
(2).化合物E是Na2O2,该物质中存在离子键和(非极性)共价键,故答案为:离子键和(非极性)共价键;
(3).根据元素周期律,同一周期随原子序数的增大原子半径逐渐减小,同一主族随原子序数的增大原子半径逐渐增大,则C、O、Na的原子半径从大到小的顺序为Na>C>O,O2-和Na+具有相同的电子层结构,原子序数越大,离子半径越小,则离子半径O2->Na+,S元素和O元素位于同一主族,S2-比O2-多一个电子层,离子半径S2->O2-,所以离子半径S2->O2->Na+,故答案为:Na>C>O;S2->O2->Na+。


科目:高中化学 来源: 题型:
【题目】原子结构模型的演变图如图: 
其中,(1)为道尔顿实心球式原子模型;(2)为卢瑟福行星运转式原子模型;(3)为汤姆生葡萄干面包式原子模型;(4)为近代量子力学原子模型;(5)为玻尔轨道式原子模型.下列符合历史演变顺序的一组排列是( )
A.(1)(3)(2)(5)(4)
B.(1)(2)(3)(4)(5)
C.(1)(5)(3)(2)(4)
D.(1)(3)(5)(4)(2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某密闭容器中发生如下反应:X(g)+3Y(g)2Z(g);△H<0.如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是( ) 
A.t5时增大了压强
B.t3时降低了温度
C.t2时加入了催化剂
D.t4~t5时间内转化率一定最低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为短周期元素,其原子半径、化合价等信息见下表。
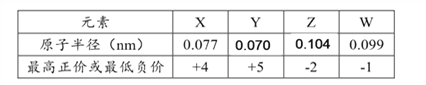
有关这四种元素的说法一定正确的是( )
A. X与W形成的化合物是离子化合物
B. Y的氢化物能与W的氢化物反应,所得产物只含有共价键
C. X、Y能分别与氧元素形成多种氧化物
D. Z处于元素周期表中第三周期ⅣA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组拟探究碳、硅元素的非金属性的相对强弱,实验装置如下:
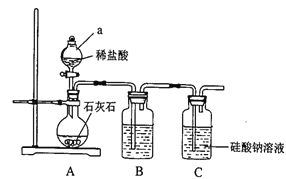
(1)连接好装置后,实验前必须进行的一步操作是_________。仪器a的名称为______。
(2)B装置中盛放的试剂是_________,C中发生反应的化学方程式为_________。
(3)该兴趣小组设计此实验通过_________(填实验现象),可判断碳的非金属性强于硅的非金属性。
(4)该小组的一位同学认为,利用此实验装置及药品,也可以证明非金属性Cl>C>Si,你是否同意该同学的观点?_________(填“同意”或“不同意”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关比色法测样品纯度的说法正确的是( )
A.比色法的优点是灵敏度高,缺点是误差较大
B.无色金属离子都不能用比色法测定
C.酸性溶液中的H+的显色剂可用酚酞代替石蕊
D.配制抗贫血(含Fe2+)药片样品溶液,加入硝酸的目的是防止Fe2+水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质的分类、名称(或俗名)、化学式都正确的是( )
分类 | 名称(俗名) | 化学式 | |
A | 碱性氧化物 | 氧化铁 | FeO |
B | 酸性氧化物 | 碳酸气 | CO |
C | 酸 | 硫酸 | H2SO3 |
D | 盐 | 纯碱 | Na2CO3 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组进行了如图所示的实验,设第一步HNO3的还原产物只有NO.相关分析不正确的是( ) 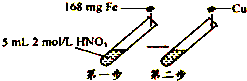
A.第一步反应后溶液中c(NO ![]() )=1.5mol/L(忽略体积变化)
)=1.5mol/L(忽略体积变化)
B.第一步反应后溶液中c(Fe2+):c(Fe3+)=1:1
C.第一步可生成标准状况下的气体44.8 mL
D.第二步可溶解铜48mg
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com