
����Ŀ��ijͬѧ�������ʵ�鷽�����Է���KCl��BaCl2���ֹ�������Իش��������⣺

��ѡ�Լ���Na2SO4��Һ��K2CO3��Һ��K2SO4��Һ������
��1�������ڵ�������______________���Լ�a��������_______________���ѧʽ��
��2�������Լ�b��������Ӧ�Ļ�ѧ����ʽΪ___________________________________��
��3���÷����ܲ��ܴﵽʵ��Ŀ�ģ�_____________�������ܣ�Ӧ��θĽ��������ܣ����ʲ��ûش�________________________________________��
��4���÷�����Ĺ���B����100mL 0.5mol/L����ҺB���������¿ɹ�ѡ���������
A.��ͷ�ι� B.��ƿ C.�ձ� D.ҩ�� E.��Ͳ F.������ƽ��
����������ƽ�Ƶù���B��������_________g��
��������ҺBʱ������������һ������Ҫʹ�õ���_____________������ĸ������ȱ�ٵ�������__________________________________��д�������ƣ���
���𰸡�����K2CO3BaCO3+2HCl=BaCl2+CO2��+H2O����Ӧ�ڲ����ڵ���Һ�м������������������ᾧ10.4B100mL����ƿ��������
��������
����KCl��BaCl2���ֹ��������������ˮ��Ȼ��������K2CO3ʹBaCl2ת��Ϊ���������˺�����������������BaCl2��Һ�����������ᾧ�������ɵù���BaCl2��������������ҺΪKCl��K2CO3�Ļ��������ᾧ�õ�����CΪKCl��K2CO3��Ӧ�����������ɵ�KCl������AΪBaCO3��ϴ�Ӻ����ᣬ�����õ�����BΪBaCl2��
��1�������������Һ��Ӧ��ˮ�ܽ⣬������Ϊ�����Һ��ķ��룬Ϊ���˲������������Ϸ�����֪����Һ�м��������K2CO3��ҺʹBaCl2ת��Ϊ�������Լ�a��������K2CO3���������������������������K2CO3��
��2������AΪBaCO3�������������ᣬ��Ӧ�����Ȼ����Ͷ�����̼��������Ӧ�Ļ�ѧ����ʽΪ��BaCO3+2HCl=BaCl2+CO2��+H2O���������������������BaCO3+2HCl=BaCl2+CO2��+H2O��
��3���÷������ܴﵽʵ��Ŀ�ģ���Ϊ�����ڽ�����ɺ�������ҺΪKCl��K2CO3�Ļ������Ӧ�ü�����������ᣬ��K2CO3��Ϊ�Ȼ�����Ȼ���ٽ��������ᾧ���õ��Ȼ��ع��壻����������������ǣ����ܣ�Ӧ�ڲ����ڵ���Һ�м������������������ᾧ��
��4��������BΪ�Ȼ�������������0.1L��0.5mol/L��208g/mol=10.4g���������������������10.4��
�����������Ȼ�����Һʱ���������ܽ⡢���ݵȣ�����Ҫ��ƿ����ȱ�ٵ�������100mL����ƿ��������������������������ǣ�B�� 100mL����ƿ����������


 ��ʦ����ָ���ο�ʱϵ�д�
��ʦ����ָ���ο�ʱϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʵ����Ǹ��л�ѧ���õ�������������������йؼ��㡣
��1����0.4 mol Al3����Al2(SO4)3��������SO42�������ʵ�����___________��
��2��___________molH2O2����ԭ������0.2molH3PO4����ԭ������ȡ�
��3��ij��������Һ�к���3.01��1022��Na+������Һ��SO42�������ʵ�����___________��
��4��0.7 mol H2O������Ϊ___________��
��5��483gNa2SO4��10H2O��������Na+�����ʵ�����___mol������H2O���ӵ���Ŀ��___����
��6��������ͬ��H2��NH3��SO2��O3���������У����з�����Ŀ���ٵ���____________��
��7��a��Xԭ�ӵ�������Ϊbg����X�����ԭ���������Ա�ʾΪ___________
��8������mgij���壬������ԭ�ӷ��ӣ���Ħ������ΪMg��mol-1���������ӵ�������NA��ʾ���������Ϸ��ż���Ӧ������д���пո�
�ٸ���������ʵ���Ϊ___________mol��
�ڸ���������ԭ������Ϊ___________����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾ��ʵ�����������ʵ����Ӧʵ��Ŀ�ĵ����� ��
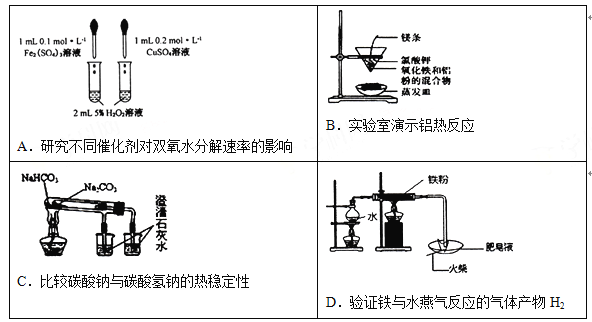
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ����ˮ�ܽ⡢���ˡ������Ȳ������ɽ����и������������ǣ� ��
A.����ء���������B.����ͭ����������
C.�Ȼ��ء���������D.����ͭ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����ͬ������![]() �����
�����![]() ���壬�������֮��Ϊ ______ ����ԭ����֮��Ϊ ______ ����ͬ������
���壬�������֮��Ϊ ______ ����ԭ����֮��Ϊ ______ ����ͬ������![]() ͬ��ͬѹ
ͬ��ͬѹ![]() �����֮��Ϊ ______ ���ܶ�֮��Ϊ ______ ��
�����֮��Ϊ ______ ���ܶ�֮��Ϊ ______ ��
��2��![]() ��
��![]() �Ļ�������У���Ԫ�ص���������Ϊ
�Ļ�������У���Ԫ�ص���������Ϊ![]() ����
����![]() ��
��![]() �����ʵ���֮���� ______ �����ֻ��������ܶ���ͬ��ͬѹ�������ܶȵ� ______ ��
�����ʵ���֮���� ______ �����ֻ��������ܶ���ͬ��ͬѹ�������ܶȵ� ______ ��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼװ�ý���ʵ�飬��ʼʱ��a��b����Һ����ƽ���ܷ�ã�����һ��ʱ�䡣����˵������ȷ����( )

A. a�ܷ���������ʴ��b�ܷ������ⸯʴ
B. һ��ʱ���a��Һ�����b��Һ��
C. a����Һ��pH����b����Һ��pH��С
D. a��b����������ͬ�ĵ缫��Ӧʽ��Fe��2e��===Fe2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���ʵ�ʴ�����������ȷ���� �� ��
A. 3������2����ϩ B. 2������5���һ���1������
C. 2��2���������� D. 3��3��������2����ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����ù���NaOH����0.5 mol�� L-1��NaOH��Һ500 mL,��������������Ʒ:���ձ�����100 mL��Ͳ����500 mL����ƿ����ҩ�ס��ݲ���������������ƽ(������)
(1)����ʱ,û��ʹ�õ���������Ʒ��___(�����),��ȱ�ٵ�������______��
(2)�����Ƶ�ת�ƹ�����ijѧ��������ͼ����,��ָ�����еĴ���:______________��

(3)������ƿʹ�÷�����,���в�������ȷ����____(�����)��
A.ʹ������ƿǰ������Ƿ�©ˮ
B.����ƿ������ˮϴ����,���ü�Һ��ϴ
C.���������ƹ��������ƽ���̵���ֽ��,ȷ�����������ձ����ܽ��,����ע������ƿ��
D.���ݺ�����ƿ��,��ʳָ��סƿ��,����һֻ�ֵ���ָ��סƿ��,������ƿ��תҡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������,��1L0.1mol��L-1һԪ��HR��Һ����ͨ�백��[��֪������Kb(NH3��H2O)=1.76��10-5]��ʹ��Һ�¶Ⱥ�������ֲ��䣬�����Һ��pH������Ũ�ȱ仯�Ĺ�ϵ����ͼ��ʾ������������ȷ���ǣ� ��
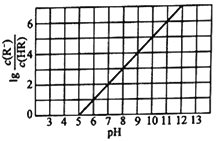
A. 0.1mol��L-1HR��Һ��pHԼΪ5 B. HRΪ���ᣬ����ʱKa(HR)=1.0��10-7
C. ��ͨ��0.1molNH3ʱ,��Һ��c(R-)<c(NH4+) D. ��c(HR)=c(R-)ʱ,��Һ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com