
汽车已经成为重要的交通工具,但其排放的尾气是空气的主要污染物之一。已知汽车尾气中的主要污染物有:CmHn(烃)、SO2、NOx、CO和C等,请回答下列有关问题。
(1)若用CmHn表示汽油的主要组成,CmHn在空气中完全燃烧的化学方程式为________________________________________________________________________,
汽油燃烧产生能量为汽车提供了动力,这一过程中能量的转化是由________能转化为________能,最终转化为机械能;
(2)通过车用燃油的精炼加工处理,可减少汽车尾气中________(填化学式)的排放;
(3)目前汽车尾气多采用催化转化的方法加以治理,写出在催化剂作用下NOx与CO反应的化学方程式__________________________________________________ ______________________
______________________
________________________________________________________________________。
科目:高中化学 来源: 题型:
某化学兴趣小组利用图一装置制取氨气并探究氨气的有关性质。

(1)装置A中烧瓶内试剂可选用________(填序号)。
a.碱石灰 b.浓硫酸 c.生石灰 d.五氧化二磷 e.烧碱
(2)若探究氨气的溶解性,需在K2的导管末端连接图二装置中的________装置(填序号),当装置D中集满氨气后,关闭K1、K2,打开K3,引发喷泉的实验操作是____________________________________________。
(3)若探究氨气的还原性,需打开K1、K3,K2处导管连接制取纯净、干燥氯气的装置。
①用二氧化锰与浓盐酸制取氯气,生成气体必须通过盛有____________________试剂的洗气瓶;
②D中氨气与氯气反应产生白烟,同时生成一种无色无味的气体,该反应的化学方程式为_____________________________________________________________;
③从K3处导管逸出的气体中含有少量Cl2,则C装置中应盛放________溶液(填化学式),反应的离子方程式为_____________________________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
某校化学研究性学习小组学习了化学反应与能量的内容后,对
CaCO3与稀盐酸的反应进行了相关探究。他们在室温条件下,将CaCO3
块状固体放入1L、1mol•L-1稀盐酸中,记录下了随反应时间的变化生成
CO2气体的物质的量情况,绘制成如图曲线。假设溶液的体积变化忽略
不计,请分析以下问题:
(1)若想加快该反应的速率,可以采取的措施是 、
(答两种)。
(2)0~2min内,用HCl浓度变化表示的平均反应速率为 ,比较0~2min、2~4min、4~6min三个时间段,反应速率最大的是 。
(3)根据定量的数据,定性的描述0~6min内该反应的化学反应速率的变化情况
呈现这种变化的原因是 。
(4)根据图像中曲线的变化趋势,第8min时,该反应的反应速率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:
X2(g)+3Y2(g) 2XY3(g) △H=-92.6kJ·mol-1
2XY3(g) △H=-92.6kJ·mol-1
起始时各物质物质的量如下表所示:
| 容器 编号 | 起始时各物质物质的量/mol | ||
| X2 | Y2 | XY3 | |
| ① | 1 | 3 | 0 |
| ② | 0.6 | 1.8 | 0.8 |
达到平衡后,①容器中XY3的物质的量为0.5mol。下列叙述正确的是
A.容器①、②中反应的平衡常数不相等
B.达平衡时,容器②中 XY3的物质的量浓度为2mol·L—1
C.容器①中反应达到平衡时放出的热量为23.15 kJ
D.容器②中反应达到平衡时放出热量
查看答案和解析>>
科目:高中化学 来源: 题型:
海水是一个巨大的化学资源宝库,下列有关海水综合利用的说法正确的是
A.海水中含有钾元素,只需经过物理变化就可以得到钾单质
B.海水蒸发制海盐的过程中只发生了化学变化
C.从海水中可以得到NaCl,电解熔融NaCl可制备Cl2
D.利用潮汐发电是将化学能转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学与生产、生活的认识不正确的是
A.合理开发利用可燃冰(固态甲 烷水合物)有助于缓解能源紧缺的状况
烷水合物)有助于缓解能源紧缺的状况
B.为防止电池中的重金属等污染土壤或水体,应积极开发废电池的综合利用技术
C.为防止纸张被酸腐蚀,可在纸浆中加入碳酸钙等添加剂
D.海水提镁的主要步骤为:海水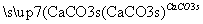 Mg(OH)2(s)
Mg(OH)2(s)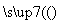 MgCl2(aq)
MgCl2(aq)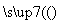 Mg(l)+Cl2(g)
Mg(l)+Cl2(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
不仅化工生产应遵循绿色化学的原则,化学实验也应遵循绿色化学的原则,实现原料和过程的绿色化。下列实验或实验过程遵循绿色化学原则的是
①在萃取操作的演示实验中,将CCl4萃取溴水改为CCl4萃取碘水 ②在铜与浓硝酸反应的实验中,将铜片改为可调节高度的铜丝 ③将实验室的废酸液和废碱液中和后再排放 ④用双氧水代替高锰酸钾制氧气 ⑤将用铜粉与浓硫酸反应制取硫酸铜的实验方案改为先将铜粉在空气中充分加热制得氧化铜,再将氧化铜溶解在稀硫酸中
A.①② B.②③
C.③④ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
对于锌-铜-稀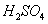 组成的原电池装置中,当导线中有
组成的原电池装置中,当导线中有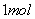 电子通过时,理论上的电极变化
电子通过时,理论上的电极变化
①锌片溶解了32.5g②锌片增重32.5g③铜片上析出了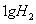 ④铜片上析出
④铜片上析出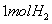
A、①③
B、①④
C、②③
D、②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com