

| ||
| ||


科目:高中化学 来源: 题型:
| 选项 | 化学工业 | 主要设备 | 措施 | 目的 |
| A | 合成氨 | 合成塔 | 500℃左右 | 防止催化剂中毒 |
| B | 电解食盐水 | 电解槽 | 石棉隔膜 | 防止氯气和氢氧化钠反应 |
| C | 接触法制硫酸 | 接触室 | 五氧化二钒 | 提高二氧化硫的转化率 |
| D | 侯式制碱 | 沉淀池 | 先通氨气,再通二氧化碳 | 有利于二氧化碳的吸收 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
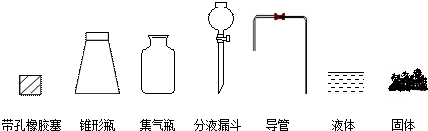
查看答案和解析>>
科目:高中化学 来源: 题型:
| 80℃,通电 |
| Ⅰ |
| 室温,KCl |
| Ⅱ |
| Cl2 |
| 460℃ |
| 蒸馏 |
| H2 |
| 1100℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 将氢氧化钠、氯化钡和硫酸铝三种固体组成的混合物溶于足量的水中,充分溶解,用1mol?L-1稀硫酸滴定,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断正确的是( )
将氢氧化钠、氯化钡和硫酸铝三种固体组成的混合物溶于足量的水中,充分溶解,用1mol?L-1稀硫酸滴定,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断正确的是( )| A、A点所表示的沉淀是:Al(OH)3、BaSO4 |
| B、B-C段所发生反应的离子方程式是:H++OH-→H2O |
| C、A-B段发生反应的离子方程式:Ba2++SO42-→BaSO4↓ |
| D、拐点E的横坐标为70mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
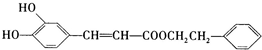 是一种天然抗癌药物,在一定条件下能发生如下转化:
是一种天然抗癌药物,在一定条件下能发生如下转化: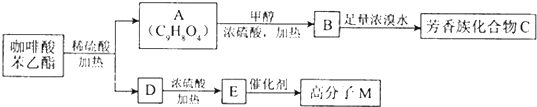
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子半径:X2->Y+ |
| B、原子的最外层电子数:X>Y>Z>W |
| C、单质沸点:X>Y>Z>W |
| D、X与Y形成的化合物中只2含有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
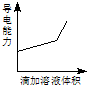 浓度均为0.1mol/L的下列各组溶液,将溶液(Ⅱ)滴加到溶液(Ⅰ)中,测得溶液(I)的导电能力变化符合如图变化趋势的是( )
浓度均为0.1mol/L的下列各组溶液,将溶液(Ⅱ)滴加到溶液(Ⅰ)中,测得溶液(I)的导电能力变化符合如图变化趋势的是( )| A | B | C | D | |
| 溶液(Ⅰ) | 盐酸 | 醋酸 | 氢氧化钠 | 氨水 |
| 溶液(Ⅱ) | 氢氧化钠 | 氢氧化钠 | 氨水 | 硝酸银 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com