
【题目】砷及其化合物有着广泛的用途。砷有两种常见的弱酸,砷酸(H3AsO4)和亚砷酸(H3AsO3)。已知砷酸(H3AsO4)的pKa1、pKa2、pKa3依次为2.25、6.77、11.40(pKa=-lgKa)。回答下列问题:
(1)已知:As(s)+![]() H2(g)+2O2(g)=H3AsO4(s)ΔHl
H2(g)+2O2(g)=H3AsO4(s)ΔHl
H2(g)+![]() O2(g)=H2O(1)ΔH2
O2(g)=H2O(1)ΔH2
As(s)+ ![]() O2(g)=
O2(g)= ![]() As2O5(s) ΔH3
As2O5(s) ΔH3
则反应As2O5(g)+3H2O(1)=2H3AsO4(s) ΔH=_________。
(2)写出砷酸(H3AsO4)的第二步电离方程式___________________________________。
(3)NaH2AsO4溶液呈______(填“酸性”、“中性”或“碱性”),试通过计算说明________________________。
(4)亚砷酸(H3AsO3)水溶液中存在多种微粒形态,各种微粒分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与溶液的pH关系如下图所示。
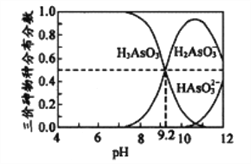
以酚酞为指示剂(变色范围pH8.2~10.0),将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加。该过程中主要反应的离子方程式为__________________________。
(5)某化学兴趣小组同学欲探究可逆反应AsO33-+I2+2OH-![]() AsO43-+2I-+H2O。设计如下图I所示装置。实验操作及现象:按图I装置加入试剂并连接装置,电流由C2流入C1。当电流变为零时,向图I装置左边烧杯中逐滴加入一定量2mol/L盐酸,发现又产生电流,实验中电流与时间的关系如图II所示。
AsO43-+2I-+H2O。设计如下图I所示装置。实验操作及现象:按图I装置加入试剂并连接装置,电流由C2流入C1。当电流变为零时,向图I装置左边烧杯中逐滴加入一定量2mol/L盐酸,发现又产生电流,实验中电流与时间的关系如图II所示。
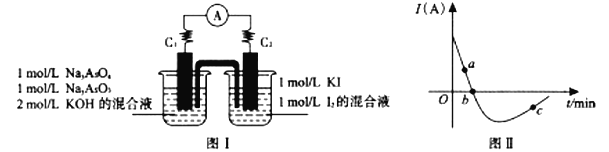
①图II中AsO43-的逆反应速率:a____b(填“>”、”<”或“=”)。
②写出图II中c点对应图I装置的正极反应式__________________________。
③能判断该反应达到平衡状态的是________________。
a.2v(I-)正=v(AsO33-)逆 b.溶液的pH不再变化
c.电流表示数变为零 d.溶液颜色不再变化
【答案】 2ΔH1-3ΔH2-2ΔH3 H2AsO4-![]() H++HAsO42- 酸性 Ka3=
H++HAsO42- 酸性 Ka3=![]() =
=![]() =10-11.75<10-6.77即Ka2>Ka3,溶液呈酸 H3ASO3+OH-=H2AsO3-+H2O < AsO43-+2e-+2H+=AsO32-+H2O bcd
=10-11.75<10-6.77即Ka2>Ka3,溶液呈酸 H3ASO3+OH-=H2AsO3-+H2O < AsO43-+2e-+2H+=AsO32-+H2O bcd
【解析】(1)已知:①As(s)+![]() H2(g)+2O2(g)=H3AsO4(s)ΔHl
H2(g)+2O2(g)=H3AsO4(s)ΔHl
②H2(g)+![]() O2(g)=H2O(1)ΔH2
O2(g)=H2O(1)ΔH2
③As(s)+ ![]() O2(g)=
O2(g)= ![]() As2O5(s) ΔH3
As2O5(s) ΔH3
根据盖斯定律,由①×2-②×3-③×2得反应As2O5(g)+3H2O(1)=2H3AsO4(s) ΔH=2ΔH1-3ΔH2-2ΔH3;(2)砷酸(H3AsO4)为多元弱酸,分步电离,第二步电离方程式为H2AsO4-![]() H++HAsO42-;(3)NaH2AsO4溶液呈酸性,Ka3=
H++HAsO42-;(3)NaH2AsO4溶液呈酸性,Ka3=![]() =
=![]() =10-11.75<10-6.77即Ka2>Ka3,溶液呈酸;(4) 根据图中曲线变化,以酚酞为指示剂(变色范围pH8.2~10.0),将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加,该过程主要为H3ASO3转化为H2AsO3-,则主要反应的离子方程式为H3ASO3+OH-=H2AsO3-+H2O;(5)①随着反应的进行,离子浓度减小,电流减小,正反应速率减小,逆反应速率增大,故图II中AsO43-的逆反应速率:a<b;②图II中c点酸性条件下对应图I装置的正极AsO43-得电子产生AsO33-,电极反应式为AsO43-+2e-+2H+=AsO32-+H2O;③a.根据速率关系, v(I-)正=2v(AsO33-)逆,则等式始终成立,反应不一定处于平衡状态; b.溶液的pH不再变化,则氢氧根离子浓度也保持不变,反应处于平衡状态;c.电流表示数变为零则氧化还原反应中电子转移不再增减,反应物的浓度保持不变,反应处于平衡状态;d.溶液颜色不再变化,则碘单质的浓度保持不变,反应处于平衡状态;答案选bcd。
=10-11.75<10-6.77即Ka2>Ka3,溶液呈酸;(4) 根据图中曲线变化,以酚酞为指示剂(变色范围pH8.2~10.0),将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加,该过程主要为H3ASO3转化为H2AsO3-,则主要反应的离子方程式为H3ASO3+OH-=H2AsO3-+H2O;(5)①随着反应的进行,离子浓度减小,电流减小,正反应速率减小,逆反应速率增大,故图II中AsO43-的逆反应速率:a<b;②图II中c点酸性条件下对应图I装置的正极AsO43-得电子产生AsO33-,电极反应式为AsO43-+2e-+2H+=AsO32-+H2O;③a.根据速率关系, v(I-)正=2v(AsO33-)逆,则等式始终成立,反应不一定处于平衡状态; b.溶液的pH不再变化,则氢氧根离子浓度也保持不变,反应处于平衡状态;c.电流表示数变为零则氧化还原反应中电子转移不再增减,反应物的浓度保持不变,反应处于平衡状态;d.溶液颜色不再变化,则碘单质的浓度保持不变,反应处于平衡状态;答案选bcd。


 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
【题目】常温下,将 20.0 g 质量分数为 14.0%的 KNO3溶液与 30.0 g 质量分数为 24.0%的 KNO3溶液混合,得到的密度为1.15 g/cm3的混合溶液。计算:
(1)混合后溶液的质量分数_________。
(2)混合后溶液的物质的量浓度_______。
(3)在1000g水中需溶解______molKNO3才能使其浓度恰好与上述混合后溶液的浓度相等?
(4)标况下44.8LHCl溶于水配成500mL溶液。计算:
①HCl的物质的量____________________;
②所得溶液中溶质的物质的量浓度____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于硅酸钠以下说法不正确的是( )
A. 硅酸钠与盐酸反应的离子方程式:SiO32—+2H+=H2SiO3↓
B. 硅酸钠溶液俗称“泡花碱”,其溶液显碱性,滴加酚酞显红色
C. Na2CO3+SiO2 ![]() Na2SiO3+CO2↑,说明硅酸酸性比碳酸强
Na2SiO3+CO2↑,说明硅酸酸性比碳酸强
D. 水玻璃久置在空气中变质,因为与空气中的CO2发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在实验室进行铁盐与亚铁盐相互转化实验。
实验I:將Fe3+转化为Fe2+

(1)Fe3+与Cu粉发生反应的离子方程式为___________________________。
(2)探究白色沉淀产生的原因,请填写实验方案:
实验方案 | 现象 | 结论 |
步骤1:取4mL____mol/LCuSO4溶液,向其中滴加3滴0.1mol/LKSCN溶液 | 产生白色沉淀 | CuSO4溶液与KSCN溶液 反应产生了白色沉淀 |
取______________ | 无明显现象 |
查阅资料:
已知:①SCN-的化学性质与I-相似 ②2Cu2++4I-=2CuI↓+I2
Cu2+与SCN-反应的离子方程式为_________________________________。
实验II:将Fe2+转化为Fe3+
实验方案 | 现象 |
向3mL0.lmol/LFeSO4溶液中加入1mL 稀硝酸 | 溶液变为棕色,放置一段时间后, 棕色消失,溶液变为黄色 |
探究上述现象出现的原因:
查阅资料:Fe2++NO![]() Fe(NO)2+(棕色)
Fe(NO)2+(棕色)
(3)用离子方程式解释NO产生的原因_____________________________________。
(4)从化学反应速率与限度的角度对体系中存在的反应进行分析:
反应I:Fe2++与HNO3反应; 反应II:Fe2+与NO反应
①依据实验现象,可推知反应I的速率比反应II_____(填“快”或“慢”)。
②反应I是一个不可逆反应,设计实验方案加以证明_________________________。
③请用化学平衡移动原理解释溶液由棕色变为黄色的原因_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向一定体积0.1mol·L-1的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH(pOH=-lg[OH-])与pH的变化关系如图所示则

A. M点所示溶液的导电能力强于Q点
B. N点所示溶液中c(CH3COO-)>c(Na+)
C. M点和N点所示溶液中水的电离程度相同
D. Q点消耗NaOH溶液的体积等于醋酸溶液的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示。下列说法错误是

A. Q位于第三周期IA族
B. X、Y、Z三种元素组成的化合物可能是盐或碱
C. 简单离子半径:M->Q+>R2+
D. Z与M的最高价氧化物对应水化物均为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学-选修3:物质结构与性质]
文艺复兴时期,群青颜料曾用在许多著名的油画上,当时群青颜料是由贵重的青金石研磨并制成的。青金石是指碱性铝硅酸盐矿物,其中含钠、铝、硅、硫、氯、氧等元素。
(1)硅元素基态原子的价电子轨道表示式为____________。
(2)第四周期中,与铝未成对电子数相同的金属元素有________种。
(3)Na+和Ne互为等电子体,电离能I2(Na)________I1(Ne)(填“>”或“<”)。
(4)①已知氯有多种含氧酸,其电离平衡常数如下:
化学式 | HClO4 | HClO3 | HClO2 | HClO |
Ka | 1×1010 | 1×101 | 1×10-2 | 4×10-8 |
HClO4的结构简式为_________,HClO3中Cl原子的杂化轨道类型为________,HClO2中含有的共价键类型为__________。以上几种含氧酸的酸性强弱不同,其原因为______________。
②氢卤酸(HX)的电离过程如图。ΔH1和ΔH2的递变规律都是HF>HCl>HBr>HI,其中ΔH1(HF)特别大的原因为_________,影响ΔH2递变的因素为______________。

(5)铝单质为面心立方晶体,晶胞参数a=q nm,铝的摩尔质量为Mg·mol-1,原子半径为r pm,阿伏伽德罗常数的值为NA。则铝单质的密度为________g·cm-3(列式即可,下同),铝晶胞中原子的体积占晶胞体积的百分率为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列不属于配合物的是( )
A. [Cu(H2O)4]SO4·H2O B. [Ag(NH3)2]OH
C. KAl(SO4)2·12H2O D. Na[Al(OH)4]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)①写出重晶石的化学式:____________;
②写出甘油的结构简式:____________。
(2)写出FeCl3与KI反应的离子方程式:____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com