
孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备 CuSO4·5H2O及纳米材料G,步骤如下:
请回答下列问题:
(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:实验步骤中试剂①最佳为_____(填代号)。
a.KMnO4 b.(NH4)2S c.H2O2 d.KSCN
向溶液B中加入CuO的作用是 。
(2)由溶液C获得CuSO4·5H2O,需要经过 、过滤等操作。除烧杯、漏斗外,过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是 。
(3)写出制备G的化学反应方程式。若实验过程中有氨气逸出,应选用下列 装置回收(填代号)。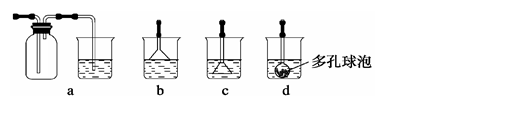
(4)欲测定溶液A中Fe2+的溶液,可用KMnO4标准溶液滴定,取用KMnO4标准溶液应使用 。取A溶液稀释一定倍数后,用KMnO4标准溶液滴定,终点现象为 。
(1)cd (2分 ) 调节溶液的pH值,促进Fe3+水解 (2分)
(2)加热蒸发、冷却结晶(2分 ) 引流 (2分)
(3)2NH3+CO2+CaCl2+H2O=CaCO3↓+2NH4Cl (2分 ) b (2分)
(4)酸式滴定管 (2分 ) 溶液变成紫红色并保持半分钟不褪色 (2分)
解析试题分析:(1)本实验要除去Fe2+、Fe3+等离子,先加入合适的氧化剂时不能引入新的杂质,可加入H2O2,发生的反应为:2H2O2+2Fe2++2H+═2Fe3++4H2O,因Fe3+遇KSCN溶液变为血红色,则可用KSCN检验Fe3+;故答案为:c;d;向溶液B中加入CuO的作用是调节溶液的pH值,促进Fe3+水解。(2)从溶液中要析出晶体,采用冷却结晶法,然后进行过滤等操作,过滤用到的仪器有烧杯、玻璃棒、漏斗、滤纸等仪器,其中玻璃棒在过滤时起到引流的作用,在蒸发时起到搅拌的作用,故答案为:冷却结晶;玻璃棒;搅拌、引流;(3)CaCl2溶液不能与CO2反应,加入碱能反应,但又不能引入杂质,应通入NH3,实验室收集氨气时要注意防止倒吸,因为氨气极易溶于水,吸收时导管不能插入到液面以下,可用倒置的漏斗,故答案为:2NH3+CO2+CaCl2+H2O=CaCO3↓+2NH4Cl ;b;(4)高锰酸钾具有强氧化性,则只能用酸式滴定管盛装高锰酸钾溶液,终点现象为溶液变成紫红色并保持半分钟不褪色 。
考点:本题考查了常见金属的单质及其化合物的应用,考查物质的制取和提纯等实验操作,注意蒸发、过滤、滴定操作的注意事项。


科目:高中化学 来源: 题型:填空题
铁和铁的化合物用途广泛。请回答下列问题:
(1)写出在潮湿空气中钢铁锈蚀时正极反应的电极反应式:_______________________。
将生锈的铁屑放入H2SO4溶液中充分溶解后,在溶液中并未检测出Fe3+,用离子方程式说明原因:______________________________________。
(2)爱迪生蓄电池的反应式为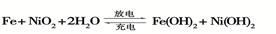
①爱迪生蓄电池的正极是 ,该电池工作一段时间后必须充电,充电时生成Fe的反应类型是______。
②高铁酸钠(Na2FeO4)是一种新型净水剂。用如图装置可以制取少量高铁酸钠。写出在用电解法制取高铁酸钠时,阳极的电极反应式___________________________________。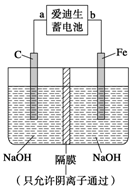
③你认为高铁酸钠作为一种新型净水剂的理由错误的是______。
a.高铁酸钠溶于水形成一种胶体,具有较强的吸附性
b.高铁酸钠在消毒杀菌时被还原生成Fe3+,Fe3+水解产生氢氧化铁胶体能吸附悬浮杂质
c.高铁酸钠具有强氧化性,能消毒杀菌
d.高铁酸钠具有强还原性,能消毒杀菌
(3)某FeO、Fe2O3混合物中,铁、氧的物质的量之比为4︰5,其中Fe2+与Fe3+物质的量之比为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
将0.1mol的镁铝混合物溶于100ml 2mol/L的H2SO4中,然后滴加1mol/L的NaOH溶液,请回答:
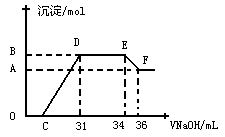
(1)若在滴加NaOH溶液的过程中,生成沉淀的质量m与加入NaOH溶液的体积关系如图所示。请回答:当V1=160mL时,则金属粉末中n(Mg)=_____mol,V2=______mL。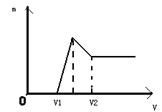
(2)若在滴加NaOH溶液的过程中欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液体积为________ml
(3)若混合物仍为0.1mol其中镁粉的物质的量的分数为a,用100ml2mol/L的硫酸溶解此混合物后再加入450ml1mol/L的氢氧化钠溶液,所得沉淀中无Al(OH)3。满足此条件a的取值范围是__ ___。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
以下是对金属及其化合物的讨论,根据要求回答问题
(1)写出钠与水反应的离子方程式 。
(2)在AlCl3溶液中逐滴滴入过量的NaOH溶液,观察到的现象是 ,
反应的离子方程式为 , 。
(3)铝分别与足量的NaOH溶液和稀硫酸反应,若两个反应在相同状况下放出等量的气体,则两个反应中消耗的铝的物质的量之比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是 。
(2)另称取铁钉6.0g放入15.0ml浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+,若要确认其中的Fe2+,应选用 (选填序号)。
a.KSCN溶液和氯水 b.NaOH溶液
c.浓氨水 d.酸性KMnO4溶液
②乙同学取336ml(标准状况)气体Y通入足量溴水中,发生反应:
SO2+Br2+2H2O=2HBr+H2SO4然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由此推知气体Y中SO2的体积分数为 。
分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含有H2和Q气体。为此设计了下列探究实验装置(图中夹持仪器省略)。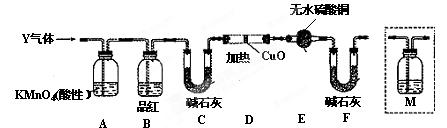
(3)装置B中试剂的作用是 。
(4)认为气体Y中还含有Q的理由是 (用化学方程式表示)。
(5)为确认Q的存在,需在装置中添加M于 (选填序号)。
a.A之前 b.A-B间 c.B-C间 d.C-D间
(6)如果气体Y中含有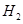 ,预计实验现象应是 。
,预计实验现象应是 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
铝是一种应用广泛的金属,工业上用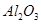 和冰晶石(
和冰晶石(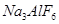 )混合熔融电解制得。
)混合熔融电解制得。
①铝土矿的主要成分是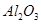 和
和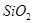 等。从铝土矿中提炼
等。从铝土矿中提炼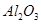 的流程如下:
的流程如下: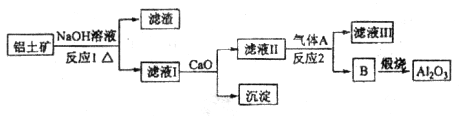
②以萤石(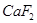 )和纯碱为原料制备冰晶石的流程如下:
)和纯碱为原料制备冰晶石的流程如下: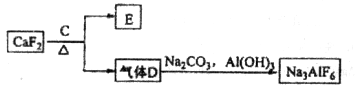
回答下列问题:
(1)写出反应1的化学方程式_________________________、________________________________;
(2)滤液Ⅰ中加入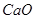 生成的沉淀是___________,反应2的离子方程式为____ ___________________
生成的沉淀是___________,反应2的离子方程式为____ ___________________
(3)E常用作制作豆腐的添加剂,化合物C是____,写出由D制备冰晶石的化学方程式_______________;
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
从辉铜矿(Cu2S)中利用火法炼铜可以提取铜,发生如下反应:
下面是由Cu2S冶炼铜及制取CuSO4·5H2O的流程图:
⑴Cu2S中铜元素的化合价为 ,当有1molCu2S与O2反应生成2molCu时,转移电子的物质的量是 。
⑵Cu2O、CuO中加入足量稀硫酸得到的体系A中看到溶液呈蓝色,且有红色物质生成,请写出生成红色物质的离子方程式 。
⑶若使A中单质溶解,操作Ⅰ中加入的试剂最好是 。(选填字母代号)
A.适量的HNO3 B.适量的NaOH C.适量的H2O2
该反应的离子方程式为 。
⑷取5.00 g胆矾样品逐渐升高温度使其分解,分解过程的热重曲线(样品质量随温度变化的曲线)如下图所示:
①由图中可以看出,胆矾分解的最低温度是 。
②通过计算确定258℃时发生反应的化学方程式为 ,e点对应的化学式为 (计算过程略去)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某研究性学习小组对铝热反应实验展开研究。现行高中化学教材中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | -- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
在中学化学中铁及其化合物应用广泛,用所学知识回答下列问题。
(1)将一定量的铁粉在氯气中燃烧后所得固体溶于水可得到溶液X。取少量X溶液两份,一份加入KSCN溶液时,溶液显红色;另一份中加入酸性KMnO4溶液时,KMnO4溶液紫色褪去。试分析:
①溶液X含有的金属阳离子应该是 。
②用化学方程式表示上述金属阳离子产生的原因 。
③酸性KMn04溶液紫色褪去的离子方程式为 。
(2)含铬化合物有毒,通常是将废水中+6价铬(如Cr2O2—7)用还原剂还原成Cr3+,再调节溶液pH使Cr3+转化为Cr(OH)3沉淀而除去。工业上有一种电解除Cr2O2—7的方法:将含K2Cr2O7的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解。
试分析该电解除Cr2O2—7的方法中:
①阴极的电极反应式为 ;
②电解时加入氯化钠的作用是 ;
③该方法能除去Cr2O2—7的原理是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com