
【题目】下列物质间的转化不能一步反应完成的是( )
A.Si→SiO2B.C→Si
C.SiO2→Na2SiO3D.SiO2→H2SiO3
科目:高中化学 来源: 题型:
【题目】下列各组物质中,存在X→Y或Y→Z不能通过一步反应完成转化的一组是
选项 | X | Y | Z |
A | Al | NaAlO2(aq) | Al(OH)3 |
B | MgO | MgCl2(aq) | Mg |
C | H2O(g) | Fe3O4 | Fe |
D | NaOH(aq) | Na2CO3(aq) | NaHCO3(aq) |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0价,部分为-2价。如图为超氧化钾晶体的一个晶胞,则下列说法中正确的是

A. 超氧化钾的化学式为KO2
B. 每个晶胞中含有8个K+和4个![]()
C. 晶体中与每个K+距离最近的K+有8个![]()
D. 晶体中0价氧原子和-2价氧原子个数比为3∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下图点滴板上进行四个溶液间反应的小实验,其对应反应的离子方程式书写正确的是( )

A. a反应:Fe2++2H++H2O2=Fe3++2H2O
B. b反应:HCO3-+OH-=CO32-+H2O
C. c反应:H++OH-=H2O
D. d反应:Al3++3NH3·H2O=Al(OH)3↓+3NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用苯甲醛在浓氢氧化钠溶液中制备苯甲醇和苯甲酸,反应如下:

已知:
①苯甲酸在水中的溶解度为:0.18g(4℃)、0.34g(25℃)、0.95g(60℃)、6.8g(95℃).
②乙醚沸点34.6℃,密度0.7138,易燃烧,当空气中含量为1.83~48.0%时易发生爆炸.
③石蜡油沸点高于250℃
④苯甲醇沸点为205.3℃

实验步骤如下:
①向图1所示装置中加入8g氢氧化钠和30mL水,搅拌溶解,稍冷,加入10mL苯甲醛.开启搅拌器,调整转速,使搅拌平稳进行,加热回流约40min;
②停止加热,从球形冷凝管上口缓缓加入冷水20mL,摇动均匀,冷却至室温.然后用乙醚萃取三次,每次10mL.水层保留待用.合并三次萃取液,依次用5mL饱和亚硫酸氢钠溶液洗涤,10mL 10%碳酸钠溶液洗涤,10mL水洗涤,然后分液,将水层弃去,所得醚层进行实验步骤③;
③将分出的醚层,倒入干燥的锥形瓶中,加无水硫酸镁,注意锥形瓶上要加塞;将锥形瓶中溶液转入图3所示的蒸馏装置,先缓缓加热,蒸出乙醚;蒸出乙醚后必须改变加热方式、冷凝方式,继续升高温度并收集205℃~206℃的馏分得产品A;
④将实验步骤②中保留待用的水层慢慢地加入到盛有30mL浓盐酸和30mL水的混合物中,同时用玻璃棒搅拌,析出白色固体.冷却,抽滤,得到粗产品,然后提纯得产品B。
根据以上步骤回答下列问题:
(1)步骤②萃取时用到的玻璃仪器除了烧杯、玻璃棒外,还需___________(仪器名称)。
(2)步骤②中饱和亚硫酸氢钠溶液洗涤是为了除去___________,而用碳酸钠溶液洗涤是为了除去醚层中极少量的苯甲酸,醚层中少量的苯甲酸是从水层转移过来的,请用离子方程式说明其产生的原因_______________________________________。
(3)步骤③中无水硫酸镁的作用是___________,锥形瓶上要加塞的原因是___________,产品A为___________。
(4)步骤③中蒸馏除去乙醚的过程中采用的加热方式为___________;蒸馏得产品A的加热方式是___________。
(5)步骤④中提纯产品B时所用到的实验方法为___________。
(6)步骤④中的抽滤又叫减压过滤,装置如图所示。其中抽气泵接自来水龙头的作用是_________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝的单质及其化合物在生产、生活、科研等领城应用广泛。
Ⅰ、工业上用铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)制备铝的某种化合物的工艺流程如下:
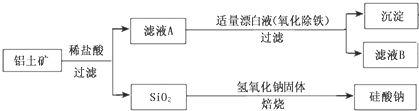
(1)加入盐酸时,氧化铝发生反应的离子方程式为______
(2)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。该过程中涉及某氧化还原反应如下,请完成:Fe2++___ClO-+ ═ Fe(OH)3↓+ Cl-+__________
Ⅱ、明矾在日常生活、生产中也占有一席之地。
(3)明矾是净水明星,用离子方程式表示其净水原理_____________________________。
(4)向0.02mol的明矾溶液中逐滴加入150mL0.2mol/LBa(OH)2溶液,生成沉淀的质量为 _____克。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组对钠在CO2气体中燃烧进行了下列实验:
操作过程 | 实验现象 |
将干燥纯净的CO2缓缓通过放有钠的干燥玻璃管(已排尽空气)中,加热 | 钠燃烧,火焰为黄色 |
反应后冷却 | 管壁附有黑色颗粒和白色物质 |
(1)若钠着火,可以选用的灭火物质是__________。
A.水 B.泡沫灭火剂 C.干沙土 D.二氧化碳
(2)该小组同学对管壁的白色物质的成分进行讨论并提出假设:
Ⅰ.白色物质可能是Na2O; Ⅱ.白色物质可能是Na2CO3; Ⅲ.白色物质还可能是__________
(3)为确定该白色物质的成分,该小组进行了如下实验:
实验步骤 | 实验现象 |
①少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加过量的CaC12溶液 | 出现白色沉淀 |
②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
①通过对上述实验的分析,你认为上述三个假设中,__________成立。
②该白色物质的水溶液pH>7,用离子方程式表示其原因:___________________。
③钠在CO2中燃烧的化学方程式为______;每生成1mol氧化产物,转移的电子数目为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸溶液与氨水反应的离子方程式正确的是
A.OH-+ H+= H2O
B.NH3·H2O+H+= NH4+ + H2O
C.OH-+ HAc = Ac-+ H2O
D.NH3·H2O + HAc =NH4+ + Ac-+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方法中,不能用于实验室里制取氨气的是
A. 在试管中将熟石灰和氯化铵混合后加热
B. 加热试管中的氯化铵固体
C. 将烧瓶中的浓氨水加热
D. 将分液漏斗中的浓氨水滴入装有生石灰的烧瓶中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com