
����Ŀ����ͼʵ��װ��������֤ijЩ���ʵ����ʡ����Թ�A��װ�������Ĺ���NaHCO3��DΪ�̶������ӲֽƬ���Իش��������⣺

(1)A�Թ��ڷ�����Ӧ________________________________��
(2)Bװ�õ�������___________________________________��
(3)��˫�������ڷ�����Ӧ�Ļ�ѧ����ʽΪ________________________________������Bװ����˫�������л����Է����Ļ�ѧ��Ӧ����ʽΪ_______________��
(4)˫�������ڹ۲쵽��ʵ��������______________________��
(5)����������ڵ�Na2O2����Na2O����˫�������ڹ۲쵽��ʵ��������__________��
���𰸡�2NaHCO3![]() Na2CO3��H2O��CO2�� ���������е�ˮ����(����CO2) 2Na2O2��2CO2===2Na2CO3��O2 2Na2O2��2H2O===4NaOH��O2�� ����ɫ��Na2O2��ת��Ϊ��ɫ��ĩ����ȼ������ȼ�ո��Ӿ��� ��ȼ��������Ϩ��
Na2CO3��H2O��CO2�� ���������е�ˮ����(����CO2) 2Na2O2��2CO2===2Na2CO3��O2 2Na2O2��2H2O===4NaOH��O2�� ����ɫ��Na2O2��ת��Ϊ��ɫ��ĩ����ȼ������ȼ�ո��Ӿ��� ��ȼ��������Ϩ��
��������
��ʵ��װ�ÿ�֪������A����2NaHCO3![]() Na2CO3��H2O��CO2����B��Ũ�������CO2��C�з���2Na2O2+2CO2��2Na2CO3+O2��������ʹ��ȼ������ȼ�ո���������������ڵ�Na2O2����Na2O����ȼ��������Ϩ����ʵ�����֤CO2��Na2O2�ķ�Ӧ���Դ������
Na2CO3��H2O��CO2����B��Ũ�������CO2��C�з���2Na2O2+2CO2��2Na2CO3+O2��������ʹ��ȼ������ȼ�ո���������������ڵ�Na2O2����Na2O����ȼ��������Ϩ����ʵ�����֤CO2��Na2O2�ķ�Ӧ���Դ������
��1��̼�����Ʋ��ȶ��������ֽ⣬����A�Թ��ڷ�����Ӧ�Ļ�ѧ����ʽ��2NaHCO3![]() Na2CO3��H2O��CO2����
Na2CO3��H2O��CO2����
��2���������ɵ�CO2�����к���ˮ����������Ũ���������������ˮ����������CO2��
��3��CO2�ܺ������Ʒ�Ӧ����̼���ƺ���������Ӧ�Ļ�ѧ����ʽΪ2Na2O2��2CO2��2Na2CO3��O2������Bװ�ã�����ˮ����������˫�������л����Է����Ļ�ѧ��Ӧ����ʽΪ2Na2O2��2H2O��4NaOH��O2����
��4��CO2�ܺ������Ʒ�Ӧ����̼���ƺ�����������ʵ�������ǵ���ɫ��Na2O2��ת��Ϊ��ɫ��ĩ����ȼ������ȼ�ո��Ӿ��ҡ�
��5������������ڵ�Na2O2����Na2O���������������̼��Ӧ����̼���ƣ�������̼��֧������ȼ�գ���ʵ��ʱ�۲쵽��ʵ�������ǵ�ȼ��������Ϩ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���H��һ���������˷ܼ�����ϳ�·������ͼ��ʾ��
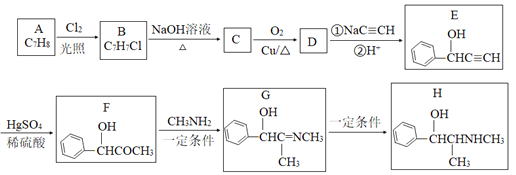
��ش������⣺
��1��A�Ļ�ѧ����Ϊ_________��C�Ľṹ��ʽΪ________��
��2��E�й����ŵ�����Ϊ________��B��C��G��H�ķ�Ӧ���ͷֱ�Ϊ________��________��
��3��D�����������_____��ԭ�ӹ�ƽ�档
��4��F��G����������Ӧ����һ����Ӧ�Ļ�ѧ����ʽΪ______________��
��5��ͬʱ��������������F��ͬ���칹����_____��(�����������칹)��
���ܷ���������Ӧ���������Ȼ�����Һ��Ӧ���۷�����ֻ��1������
���к˴Ź���������6���Ľṹ��ʽΪ__________��
��6�����������ϳ�·�ߺ���Ϣ������ϩΪԭ���Ʊ�ǿ��ˮ����֬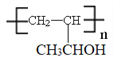 �ĺϳ�·������ͼ����ѡ�����������Լ������Լ���ѡ��_____________________________��
�ĺϳ�·������ͼ����ѡ�����������Լ������Լ���ѡ��_____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Һ��һ�����ʵ���Ũ��ΪC1mol/L���ܶ�Ϊ��1g/cm3����һ�����ʵ���Ũ��ΪC2mol/L���ܶ�Ϊ��2g/cm3�������ǵ������Ϻ���Һ���ܶ�Ϊ��3g/cm3��������Һ�����ʵ���Ũ��Ϊ
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������̼�IJ������������ҹ���Դ�����һ����Ҫս�Է���ҵ����CO2��H2��Ӧ�ϳɼ��ѡ���֪��
CO2(g)��3H2(g)��CH3OH(g)��H2O(g) ��H1����53.7 kJ��mol��1
CH3OCH3(g)��H2O(g)��2CH3OH(g)��H2����23.4 kJ��mol��1
��1����Ӧ2CO2(g)��6H2(g) ![]() CH3OCH3(g)��3H2O(g) ��H3��________kJ��mol��1��
CH3OCH3(g)��3H2O(g) ��H3��________kJ��mol��1��
��2��һ�������£������ϳɼ��ѵķ�Ӧ�ﵽƽ��״̬�����ı䷴Ӧ��ijһ�����������б仯��˵��ƽ��һ��������Ӧ�����ƶ�����________(����ĸ)��
a������Ӧ������������С b��H2��ת��������
c�������������ٷֺ������� d�������е�![]() ֵ��С
ֵ��С
��3����ijѹǿ�£��ϳɼ��ѵķ�Ӧ�ڲ�ͬ�¶ȡ���ͬͶ�ϱ�ʱ��CO2��ת��������ͼ��ʾ��T1�¶��£���4mol CO2��8 mol H2����2 L���ܱ������У�10min ��Ӧ�ﵽƽ��״̬����0��10min�ڵ�ƽ����Ӧ����v(CH3OCH3)��________________��KA��KB��KC����֮��Ĵ�С��ϵΪ____________________��
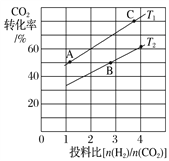
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ����������������ϡ���ἰ������CuO�Ƶ���ͭ������������������ַ�����
��Fe![]() H2
H2![]() Cu ��CuO
Cu ��CuO![]() CuSO4
CuSO4![]() Cu
Cu
����ʵ��ԭ����в������������Ƶõ���ͭ����Ϊ
A. һ���� B. �ٶ� C. �ڶ� D. ���ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��KIO3��ʳ�õ��ε����Ӽ�����ҵ����ȡKIO3�ķ���֮һ��ͼ��ʾ�����������������Ӹ�Ĥֻ����������������ͨ���������й�˵������ȷ���ǣ� ��
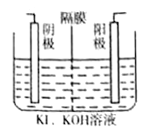
A. ��������������ʯī������
B. װ���еĸ�ĤΪ�����Ӹ�Ĥ
C. �����·��ͨ��2 mole-ʱ�������ϻ���22.4LH2����
D. �����缫��ӦʽΪ��I--6e-+6OH-=IO3-+3H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������Ȼ�ѧ����ʽ�ó��Ľ�����ȷ���ǣ� ��
A. ��֪2SO2(g)+O2 ![]() 2SO3(g) Ϊ���ȷ�Ӧ����SO2������һ������SO3������
2SO3(g) Ϊ���ȷ�Ӧ����SO2������һ������SO3������
B. ��֪C(ʯī,s)=C(���ʯ,s) ��H��0������ʯ��ʯī�ȶ�
C. ��֪H+(aq)+OH-(aq)=H2O(1),��H=��57.3kJ/mol�����κ�����кͷ�Ӧ����ЧӦ��Ϊ57.3 kJ
D. ��֪2C(s)+2O2(g)=2CO2(g) ��H1��2C(s)+O2(g)=2CO(g) ��H2 ����H1����H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2L���ܱ�������,�������·�Ӧ:2A(g)+ B(g) ![]() 2C(g)+D(g) ������������A��B����4 mol����ǰ10����A��ƽ����Ӧ�ٶ�Ϊ0.12 mol/��L������10����ʱ��������B�����ʵ������� ��
2C(g)+D(g) ������������A��B����4 mol����ǰ10����A��ƽ����Ӧ�ٶ�Ϊ0.12 mol/��L������10����ʱ��������B�����ʵ������� ��
A. 1.6 mol B. 2.8 mol
C. 2.4 mol D. 1.2 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ���ǣ� ��
A. ����Ͷ�뵽NaOH��Һ�У�2Al+2OH��+2H2O�T�T 2AlO2��+3H2��
B. AlCl3��Һ�м��������İ�ˮ��Al3++ 3OH- �T�T Al(OH)3��
C. ���Ȼ�����Һ�м�������![]()
D. FeCl2��Һ��Cl2��Ӧ��2Fe2++Cl2=2Fe3++2Cl-
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com