
【题目】二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。工业上用CO2和H2反应合成甲醚。已知:
CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH1=-53.7 kJ·mol-1
CH3OCH3(g)+H2O(g)=2CH3OH(g)ΔH2=+23.4 kJ·mol-1
(1)反应2CO2(g)+6H2(g) ![]() CH3OCH3(g)+3H2O(g) ΔH3=________kJ·mol-1。
CH3OCH3(g)+3H2O(g) ΔH3=________kJ·mol-1。
(2)一定条件下,上述合成甲醚的反应达到平衡状态后,若改变反应的某一个条件,下列变化能说明平衡一定向正反应方向移动的是________(填字母)。
a.正反应速率先增大后减小 b.H2的转化率增大
c.生成物的体积百分含量增大 d.容器中的![]() 值变小
值变小
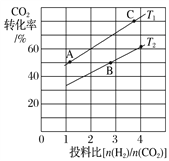
(3)在某压强下,合成甲醚的反应在不同温度、不同投料比时,CO2的转化率如下图所示。T1温度下,将4mol CO2和8 mol H2充入2 L的密闭容器中,10min 后反应达到平衡状态,则0~10min内的平均反应速率v(CH3OCH3)=________________;KA、KB、KC三者之间的大小关系为____________________。
【答案】 -130.8 ab 0.06mol·L-1·min-1 KA=KC>KB
【解析】(1)已知:①CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H1=-53.7kJmol-1,②CH3OCH3(g)+H2O(g)═2CH3OH(g) △H2=+23.4kJmol-1,根据盖斯定律,①×2-②可得:2CO2(g)+6H2(g)CH3OCH3(g)+3H2O(g) △H3=2△H1-△H2=2×(-53.7kJmol-1)-23.4kJmol-1 =-130.8kJmol-1,故答案为:-130.8;
(2)①a.正反应速率先增大后减小,可能是增大反应物浓度,平衡正向移动,故a正确;b.H2的转化率增大,平衡一定正向移动,故b正确;c.反应物的体积百分含量减小,可能是增大生成物浓度,平衡逆向移动,故c错误;d.容器中的![]() 变小,可能是减小二氧化碳物质的量,平衡逆向移动,故d错误;故答案为:ab;
变小,可能是减小二氧化碳物质的量,平衡逆向移动,故d错误;故答案为:ab;
(3)T1温度下,将4molCO2和8molH2充入2L的密闭容器中,由图象可知,10min后反应达到平衡状态时二氧化碳转化率为60%,则生成CH3OCH3为4mol×60%×![]() =1.2mol,所以平均反应速率v(CH3OCH3)=
=1.2mol,所以平均反应速率v(CH3OCH3)= 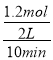 =0.06molL-1min-1 ;平衡常数仅与温度有关,温度不变,平衡常数不变,所以KA=KC,在相同投料比时,T1温度下二氧化碳转化率大,所以T1温度下正向进行程度比T2温度大,则KA=KC>KB,故答案为:0.06 mol/(Lmin);KA=KC>KB。
=0.06molL-1min-1 ;平衡常数仅与温度有关,温度不变,平衡常数不变,所以KA=KC,在相同投料比时,T1温度下二氧化碳转化率大,所以T1温度下正向进行程度比T2温度大,则KA=KC>KB,故答案为:0.06 mol/(Lmin);KA=KC>KB。


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】下列溶液中微粒的物质的量浓度关系正确的是
A. 0.lmol/L的NH4Cl溶液与0.05mol/L的NaOH溶液等体积混合后的溶液: c(C1-)>c(NH4+)>c(Na+)>c(OH-)>c(H+)
B. 等物质的量的NaC1O、NaHCO3混合溶液中: c(HC1O)+c(C1O-)=c(HCO3-)+c(H2CO3)+2c(CO32-)
C. pH=2 的HA溶液与pH=12的NaOH溶液等体积混合: c(Na+)=c(A-)>c(OH-)=c(H+)
D. 某二元弱酸的酸式盐NaHA 溶液中:c (OH-)+c(H2A) =c(H+)+2c(A-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是
A. 增加c(CO),平衡向正向移动,反应的平衡常数增大
B. 第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
C. 第二阶段,Ni(CO)4分解率较低
D. 该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O中,下列说法正确的是( )
A. 氧化产物与还原产物物质的量之比是2∶5
B. 被氧化的HCl占参加反应HCl总分子数的![]()
C. KMnO4只有一部分发生还原反应
D. KMnO4与HCl恰好分别完全发生还原反应和氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列说有关说法正确的是
A. 在常温常压下,11.2L N2含有的分子数小于0.5NA
B. 标准状况下,2.24L SO3含有的原子数为0.4NA
C. 将1L 2mol/L的FeCl3溶液,其中含有Cl-为2NA
D. 46g NO2和N2O4混合气体所含氧原子数目有可能为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图实验装置用于验证某些物质的性质。在试管A中装入足量的固体NaHCO3,D为固定蚊香的硬纸片。试回答下列问题:

(1)A试管内发生反应________________________________。
(2)B装置的作用是___________________________________。
(3)在双球干燥管内发生反应的化学方程式为________________________________,若无B装置则双球干燥管中还可以发生的化学反应方程式为_______________。
(4)双球干燥管内观察到的实验现象是______________________。
(5)若将干燥管内的Na2O2换成Na2O,则双球干燥管内观察到的实验现象是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法不正确的是
A. 22g3H2O中所含中子的数目为12NA
B. 1LpH=1 H3PO4溶液中所含H+的数目为0.1NA
C. 叠氮化铵(NH4N3)发生爆炸反应:NH4N3==2N2↑+2H2↑,当产生标准状况下22.4L气体时,转移电子的数目为NA
D. 1mol乙酸与3molC2H5OH充分反应生成CH3COOC2H5分子的数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如图1所示.
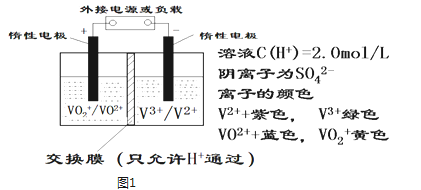
①当左槽溶液逐渐由黄变蓝,其电极反应式为 ___ .
②充电过程中,右槽溶液颜色逐渐___ 色变为___ 色.
③放电过程中氢离子的作用是___ ___ ;充电时若转移的电子数为3.01×1023个,左槽溶液中n(H+)的变化量为 ___ .
(1)若负载是镀铜的电镀槽,则纯铜应该连接___ 槽(填左或右)中的电极.
(2)若负载是用石墨作电极,用3mol/L KCl和0.5mol/L Al2(SO4)3的混合溶液作电解液的电解池时,图2电解变化的曲线合理的是___
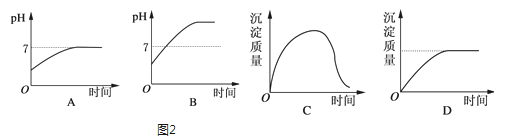
(3)电解法处理污水已经得到广泛的应用.若负载是酸性介质中将有毒的Cr2O72﹣转变为Cr3+的电解池.装置如图3所示,请用文字描述其工作原理___
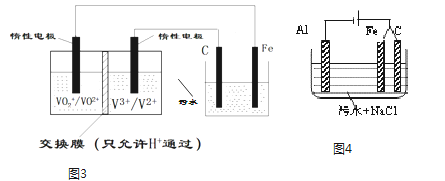
(4)若负载是进行三电极法污水处理的电解池原理如图4所示,增加的铁电极的可能作用是___
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com