
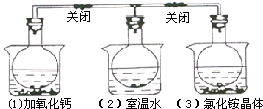
 如图所示,三个烧瓶中分别充满NO2气体,并分别放置在盛有下列物质的烧杯中(烧杯内有水):在(1)中加入CaO,在(2)中不加其他任何物质,在(3)中加入NH4Cl晶体,发现(1)中红棕色变深,(3)中红棕色变浅,下列叙述正确的是( )
如图所示,三个烧瓶中分别充满NO2气体,并分别放置在盛有下列物质的烧杯中(烧杯内有水):在(1)中加入CaO,在(2)中不加其他任何物质,在(3)中加入NH4Cl晶体,发现(1)中红棕色变深,(3)中红棕色变浅,下列叙述正确的是( )| A、烧瓶(3)中气体的压强增大 |
| B、NH4Cl溶于水时放出热量 |
| C、烧瓶(1)中平衡时混合气体的平均相对分子质量增大 |
| D、2NO2?N2O4是放热反应 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
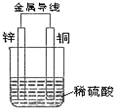
| A、铜片上有气泡逸出 |
| B、溶液的SO42-浓度逐渐减小 |
| C、电子由铜片经导线流向锌片 |
| D、该装置能将电能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某钠盐溶于盐酸产生能使澄清石灰水变浑浊的无色无味气体,说明该钠盐是Na2CO3 |
| B、用饱和Na2CO3溶液除去CO2中混有的HCl |
| C、工业上常采用电解熔融MgO的方法制取金属镁 |
| D、除去MgCl2溶液中少量FeCl3可向其中加入足量Mg(OH)2粉末,充分搅拌后过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、8句 | B、6句 | C、5句 | D、7句 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 不纯物质 | 除杂试剂 | 分离方法 | |
| A | 苯(甲苯) | KMnO4(酸化),NaOH溶液 | 分液 |
| B | NH4Cl溶液(FeCl3) | NaOH溶液 | 过滤 |
| C | 乙酸乙酯(乙酸) | KOH溶液,水 | 分液 |
| D | CO2(SO2) | Na2CO3 | 洗气 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
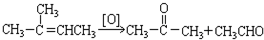
 在上述类似条件下发生反应,请写出反应的方程式:
在上述类似条件下发生反应,请写出反应的方程式:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:2 | B、1:1 |
| C、1:3 | D、任意比 |
查看答案和解析>>
科目:高中化学 来源: 题型:
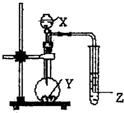 如图示的装置中,把X溶液逐滴滴下与Y物质反应,若X为浓硫酸,Y为第三周期金属元素中常温下与水难反应的单质.Z为品红溶液.实验中观察到Z褪色.则Y为( )
如图示的装置中,把X溶液逐滴滴下与Y物质反应,若X为浓硫酸,Y为第三周期金属元素中常温下与水难反应的单质.Z为品红溶液.实验中观察到Z褪色.则Y为( )| A、Na | B、Mg |
| C、Al | D、Mg或Al |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com