
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | |
 2Fe+Al2O3 2Al+2OH-+2H2O===2AlO+3H2↑
2Fe+Al2O3 2Al+2OH-+2H2O===2AlO+3H2↑

科目:高中化学 来源:不详 题型:单选题
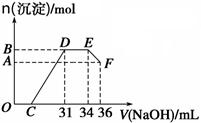
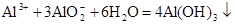 过程的是
过程的是| A.向铝盐溶液中不断滴加氢氧化钠溶液 |
| B.向偏铝酸盐溶液中不断加入盐酸 |
| C.向偏铝酸钠溶液中不断通入二氧化碳气体 |
| D.向氢氧化钠溶液中不断滴加铝盐溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铝是地壳里含量最多的金属元素 | B.在常温下,铝不能和氧气反应 |
| C.铝是一种比较活泼的金属 | D.在化学反应中,铝容易失去电子,是还原剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1︰1 | B.3︰2 | C.2︰3 | D.28︰9 |
查看答案和解析>>
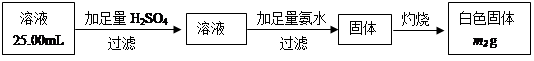
科目:高中化学 来源:不详 题型:填空题
| 实验步骤 | 预期实验现象和结论 |
| 步骤1:将反应所得浊液过滤、洗涤,取少量固体于试管中,加入足量的6mol·L-1 H2SO4溶液,充分振荡,静置。 | ___________________________________, 证明黑色固体含有Si |
| 步骤2: | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
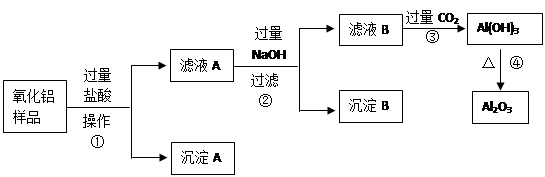
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1:2 | B.1:1 | C.1:3 | D.2:1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.4mol/L | B.0.5mol/L | C.0.6mol/L | D.1mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com