
【题目】下列指定反应的离子方程式正确的是( )
A.将铜丝插入稀硝酸中:Cu+4H++2NO3-![]() Cu2++2NO2↑+H2O
Cu2++2NO2↑+H2O
B.向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe![]() 2Fe2+
2Fe2+
C.向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3·H2O![]() Al(OH)3↓+3NH4+
Al(OH)3↓+3NH4+
D.向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+![]() H2SiO3↓+2Na+
H2SiO3↓+2Na+
科目:高中化学 来源: 题型:
【题目】对Cl2的叙述正确的是
A. 能用钢瓶贮存B. 与过量的Fe反应只生成FeCl2
C. 与H2混合光照可制取HClD. 与澄清石灰水反应制取漂粉精
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】融雪剂通过降低冰雪融化温度的原理融化道路上的积雪。研究发现,一般融雪剂残留物可腐蚀路面和汽车轮胎等。目前我国北方在冬季仍采用沙土和铲雪车为主,融雪剂为辅的方式清除路面冰雪,保证道路通畅。
请回答下列问题:
(1)氯化钙是常用融雪剂的主要成分之一,以工业碳酸钙(含有少量Na+、Mg2+、Fe3+等杂质)生产氯化钙的主要流程如下:

①流程中试剂W的名称是 ________________。
②流程中滤渣的主要成分是________________(填化学式)。
③流程中操作Y的目的是_______________。
④如果用惰性电极电解用试剂W溶解后的溶液,则电解开始时阴极发生的电极反应式为_________。
(2)下列就融雪剂使用的有关原理的解释正确的是_________________。
A.“会加快冰雪的融化”是因为提高了冰点
B.“会造成绿化植物死亡”是与盐析有关
C.“会造成土壤板结贫瘠”是与物质的分解吸热有关
D.“会加快路基上铁的腐蚀”是与形成原电池有关
(3)某公司生产的融雪剂由NaCl、NaNO3、AlCl3、CuSO4、K2CO3中的几种物质组成。某同学设计下列过程探究其组成:
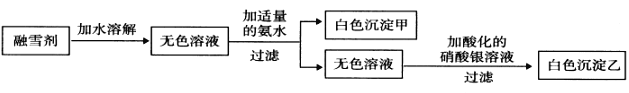
请回答下列问题:
①该融雪剂中一定不含的物质是_________________(填名称)。
②若取融雪剂样品a g,通过上述探究途径得白色沉淀乙bmol,则该融雪剂中含氯元素的质量分数为 ____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.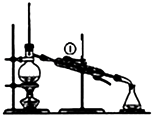 装置可用于实验室制取蒸馏水,从①处通入冷却水
装置可用于实验室制取蒸馏水,从①处通入冷却水
B.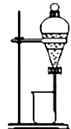 萃取操作时,所选萃取剂的密度必须要大于水的密度
萃取操作时,所选萃取剂的密度必须要大于水的密度
C.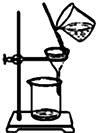 装置可用于除去固体BaCl2中的MgSO4
装置可用于除去固体BaCl2中的MgSO4
D.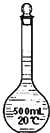 装置在配制一定物质的量浓度的溶液之前无需润洗
装置在配制一定物质的量浓度的溶液之前无需润洗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标况下,m g气体A与n g气体B的分子数目一样多,以下说法不正确的是( )
A.在任意条件下,若两种分子保持原组成,则其相对分子质量之比为m:n
B.25℃,1.25×105 Pa时,两气体的密度之比为n:m
C.同质量的A,B在非标准状况下,其分子数之比为n:m
D.相同状况下,同体积的气体A与B的质量之比为m:n
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:周期表中前四周期的六种元素A、B、C、D、E、F核电荷数依次增大,其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的熔点在同周期元素形成的单质中是最高的;F2+离子核外各层电子均充满。请根据以上信息,回答下列问题:
(1)A、B、C、D的第一电离能由小到大的顺序为____。(用元素符号表示)
(2)B的氯化物的熔点比D的氯化物的熔点高,理由是____________________。
(3)E的最高价氧化物分子的空间构型是__________,是____分子(填“极性”“非极性”)。
(4)F原子的核外电子排布式是________________。
(5)E、F形成某种化合物有如图所示两种晶体结构(深色球表示F原子),其化学式为_________。(a)中E原子的配位数为____。若在(b)的结构中取出一个平行六面体作为晶胞,则平均一个晶胞中含有____个F原子。结构(a)与(b)中晶胞的原子空间利用率相比,(a)____(b)(填“>”“<”或“=”)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com