
【题目】下列说法中不正确的是
A.宇宙星体、地球内部都处于高压状态,探究“高压下钠和锂单质金属![]() 绝缘体转变”现象的本质、理解处于高压状态下一些物质的行为具有重要意义,它们可以为研究星体和地球内部构造提供理论支持
绝缘体转变”现象的本质、理解处于高压状态下一些物质的行为具有重要意义,它们可以为研究星体和地球内部构造提供理论支持
B.工业、农业以及日常生活中产生的污水应当分开处理.常用的污水处理方法有中和法、氧化还原法、离子交换法、萃取法、吹脱法、吸附法、电渗析法等,其中前三种属于化学处理方法
C.新型炸药--![]() 塑胶炸药得名于其空间网状延展结构的每个结构基元含有4个碳原子,由于该炸药成体时无需包裹金属外壳及添加金属芯件,因此能轻易躲过普通X光安全检查,具有较强的隐蔽性
塑胶炸药得名于其空间网状延展结构的每个结构基元含有4个碳原子,由于该炸药成体时无需包裹金属外壳及添加金属芯件,因此能轻易躲过普通X光安全检查,具有较强的隐蔽性
D.建筑领域常使用的黏土、石英、白垩石和多用于农业和食品工业的硅藻土、硅胶均不属于硅酸盐材料的范畴
【答案】C
【解析】
A.高压下金属钠转变为透明绝缘体的奇异现象,破解了金属锂的高压半导体相的结构谜团,实现了高压下金属![]() 绝缘体转变这一高压相变领域多年期盼的科学夙愿,突破了固体高压金属化的传统观点和认识,为研究星体和地球内部构造提供理论支持,故A正确;
绝缘体转变这一高压相变领域多年期盼的科学夙愿,突破了固体高压金属化的传统观点和认识,为研究星体和地球内部构造提供理论支持,故A正确;
B.现代废水处理方法主要分为物理处理法、化学处理法和生物处理法三类,化学处理法有:中和法、离子交换法、氧化还原法等;萃取法、吹脱法、吸附法、电渗析法属于物理处理方法,故B正确;
C.若![]() 炸弹为空间网状结构的原子晶体,则其熔点很高、很难爆炸,实际上它是以
炸弹为空间网状结构的原子晶体,则其熔点很高、很难爆炸,实际上它是以![]() 为单元的分子晶体,故C错误;
为单元的分子晶体,故C错误;
D.硅酸盐材料的主要成分是含有硅酸盐,石英的主要成分是二氧化硅,硅藻土的主要成分是二氧化硅,硅胶又称为硅酸凝胶,是一种高活性吸附材料,属非晶态物质,其化学分子式为mSiO2·nH2O,一般的黏土都由硅酸盐矿物在地球表面风化后形成,成分主要为氧化硅与氧化铝,白垩石是一种白色疏松的土状石灰岩,其主要化学成分是CaCO3,以上物质主要成分都不是硅酸盐,不属于硅酸盐材料,故D正确;
答案选C。


 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:
【题目】H2与碱金属等单质在较高温度下可以化合形成离子型金属氢化物,如NaH、LiH等,它们具有极强的还原性,也是良好的野外生氢剂(NaH+H2O=NaOH+H2↑),下列说法不正确的是
A.金属氢化物具有强还原性的原因是其中的氢元素为-l价
B.NaH的电子式可表示为Na+[:H]-
C.NaAlH4与水反应:NaAlH4+H2O=NaOH+Al(OH)3+H2↑
D.工业上用有效氢含量衡量含氢还原剂的供氢能力,有效氢指单位质量(克)的含氢还原剂的还原能力相当于多少克氢气的还原能力。则LiAlH4的有效氢含量约为0.21
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤和石油不仅是重要的矿物能源,更可以通过综合利用得到多种有机化工产品。煤干馏后可得到焦炭、煤焦油、粗氨水和焦炉气等。焦炭可通过以下途径制取聚氯乙烯等化工产品。
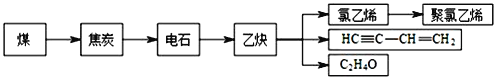
完成下列填空:
(1)石油化工生产乙烯的操作名称为___,乙炔的分子空间构型是____,由乙炔生产HC≡C-CH=CH2的基本反应类型是___。在石油生产乙烯的过程中会产生副产品异戊烯,通过催化脱氢法得到异戊二烯,进而通过1,4-加聚反应得到异戊橡胶,由异戊二烯生产异戊橡胶的化学方程式为:___。
(2)乙炔可用来合成聚氯乙烯。请以乙炔为原料,无机试剂任选,设计聚氯乙烯的合成路线。____
(合成路线常用的表示方式为:![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛(Ti)被称为继铁、铝之后的第三金属,钛白(TiO2)是目前最好的白色颜料。制备TiO2和Ti的原料是钛铁矿,我国的钛铁储量居世界首位。含Fe2O3的钛铁矿(主要成分为FeTiO3)制备TiO2流程如下:

(1)步骤①加Fe的目的是__;步骤②冷却的目的是__。
(2)上述制备TiO2的过程中,可以利用的副产物是__;考虑成本和废物综合利用因素,废液中应加入___处理。
(3)由金红石(TiO2)制取单质钛(Ti),涉及到的步骤为
![]() →
→![]()
![]()
![]()
反应TiCl4+2Mg=2MgCl2+Ti在Ar气氛中进行的理由是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关热化学方程式书写及对应表述均正确的是( )
A.已知2C(s)+O2(g)=2CO(g) △H=-22.1kJ·mol-1则可知C的燃烧热△H=-11.05kJ·mol-1
B.密闭容器中,9.6g硫粉与11.2g铁粉混合加热生成硫化亚铁17.6g时,放出19.12kJ热量.则Fe(s)+S(s) =FeS(s) △H=-95.6kJ·mol-1
C.已知1mol氢气完全燃烧生成液态水所放出的热量为285.5kJ,则水分解的热化学方程式:2H2O(l)=2H2(g) + O2(g) △H=+285.5kJ·mol-1
D.1L0.5mol/LH2SO4溶液与1L0.5mol/LBa(OH)2溶液完全反应生成1molH2O放出的热叫做中和热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某澄清透明溶液中只可能含有①Al3+,②Mg2+,③Fe3+,④Fe2+,⑤H+,⑥CO32-,⑦NO3-中的几种,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量与NaOH的物质的量的关系如图所示.则该溶液中一定含有的离子是![]()

A.⑤⑥⑦B.②③⑤⑦C.①②③⑥⑦D.①②③④⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理研究化学反应有重要意义。
(1)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)![]() 2SO3(g),混合体系中SO3的百分含量和温度的关系如图1所示(曲线上任何一点都表示平衡状态)。
2SO3(g),混合体系中SO3的百分含量和温度的关系如图1所示(曲线上任何一点都表示平衡状态)。
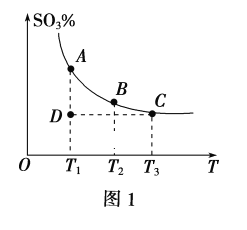
①若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡___(填“向左”“向右”或“不”)移动。
②若反应进行到状态D时,v正___(填“>”“<”或“=”)v逆。
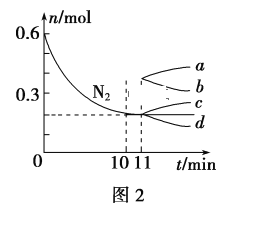
(2)已知N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,在某温度下,2L的密闭容器中发生合成氨的反应,图2表示N2的物质的量随时间的变化曲线。用H2表示0~10min内该反应的平均速率v(H2)=__。从第11min起,压缩容器的体积为1L,则n(N2)的变化曲线为___(填编号)。
2NH3(g) ΔH<0,在某温度下,2L的密闭容器中发生合成氨的反应,图2表示N2的物质的量随时间的变化曲线。用H2表示0~10min内该反应的平均速率v(H2)=__。从第11min起,压缩容器的体积为1L,则n(N2)的变化曲线为___(填编号)。
(3)298K时,将20mL3xmol·L-1 Na3AsO3、20mL3xmol·L-1I2和20 mLNaOH溶液混合,发生反应:AsO33-(aq)+I2(aq)+2OH-(aq)![]() AsO43-(aq)+2I-(aq)+H2O(l)。溶液中c(AsO43-)与反应时间(t)的关系如图所示。
AsO43-(aq)+2I-(aq)+H2O(l)。溶液中c(AsO43-)与反应时间(t)的关系如图所示。
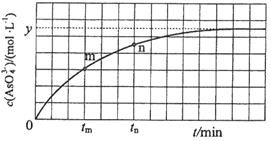
①下列可判断反应达到平衡的是___(填标号)。
a.溶液的pH不再变化 b.v(I-)=2v(AsO33-)
c.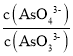 不再变化 d.c(I-)=y mol·L-1
不再变化 d.c(I-)=y mol·L-1
②tm时,v正___v逆(填“大于”“小于”或“等于”)。
③tm时v逆___tn时v逆(填“大于”“小于”或“等于”),理由是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在3A(g)+B(g) = 2C(g)+4D(g)反应中,表示该反应速率最快的是( )
A.v(C)=0.8 mol /(L·s)B.v(B)=0.3 mol/(L·s)
C.v(A)=0.5 mol /(L·s)D.v(D)=1 mol /(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学上常用燃烧法测定有机物的分子式,这种方法是在电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成。下图所示的是用燃烧法确定有机物分子式的常用装置。
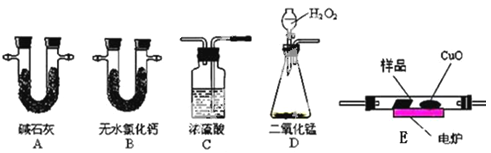
实验探究小组称取一定质量的样品(只含C、H、O三种元素中的两种或三种),进行实验,通过测定产生的CO2和水的质量确定有机物的组成,请回答下列问题:
(1)C中浓硫酸的作用是除去氧气中的水蒸气,实验装置的连接顺序应是:___________(每种装置只用一次);
(2)实验数据记录和处理
物理量实验序号 | 燃烧有机物的质量 | ① | ② | ||
实验前质量 | 实验后质量 | 实验前质量 | 实验后质量 | ||
1 | m1 | m2 | m3 | m4 | m5 |
上表中①、②分别指哪个装置?____________ 、 _____________。
(3)若实验准确称取4.4 g样品,经燃烧后测得产生CO28.8 g,水蒸气3.6g。要确定该有机物的分子式,还必须知道的数据是________;
(4)相同条件下,若该有机物蒸气对氢气的相对分子质量为22,且它的核磁共振氢谱上有两个峰,其强度比为3:1,试通过计算确定该有机物的结构简式___________,与该有机物相对分子质量相同的烃的一氯代物有_____种。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com