
将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g) 2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
①用物质A表示的反应平均速率为0.6 mol·L-1·s-1
②用物质B表示的反应的平均速率为0.15mol·L-1·s-1
③2s时物质A的转化率为30%
④2s时物质B的浓度为0.3 mol·L-1
其中正确的是
A.①③ B.①④ C.②③ D.③④
C
【解析】
试题分析:经2 s后测得C的浓度为0.6 mol·L-1,则C物质表示的反应速率是0.6mol/L÷2s=0.3mol/(L·s),反应速率之比是相应的化学计量数之比,因此A物质表示的反应速率是0.3mol/(L·s),①不正确;反应速率之比是相应的化学计量数之比,因此B物质表示的反应速率是0.3mol/(L·s)÷2=0.15mol/(L·s),②正确;经2 s后测得C的浓度为0.6 mol·L-1,则根据方程式可知消耗A物质的浓度是0.6mol/L,A物质的起始浓度是2mol/L,所以2s时物质A的转化率为30%,③正确;B的起始浓度是1mol/L,根据方程式知,△c(B)=0.15mol/(L·s)×2s =0.3mol/L,所以2s时物质B的浓度为:1mol/L-0.3mol/L=0.7 mol/L,故④错误;故选C。
考点:考查化学平衡的计算、化学反应速率的计算


 灵星计算小达人系列答案
灵星计算小达人系列答案科目:高中化学 来源:2015届江苏省苏州市高三9月学情调研化学试卷(解析版) 题型:选择题
下列指定反应的离子方程式正确的是
A.向苯酚钠溶液中通入少量的CO2:C6H5O-+CO2+H2O → C6H5OH+HCO3-
B.AlCl3溶液中加入少量氨水:Al3++3OH- = Al(OH)3↓
C.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH- = Fe(OH)2↓
D.用惰性电极电解氯化钠溶液:2Cl-+2H+ 通电 H2↑+Cl2↑
查看答案和解析>>
科目:高中化学 来源:2015届江苏省沭阳县高二下学期期中调研测试化学试卷(解析版) 题型:填空题
(10分)可逆反应aA(g) + bB(g) cC(g) + dD(g) ,反应时间与C%(产物C的体积分数)函数关系如图所示。A图表示的是温度不同的曲线,B图表示压强不同的曲线,C图表示使用催化剂和不使用催化剂时的反应曲线。
cC(g) + dD(g) ,反应时间与C%(产物C的体积分数)函数关系如图所示。A图表示的是温度不同的曲线,B图表示压强不同的曲线,C图表示使用催化剂和不使用催化剂时的反应曲线。

试比较下列大小关系:T1 T2, P1 P2, ΔH 0,ΔS 0。 使用催化剂的是 反应线。
查看答案和解析>>
科目:高中化学 来源:2015届江苏省沭阳县高二下学期期中调研测试化学试卷(解析版) 题型:选择题
化学与科学、技术、社会和环境密切相关。下列有关说法中错误的是
A.对废旧电池进行回收处理,主要是为了环境保护和变废为宝
B.用电解水的方法制取大量H2,可以缓解能源不足的问题
C.大力开发和应用氢能源有利于实现“低碳经济”
D.工业上,不能采用电解MgCl2溶液的方法制取金属镁
查看答案和解析>>
科目:高中化学 来源:2015届江苏省无锡江阴市高二下学期期中考试化学试卷(解析版) 题型:选择题
可逆反应mA(g)+nB(g) pC(g)+qD(g)的v-t图象如下右图,如若其它条件不变,只是在反应前加入合适的催化剂,则其v-t图象如下右图:①a1>a2 ②a1<a2 ③b1>b2 ④b1<b2 ⑤t1>t2 ⑥t1=t2 ⑦两图中阴影部分面积相等 ⑧右图中阴影部分面积更大,以上说法中正确的是
pC(g)+qD(g)的v-t图象如下右图,如若其它条件不变,只是在反应前加入合适的催化剂,则其v-t图象如下右图:①a1>a2 ②a1<a2 ③b1>b2 ④b1<b2 ⑤t1>t2 ⑥t1=t2 ⑦两图中阴影部分面积相等 ⑧右图中阴影部分面积更大,以上说法中正确的是
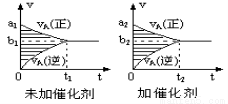
A.②③⑤⑧ B. ①④⑥⑧ C. ②④⑤⑦ D. ①③⑥⑦
查看答案和解析>>
科目:高中化学 来源:2015届江苏省无锡江阴市高二下学期期中考试化学试卷(解析版) 题型:选择题
下列热化学方程式正确的是
A.S(s)+O2(g)= SO2(g);ΔH= -269.8kJ/mol
B.NaOH (aq)+HCl(aq)=NaCl(aq)+H2O(l);ΔH=+57.3kJ/mol
C.表示乙醇的燃烧热:C2H5OH(l)+3O2(g)=2CO2(g)+ 3H2O(g);ΔH=-1367.0 kJ/mol
D.2NO2 = O2+2NO;ΔH= +116.2kJ/mol
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高二下学期4月阶段测试化学试卷(解析版) 题型:填空题
碘在科研与生活中有重要应用,某兴趣小组用0.50 mol·L-1 KI、0.2%淀粉溶液、0.20 mol·L-1 K2S2O8、0.10 mol·L-1 Na2S2O3等试剂,探究反应条件对化学反应速率的影响。
已知:S2O82-+2I- 2SO42-+I2(慢) I2+2S2O32-
2SO42-+I2(慢) I2+2S2O32- 2I-+ S4O62-(快)
2I-+ S4O62-(快)
向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的 耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色,S2O32-与S2O82-初始的物质的量需满足的关系为:n(S2O32-)∶n(S2O82-) 。
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
实验序号 | 体积V/mL | ||||
K2S2O8溶液 | 水 | KI溶液 | Na2S2O3溶液 | 淀粉溶液 | |
① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
② | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
③ | 8.0 | Vx | 4.0 | 4.0 | 2.0 |
表中Vx mL,理由是 。
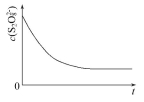
(3)已知某条件下,浓度c(S2O82-)反应时间t的变化曲线如图所示,若保持其他条件不变,请在答题卡坐标图中,分别画出降低反应温度和加入催化剂时c(S2O82-)-t的变化曲线示意图(进行相应的标注)
碘也可用作心脏起搏器电源-锂碘电池的材料,该电池反应为: 2Li(s)+I2(s) 2LiI(s)ΔH
2LiI(s)ΔH
已知: ①4Li(s)+O2(g) 2Li2O(s) ΔH1 ②4LiI(s)+O2(g)
2Li2O(s) ΔH1 ②4LiI(s)+O2(g) 2I2(s)+2Li2O(s)ΔH2
2I2(s)+2Li2O(s)ΔH2
则电池反应的ΔH= ;碘电极作为该电池的 极。
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高二下学期4月阶段测试化学试卷(解析版) 题型:选择题
H2S水溶液中存在电离平衡H2S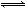 H++HS-和HS-
H++HS-和HS-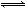 H++S2-。若向H2S溶液中
H++S2-。若向H2S溶液中
A.滴加新制氯水,溶液pH减小 B.通入过量SO2气体,溶液pH增大
C.加水,溶液中氢离子浓度增大 D.加入少量硫酸铜固体,所有离子浓度都减小
查看答案和解析>>
科目:高中化学 来源:2015届江苏省南京市高三9月学情调研卷化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是()
A.1.0 mol·L-1KNO3溶液:H+、Fe2+、SCN-、SO42-
B.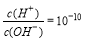 的溶液:K+、Ba2+、NO3-、Cl-
的溶液:K+、Ba2+、NO3-、Cl-
C.pH=0的溶液:Al3+、Cl-、SO42-、CO32-
D.c(ClO-) = 1.0 mol·L-1的溶液:Na+、I-、S2-、SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com