
【题目】从石油和煤中可以提炼出化工原料A和B,A是一种果实催熟剂,它的产量用来 衡量一个国家的石油化工发展水平。B是一种比水轻的油状液体,仅由碳氢两种元素组成,碳元素与氢元素的质量比为12:1,B的相对分子质量为78。回答下列问题:
(1)A的结构简式:________;
(2)A使溴的四氯化碳溶液褪色的化学反应方程式:___________;
(3)在碘水中加入B振荡静置后的现象:_______________,该操作叫______________;
(4)B与浓硫酸和浓硝酸在50~60℃反应的化学反应方程式:_________;
反应类型为:_________________;
(5)等质量的A、B完全燃烧时消耗O2的物质的量________(填“A>B”、“A<B”或“A=B”)。
【答案】 CH2=CH2 CH2=CH2+Br2→CH2Br-CH2Br 下层无色,上层紫红色 萃取 ![]() +HO-NO2
+HO-NO2![]()
![]() + H2O 取代反应(或硝化) A>B
+ H2O 取代反应(或硝化) A>B
【解析】A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平,则A为乙烯,B是一种比水轻的油状液体,B仅由碳氢两种元素组成,碳元素与氢元素的质量比为12:1,则原子个数之比为1:1,最简式为CH,B的相对分子质量为78,设B的分子式为(CH)n,则(12+1)n=78,解得n=6,所以分子式为C6H6,故B为苯。
(1)A为乙烯,其结构简式为:CH2=CH2;
答案为:CH2=CH2;
(2)乙烯使溴的四氯化碳溶液褪色发生加成反应,该反应为CH2=CH2+Br2→CH2Br-CH2Br;
答案为:CH2=CH2+Br2→CH2Br-CH2Br ;
(3)碘水中加入苯发生萃取,苯的密度比水的小,则苯在上层,观察到下层无色,上层紫红色;该操作叫萃取,
答案为:下层无色,上层紫红色;萃取;
(4)B与浓H2SO4与浓HNO3在50-60℃反应的化学反应方程![]() +HO-NO2
+HO-NO2![]()
![]() + H2O ,属于取代反应,也是硝化反应;
+ H2O ,属于取代反应,也是硝化反应;
答案为:![]() +HO-NO2
+HO-NO2![]()
![]() + H2O ;取代反应(或硝化);
+ H2O ;取代反应(或硝化);
(5)乙烯中H元素质量分数比苯中H元素质量分数大,故相同质量的乙烯、苯燃烧,乙烯消耗的氧气更多,即等质量的A、B完全燃烧时消耗O2的物质的量A>B,
故答案为:A>B。


科目:高中化学 来源: 题型:
【题目】已知:P4(s)+6Cl2(g)=4PCl3(g)△H=akJ/mol、P4(s)+10Cl2(g)=4PCl5(g)△H=bkJ/mol。P4具有正四面体结构,PCl5中P-Cl键的键能为ckJ/mol,PCl3中P-Cl键的键能为1.2ckJ/mol,下列叙述正确的是
A. P-P键的键能大于P-Cl键的键能
B. PCl3比PCl5更稳定
C. Cl-Cl键的键能![]() kJ/mol
kJ/mol
D. P-P键的键能为![]() kJ/mol
kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 25℃时部分弱电解质的电离平衡常数数据如表:
化学式 | HSCN | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.3×10﹣1 | 1.8×10﹣5 | Ka1=4.3×10﹣1Ka2=5.6×10﹣1 | 3.0×10﹣8 |
回答下列问题:
(1)写出碳酸的主要的电离方程式 . 若将碳酸饱和溶液稀释 10 倍,则稀释后的溶液中 c(H+)原来的十分之一(填“大于”、“小于”或“等于”).
(2)物质的量浓度均为 0.1mol/L 的五种溶液:pH 由小到大的顺序为(用编号填写).
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3 e.NaSCN
(3)25℃时,将 20mL0.1molL﹣1CH COOH 溶液和 20mL0.1molL﹣1HSCN 溶液分别与 20mL0.1molL﹣1NaHCO 溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图.
反应初始阶段两种溶液产生 CO2气体的速率存在明显差异的原因是反应结束后,假设 NaHCO3完全反应且气体全部逸出,则所得两溶液中,c(CH3COO)c(SCN)(填“>”、“<”或“=”)
(4)25℃时,CH3COONa 与 CH3COOH 的混合溶液,若测得 pH=8,则溶液中c(Na+)﹣c(CH3COO﹣)=mol/L(填代入数据后的计算式,不必算出具体数值).
(5)向 NaClO 溶液中通入少量的 CO2 , 发生反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取镁,可按如下步骤进行:
①把贝壳制成石灰乳
②在引入的海水中加入石灰乳,沉降、过滤,洗涤沉淀物
③将沉淀物与盐酸反应,结晶过滤,干燥产物
④冶炼③的产物得到金属Mg
关于提取镁,下列说法不正确的是
A. 此法的优点之一是原料来源丰富
B. 进行①②③步骤的目的是从海水中提取MgCl2
C. 用③的产物冶炼金属Mg,可以用热还原法(还原剂C、CO、H2)
D. 以上提取镁的过程中涉及的反应有分解反应、化合反应和复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A、D同主族,C与E同主族,D、E、F同周期,A、B的最外层电子数之和与C的最外层电子数相等, A能分别与B、C形成电子总数相等的分子,且A与C形成的化合物常温下为液态,A能分别与E、F形成电子总数相等的气体分子。请回答下列问题:
(1)F的元素符号为_________,E、F的简单离子中半径较大的是______(填离子符号)。
(2)A、C、D三种元素组成的一种常见化合物,是氯碱工业的重要产品,该化合物电子式为__________。
(3)B、C简单氢化物中稳定性较强的是__________(填分子式)。
(4)B与F两种元素形成的一种化合物分子,各原子均达8电子稳定结构,则该化合物的化学式为___________;B的简单氢化物与F的单质常温下可发生置换反应,请写出该反应的化学方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】抗过敏药物H 可通过如下合成路线制备。

已知: ![]()
(1)A物质的名称为_______________,B中含氧官能团的名称为__________________。
(2)由B生成C的反应类型为________________,由E 生成F 的反应类型为_______________。
(3)下列试剂可用于鉴别![]() 和
和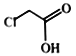 的有________(填标号)。
的有________(填标号)。
a.NaOH 溶液 b.小苏打溶液 c.AgNO3溶液 d.溴的CCl4溶液
(4)由D生成E的化学方程式为____________________________________。
(5)己知联苯由两个苯环通过单键连接而成(![]() ),分子中苯环间的单键可以自由旋转。则B的同分异构体中含联苯基团且能发生银镜反应的至少有____种。
),分子中苯环间的单键可以自由旋转。则B的同分异构体中含联苯基团且能发生银镜反应的至少有____种。
(6)M(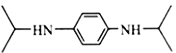 )是制备合成染料、颜料的重要中间产物。参照上面合成路线,请以丙酮(
)是制备合成染料、颜料的重要中间产物。参照上面合成路线,请以丙酮(![]() )和对苯二胺(
)和对苯二胺(![]() )为主要有机原料设计M的合成路线________________(其它试剂任选)。
)为主要有机原料设计M的合成路线________________(其它试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法中正确的是

A. ①②中Mg作负极、③④中Fe作负极
B. ②中A1作负极,电极反应式为2A1-6e-=2Al3+
C. ③中Fe作负极,电极反应式为Fe-2e-=Fe2+
D. ④中Cu作正极,电极反应式为O2+4e-+2H2O=4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图,电解总反应:2Cu+H2O ![]() Cu2O+H2↑.下列说法正确的是( )
Cu2O+H2↑.下列说法正确的是( ) 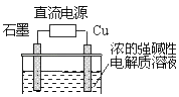
A.石墨电极上产生氧气
B.铜电极发生还原反应
C.铜电极接直流电源的正极
D.当有0.1mol电子转移时,有0.1molCu2O生成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com