
【题目】Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图,电解总反应:2Cu+H2O ![]() Cu2O+H2↑.下列说法正确的是( )
Cu2O+H2↑.下列说法正确的是( ) 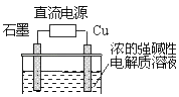
A.石墨电极上产生氧气
B.铜电极发生还原反应
C.铜电极接直流电源的正极
D.当有0.1mol电子转移时,有0.1molCu2O生成
【答案】C
【解析】解:A、电解总反应:2Cu+H2O ![]() Cu2O+H2↑,金属铜失电子,说明金属铜一定作阳极,石墨做阴极,在阴极上是溶液中的氢离子得电子,产生氢气,故A错误;
Cu2O+H2↑,金属铜失电子,说明金属铜一定作阳极,石墨做阴极,在阴极上是溶液中的氢离子得电子,产生氢气,故A错误;
B、铜电极本身失电子,发生氧化反应,故B错误;
C、铜电极是电解池的阳极,接直流电源的正极,故C正确;
D、反应2Cu+H2O═Cu2O+H2↑失电子物质的量为2mol,生成氧化亚铜1mol,所以当有0.1mol电子转移时,有0.05molCu2O生成,故D错误.
故选C.
根据电解总反应为2Cu+H2O ![]() Cu2O+H2↑可以知道金属铜为阳极材料,在阳极发生失电子的氧化反应,在阴极上是氢离子发生的电子的还原反应,根据电极反应计算生成的Cu2O.
Cu2O+H2↑可以知道金属铜为阳极材料,在阳极发生失电子的氧化反应,在阴极上是氢离子发生的电子的还原反应,根据电极反应计算生成的Cu2O.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】从石油和煤中可以提炼出化工原料A和B,A是一种果实催熟剂,它的产量用来 衡量一个国家的石油化工发展水平。B是一种比水轻的油状液体,仅由碳氢两种元素组成,碳元素与氢元素的质量比为12:1,B的相对分子质量为78。回答下列问题:
(1)A的结构简式:________;
(2)A使溴的四氯化碳溶液褪色的化学反应方程式:___________;
(3)在碘水中加入B振荡静置后的现象:_______________,该操作叫______________;
(4)B与浓硫酸和浓硝酸在50~60℃反应的化学反应方程式:_________;
反应类型为:_________________;
(5)等质量的A、B完全燃烧时消耗O2的物质的量________(填“A>B”、“A<B”或“A=B”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.摩尔是国际单位制的七个基本物理量之一
B.物质的量是表示数量的单位
C.摩尔是物质的量的单位,符号为mol
D.1mol任何物质都含有约6.02×1023个原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室验证钠能与二氧化碳发生反应,并确定其产物的装置如图所示(已知:PdC12溶液遇CO能产生黑色的Pd),下列说法错误的是

A. 装置①的仪器还可以制取H2、NH3等气体
B. 装置⑤中石灰水变浑浊后,再点燃酒精灯
C. 装置②③中分别盛装饱和Na2CO3溶液、浓H2SO4
D. 装置⑥中有黑色沉淀,发生的反应是PdC12+CO+H2O=Pd↓+CO2+2HC1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个固定容积的密闭容器中充入2molNO2 , 一定温度下建立如下平衡:2NO2![]() N2O4 , 此时平衡混合气中NO2的体积分数为x%,若再充入1mol N2O4 , 在温度不变的情况下,达到新的平衡时,测得NO2的体积分数为y%,则x和y的大小关系正确的是( )
N2O4 , 此时平衡混合气中NO2的体积分数为x%,若再充入1mol N2O4 , 在温度不变的情况下,达到新的平衡时,测得NO2的体积分数为y%,则x和y的大小关系正确的是( )
A.x>y
B.x<y
C.x=y
D.不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用化学用语表示NH3+HCl=NH4Cl中的相关微粒,其中不正确的是
A. 中子数为8的氮原子:![]() B. 氯化铵的电子式:
B. 氯化铵的电子式: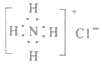
C. HCl的结构式:H-Cl D. 氯原子的结构示意图: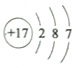
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中某区域的一些元素多用于制造半导体材料,它们是( )
A.左、下方区域的金属元素
B.金属元素和非金属分界线附近的元素
C.右、上方区域的非金属元素
D.稀有气体元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2SO2(g)+O2(g)2SO3(g)△H<0.某温度下,将2mol SO2和1mol O2置于10L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示.则下列说法正确的是( ) 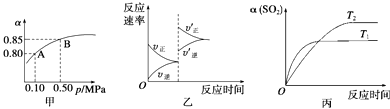
A.由图甲知,A点SO2的平衡浓度为0.4 mol/L
B.由图甲知,B点SO2、O2、SO3的平衡浓度之比为2:1:2
C.达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示
D.压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是人类最理想的能源。已知在25℃、101 kPa下,1 g 氢气完全燃烧生成液态水时放出热量142.9 kJ,则下列热化学方程式书写正确的是( )
A.2H2+O2=2H2O ΔH=-142.9 kJ·mol-1
B.2H2(g)+O2(g)=2H2O(l)ΔH=-142.9 kJ·mol-1
C.2H2(g)+O2(g)=2H2O(l)ΔH=-571.6 kJ·mol-1
D.2H2(g)+O2(g)=2H2O(l)ΔH=+571.6 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com