
【题目】在海水资源的综合利用中,不需要化学变化就能够从海水中获得的物质是
A. 溴、碘单质 B. 钠、镁单质 C. 食盐、淡水 D. 烧碱、纯碱
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】从下列实验事实所引出的相应结论正确的是 ( )
选项 | 实验事实 | 结论 |
A | 其他条件相同,Na2S2O3溶液浓度越大,析出硫沉淀所需时间越短 | 当其他条件不变时,增大反应物浓度化学反应速率加快 |
B | 在化学反应前后,催化剂的质量和化学性质都没有发生改变 | 催化剂一定不参与化学反应 |
C | 物质的量浓度相同的盐酸和醋酸分别与等质量的形状相同的锌粒反应 | 反应开始速率相同 |
D | 在容积可变的密闭容器中发生反应H2(g)+I2(g) | 正反应速率加快,逆反应速率不变 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热N2O5依次发生的分解反应为:
①N2O5(g) ![]() N2O3(g)+O2(g)
N2O3(g)+O2(g)
②N2O3(g) ![]() N2O(g)+O2(g)
N2O(g)+O2(g)
在容积为2 L的密闭容器中充入8 mol N2O5,加热到t ℃,达到平衡状态后O2为9 mol,N2O3为3.4 mol。则平衡体系中N2O5的物质的量浓度为
A. 1.8mol/L B. 0.9 mol/L C. 2.3 mol/L D. 4.0 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关碱金属元素,下列说法正确的是( )
A. 单质沸点随原子序数的递增而升高
B. 周期表第一列是第IA族元素,又称碱金属元素
C. 金属锂在空气中燃烧,产物是Li2O2
D. 金属锂常用于制造锂电池,这跟它还原性强、密度小有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是

A.温度: T1>T2>T3
B.正反应速率:υ(b)>υ(d) υ(a)>υ(c)
C.平衡常数:K(a)>K(c) K(b)=K(d)
D.平均摩尔质量: M(b)>M(d) M(a)<M(c)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解200mL的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.1mol碱式碳酸铜晶体(不含结晶水)后,恰好恢复到电解前的浓度(不考虑二氧化碳的溶解)。下列说法正确的是( )
A. 电解过程中转移的物质的量为0.2 mol B. 电解过程中共产生气体5.6L
C. 原溶液的物质的量浓度为1.0mol/L D. 电解过程中,阴极产物只有Cu单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y、Z原子序数之和是W的2倍,X、Z在周期表中的相对位置如图所示,X的最低负价绝对值与其原子最外层电子数相等。下列说法不正确的是

A. 原子半径:Y>Z>W B. 一定条件下,Y可置换出X
C. 气态氢化物稳定性:Z>W D. 熔点YW2>XW4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2013年9月以来,我国很多地区再大面积出现雾霾,特别是华中华北尤其严重,汽车尾气、燃煤废气和冬季取暖排放的CO2等都是形成雾霾的原因。
Ⅰ.用于净化汽车尾气的反应为:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)△H<0,在一定温度下,如图在一体积固定的密闭容器中充入一定量的NO和CO,在t1时刻达到平衡状态。
2CO2(g)+N2(g)△H<0,在一定温度下,如图在一体积固定的密闭容器中充入一定量的NO和CO,在t1时刻达到平衡状态。
(1)能判断该反应达到平衡状态的标志是_______。
A.在单位时间内生成1mol CO2的同时消耗了1mol CO
B.混合气体的密度不再改变
C.混合气体的平均相对分子质量不再改变
D.混合气体的压强不再变化
(2)在t2时刻将容器的容积迅速扩大到原来的2倍,在其他条件不变的情况下,t3时刻达到新的平衡状态,之后不再改变条件.请在图中补充画出从t2到t4时刻正反应速率随时间的变化曲线:___________

Ⅱ.使用石油热裂解的副产物CH4来制取H2,其生产流程如图1所示:
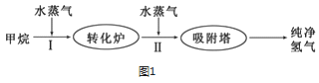
(3)此流程的第Ⅰ步反应为:CH4(g)+H2O(g)![]() CO(g)+3H2(g),一定条件下CH4的平均转化率与温度、压强的关系如图2所示,则P1_____P2(填“>”、“<”或“=”),100℃时,将1molCH4(g)和2molH2O(g)通入容积为100L的恒容的密闭容器中,达到平衡时CH4的转化率为0.5。此时该反应的平衡常数K____________ (写出完整的计算过程)
CO(g)+3H2(g),一定条件下CH4的平均转化率与温度、压强的关系如图2所示,则P1_____P2(填“>”、“<”或“=”),100℃时,将1molCH4(g)和2molH2O(g)通入容积为100L的恒容的密闭容器中,达到平衡时CH4的转化率为0.5。此时该反应的平衡常数K____________ (写出完整的计算过程)

(4)此流程的第Ⅱ步反应的平衡常数随温度的变化情况如下表
温度/℃ | 400 | 500 | 830 |
平衡常数K | 10 | 9 | 1 |
温度/℃ | 400 | 500 | 830 |
平衡常数K | 10 | 9 | 1 |
从表上可以推断该反应是___________(填“吸热”或“放热”)反应,若反应在500℃时进行,设CO(g)和H2O(g)的起始浓度均为0.020mol/L,在该条件下,反应达到平衡时,CO的转化率为________;
(5)图3表反应Ⅱ在t1时达到平衡,在t2时因改变某个条件引起浓度变化的情况,图中t2时改变的条件是降低温度或________________(写一种)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com