
【题目】一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是

A. 该反应的化学方程式为6A+2 D![]() 3B+4C
3B+4C
B. 反应进行到1 s时,v(A)=v(B)
C. 反应进行到5 s时,B的平均反应速率为0.06mol/(L·s)
D. 反应进行到5 s时,v(A)=v(B)=v(C)=v(D)
【答案】C
【解析】A.由图可知,反应达到平衡时A物质增加了1.2mol、D物质增加了0.4mol、B物质减少了0.6mol、C物质减小了0.8mol,所以A、D为生成物,物质的量之比为3:1,B、C为反应物,物质的量之比为3:4,反应方程式为:3B+4C![]() 6A+2D,故A错误;B.反应到1s时,v(A)═
6A+2D,故A错误;B.反应到1s时,v(A)═![]() =
=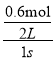 =0.3mol/(Ls),v(C)═
=0.3mol/(Ls),v(C)═![]() =
= =0.1mol/(Ls),所以v(A)≠v(C),故B错误;C.反应进行到5s时,v(B)=
=0.1mol/(Ls),所以v(A)≠v(C),故B错误;C.反应进行到5s时,v(B)= ![]() =
=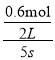 =0.06mol/(Ls),故C正确;D.反应进行到5s时,v(A)=
=0.06mol/(Ls),故C正确;D.反应进行到5s时,v(A)= ![]() =
=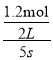 =0.12mol/(Ls),v(B)=
=0.12mol/(Ls),v(B)= ![]() =
=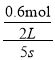 =0.06mol/(Ls),v(C)==
=0.06mol/(Ls),v(C)== ![]() =
=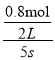 =0.08mol/(Ls),v(D)==
=0.08mol/(Ls),v(D)== ![]() =
=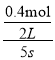 =0.04mol/(Ls),所以反应进行到5s时,各物质的反应速率不相等,故D错误;答案为C。
=0.04mol/(Ls),所以反应进行到5s时,各物质的反应速率不相等,故D错误;答案为C。


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】碳、硫的含量影响钢铁性能。某兴趣小组用如下流程对钢样进行探究。

(1)钢样中硫元素以FeS形式存在,FeS在足量氧气中灼烧,生成的固体产物中Fe、O两种元素的质量比为21:8,则该固体产物的化学式为_____________。
(2)检验钢样灼烧生成气体中的CO2,需要的试剂是____________ (填字母)。
a.酸性KMnO4溶液 b.澄清石灰水 c.饱和小苏打溶液 d.浓H2SO4
(3)取10.00 g钢样在足量氧气中充分灼烧,将生成的气体用足量1%的H2O2溶液充分吸收,再用0.1000 mol·L-1NaOH溶液滴定吸收液至终点,消耗NaOH溶液20.00mL;另取10.00g钢样在足量氧气中充分灼烧,将生成的气体通过盛有足量碱石灰的U型管(如下图),碱石灰增重0.614 g。

①用l%H2O2溶液吸收SO2,发生反应的离子方程式为___________________。
②分别计算该钢样中硫、碳元素的质量分数(写出计算过程)。
③实验测得的碳元素质量分数比真实值偏高,其可能的原因是______________(填字母)
a.U型管中生成的亚硫酸盐吸收了O2
b.碱石灰吸收了空气中的CO2
c.气体通过碱石灰的流速过快,末被充分吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】树脂交联程度决定了树脂的成膜性。下面是一种成膜性良好的醇酸型树脂的合成路线,如下图所示:

(1)合成A的化学方程式是__________。
(2)B的分子式为C4H7Br,且B不存在顺反异构,B的结构简式为_______,A到B步骤的反应类型是_________。
(3)E中含氧官能团的名称是______,D 的系统命名为_________。
(4)下列说法正确的是_______。
A.lmol化合物C最多消耗3molNaOH
B.lmol化合物E与足量银氨溶液反应产生2molAg
C. F不会与Cu(OH)2悬浊液反应
D.丁烷、1-丁醇、化合物D中沸点最高的是丁烷
(5)写出D、F在一定条件下生成醇酸型树脂的化学方程式__________。
(6) 的符合下列条件的同分异构体有_____种。
的符合下列条件的同分异构体有_____种。
① 苯的二取代衍生物;② 遇FeCl3溶液显紫色;③ 可发生消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用湿法炼锌产生的铜镉渣生产金属镉的流程如下:

已知:铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质。
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1 mol·L-1计算):
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 | Mn(OH)2 |
开始沉淀的pH | 1.5 | 6.5 | 7.2 | 8.2 |
沉淀完全的pH | 3.3 | 9.9 | 9.5 | 10.6 |
(1)为了提高铜镉渣浸出的速率,可采取的措施有:①适当升高温度;②搅拌;③______等。已知浸出的金属离子均为二价,写出浸出钴的化学方程式__________________。
(2)除钴的过程中,需要加入活化剂Sb2O3,锌粉会与Sb2O3、Co2+的溶液形成微电池并产生合金CoSb。该微电池的正极反应式为________________________________。
(3)除铁的过程分两步进行:
①先加入适量KMnO4,发生反应的离子方程式为______________________________,
②再加入ZnO控制反应液的pH范围为_____________。
(4)除铁过程第①步,若加入KMnO4时条件控制不当,MnO2会继续反应,造成的结果是______________,若加入的KMnO4不足量,则待电解溶液中有Fe元素残余。请设计实验方案加以验证_________________。
(5)净化后的溶液用惰性电极电解可获得镉单质。电解废液中可循环利用的溶质是____。
(6)处理含镉废水常用化学沉淀法,以下是几种镉的难溶化合物的溶度积常数(25℃):
Ksp(CdCO3)=5.210-12, Ksp(CdS)=3.610-29,Ksp(Cd(OH)2)=2.010-16,根据上述信息:
沉淀Cd2+效果最佳的试剂是____________。
a.Na2CO3 b.Na2S c.CaO
若采用生石灰处理含镉废水最佳pH为11,此时溶液中c(Cd2+)=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种气体,取X和Y按1∶1的物质的量之比混合,放入密闭容器中发生如下反应:X+2Y![]() 2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2,则Y的转化率最接近于( )
2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2,则Y的转化率最接近于( )
A. 33% B. 40% C. 50% D. 65%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表前4周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是 ( )

A.W、R元素单质分子内都存在非极性键
B.X、Z元素都能形成双原子分子
C.键长W—H<Y—H,键的极性Y—H>W—H
D.键长X—H<W—H,键能X—H<W—H
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是
A. 分子组成相差一个或几个-CH2—原子团的物质互为同系物,它们的化学性质肯定相似
B. 正丁烷中4个碳原子共直线
C. 甲烷是烷烃中碳含量最低的,也是组成最简单的烃
D. 分子式为C4H10的烃有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应C+CO2 ![]() 2CO,下列措施可使反应速率增大的是( )
2CO,下列措施可使反应速率增大的是( )
①升高温度 ②增加碳的量 ③恒温恒容下通入CO2
④恒温恒压下充入N2 ⑤恒温恒容充入N2 ⑥恒温恒容通入CO
A. ①③④ B. ②④⑥ C. ①③⑥ D. ③⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com