
【题目】NA为阿伏加德罗常数的值,下列说法正确的是
A. 1molHClO中所含H—Cl键的数目为NA
B. 8.8g乙酸乙酯中所含碳原子数为0.4NA
C. 1.2gC与0.1molCO2在高温下充分反应生成的CO分子数为0.1NA
D. 标准状况下,1L0.1mol·L-1HCl溶液中滴加氨水至pH=7,溶液中NH4+的数目为0.1NA
【答案】B
【解析】
A.HClO的结构式为H-O-Cl,不存在H-Cl键,故A错误;
B.乙酸乙酯的分子式为:C4H8O2,8.8g乙酸乙酯的物质的量为0.1mol,一个分子中含有4个碳原子,故碳原子数为0.4NA,故B正确;
C.C与CO2在高温下反应的方程式为:C+CO2![]() 2CO,1.2gC的物质的量为0.1mol,与0.1molCO2反应生成0.2mol的CO,即0.2NA,故C错误;
2CO,1.2gC的物质的量为0.1mol,与0.1molCO2反应生成0.2mol的CO,即0.2NA,故C错误;
D.常温时,pH=7为中性,标准状况下,pH=7为酸性,即c(H+)>c(OH-),根据溶液呈电中性,则c(Cl-)>c(NH4+),n(Cl-)=0.1mol,则NH4+的数目小于0.1NA,故D错误。
故选B。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是()
A. 摩尔是一个基本物理量
B. 1mol H2O中所含氧原子的质量为16g
C. 10L氢气比8L氢气所含H2的物质的量多
D. 某物质含有6.02×1023个粒子,则该物质的体积为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸钾和亚硫酸氢钾溶液能发生氧化还原反应:![]() 已知该反应的速率随
已知该反应的速率随![]() 的增大而加快
的增大而加快![]() 为
为![]() 的速率时间关系图。下列说法中正确的是
的速率时间关系图。下列说法中正确的是
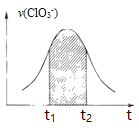
A. 反应开始时速率增大一定是温度升高所致
B. 纵坐标为![]() 的
的![]() 曲线与图中曲线不重合
曲线与图中曲线不重合
C. 图中阴影部分的面积表示![]() 时间内
时间内![]() 的减小
的减小
D. 后期反应速率下降的主要原因是反应物浓度减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数,下列叙述正确的是
A. NA的单位是摩尔
B. 标准状况下,22.4 L氦气所含的原子数为2NA
C. 1.7 g H2O2中含有的电子数为0.9 NA
D. 1 mol·L-1 NaCl溶液含有NA个Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如何降低大气中![]() 的含量及有效地开发利用
的含量及有效地开发利用![]() 引起了全世界的普遍重视。目前工业上有一种方法是用
引起了全世界的普遍重视。目前工业上有一种方法是用![]() 来生产燃料甲醇。为探究该反应原理,进行如下实验:在容积为1L的密闭容器中,充入
来生产燃料甲醇。为探究该反应原理,进行如下实验:在容积为1L的密闭容器中,充入![]() 和
和![]() ,在
,在![]() 下发生发应,
下发生发应,![]() 实验测得
实验测得![]() 和
和![]() 的物质的量浓度随时间变化如下所示:
的物质的量浓度随时间变化如下所示:
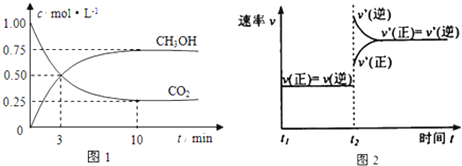
(1)从反应开始到平衡,氢气的平均反应速率![]() ______。500℃达平衡时,
______。500℃达平衡时,![]() 的体积分数为______,如上图是改变某条件时化学反应速率随时间变化的示意图,则该条件是______ 该反应的逆反应为______反应
的体积分数为______,如上图是改变某条件时化学反应速率随时间变化的示意图,则该条件是______ 该反应的逆反应为______反应![]() 填“放热”或“吸热”
填“放热”或“吸热”![]()
(2)500℃该反应的平衡常数为______![]() 保留两位小数
保留两位小数![]() ,若降低温度到300℃进行,达平衡时,K值______
,若降低温度到300℃进行,达平衡时,K值______![]() 填“增大”“减小”或“不变”
填“增大”“减小”或“不变”![]() .
.
(3)下列措施中能使![]() 的转化率增大的是______.
的转化率增大的是______.
A. 在原容器中再充入![]()
B. 在原容器中再充入![]() 和
和![]()
C. 在原容器中充入![]()
![]() 使用更有效的催化剂
使用更有效的催化剂
E. 将水蒸气从体系中分离出
(4)500℃条件下,改变起始反应物的用量,测得某时刻![]() 、
、![]() 、
、![]() 和
和![]() 的浓度均为
的浓度均为![]() ,则此时
,则此时![]() 正
正![]() ______
______![]() 逆
逆![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]()
(5)假定该反应是在恒容恒温条件下进行,判断该反应达到平衡的标志______.
A. 消耗![]() 同时生成1mol
同时生成1mol![]()
![]() 混合气体密度不变
混合气体密度不变
C. 混合气体平均相对分子质量不变
D.3v正(H2)=v逆(H2O)
E.![]() .不变
.不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】抗结肠炎药物Y结构如图所示,以下说法错误的是
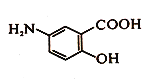
A. 该有机物既能和酸反应又能和碱反应
B. 1mol该有机物可以和2molNaOH发生反应
C. 该有机物可以发生缩聚反应
D. 该有机物不能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化氢毒性很大,俗称“一口闷”,工业废水中的硫化物在酸性条件下会以硫化氢的形式逸出。某课外小组以碘量法测定废水中的硫化物,实验装置如图所示,实验步骤及测定原理如下:

Ⅰ.取样、吹气、固硫
连接装置,打开氮气源,检查装置气密性。移取一定体积1mol·L-1乙酸锌溶液于两支吸收管中,取200mL水样于反应瓶中,通入氮气一段时间。移取10mL盐酸于反应瓶中,水浴加热,继续通入氮气。已知乙酸锌与硫化氢反应生成硫化锌沉淀(硫化氢被完全吸收)。
Ⅱ.滴定
关闭气源,往两个吸收管中各加入0.010mol·L-1的碘标准溶液100mL(过量),再加入盐酸5mL,静置。加入淀粉指示液,用0.010mol·L-1的硫代硫酸钠标准溶液对两支吸收管中的液体进行滴定。(已知:![]() )
)
回答下列问题:
(1)水浴加热的温度不能高于85℃,原因是_____________________________。
(2)加入碘标准溶液时,吸收管中发生反应的化学方程式为________________。
(3)该实验使用两个吸收管的原因是_____________________________,若只使用一个吸收管,会导致测定结果偏______________________(填“高”或“低”)。
(4)该200mL水样经吹气、固硫后,滴定操作时共消耗160mLNa2S2O3溶液,则废水中硫的含量为________mg·L-1。
(5)实验室常用FeS固体与酸反应制取H2S。实验室制取H2S时,从反应物与生成物的状态、性质和反应条件分析,下列发生装置中可选用的是________(填序号)。

(6)将二氧化氯溶液加入硫化氢溶液中,然后加入少量稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成。写出二氧化氯与硫化氢溶液反应的离子方程式:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 1molH2SO4的质量为98g·mol-1 B. H2SO4的摩尔质量为98g
C. 1molO2体积是22.4L D. 1molO2约有6.02×1023个分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:

(1)氢氧燃料电池能量转化的主要形式是____________________________________________,在导线中电子流动方向为________(用a、b表示)。
(2)负极反应式为________________________________________________________________。
(3)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H2===2LiH Ⅱ.LiH+H2O===LiOH+H2↑
①反应Ⅰ中的还原剂是________,反应Ⅱ中的氧化剂是________。
②金属锂吸收的氢气与放出的氢气的物质的量之比为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com