
| A. | CH3CH2COOCH=CH2 | B. | CH3CH2COOCH2CH2CH3 | ||
| C. | CH2=CHCH2COOCH2CH2CH=CH2 | D. | CH3CH2CH2COOCH2CH(CH3)2 |
分析 设酯的化学式为CxHyOz,酯完全燃烧生成等物质的量的CO2和水,则分子中H原子数目是C原子数目的2倍,属于饱和一元酯,酯X水解可得酸甲和醇乙,醇氧化后可得酸丙,且甲和丙是同分异构体,则形成该酯的羧酸与醇具有相同的C原子数目,据此分析判断.
解答 解:A.CH3CH2COOCH=CH2中H原子数目不是C原子的2倍,属于不饱和一元酯,不符合题意,故A不选;
B.CH3CH2COOCH2CH2CH3中H原子数目是C原子的2倍,形成该酯的羧酸为CH3CH2COOH,和CH3CH2COH,CH3CH2COH氧化生成CH3CH2COH,与题意不符合,故B不选;
C.CH2=CHCH2COOCH2CH2CH=CH2中H原子数目不是C原子的2倍,属于不饱和一元酯,不符合题意,故C不选;
D.CH3CH2CH2COOCH2CH(CH3)2中H原子数目是C原子的2倍,形成该酯的羧酸为CH3CH2CH2COOH、醇为HOCH2CH(CH3)2,HOCH2CH(CH3)2氧化生成(CH3)2CHCOOH,与CH3CH2CH2COOH互为同分异构体,符合题意,故D选;
故选:D.
点评 本题考查有机物的推断、同分异构体、酯及醇等性质与转化,难度中等,根据题目确定酯的结构特点,利用代入法进行验证.


科目:高中化学 来源: 题型:解答题
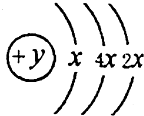 A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图如图,B、C可形成离子化合物B2C或B2C2,据此填空:
A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图如图,B、C可形成离子化合物B2C或B2C2,据此填空:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、Na+、NO3-、Cl- | B. | K+、Ba2+、Cl-、NO3- | ||
| C. | HCO3-、Ca2+、Na+、NO3- | D. | Cu2+、Cl-、K+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由于碘在酒精中的溶解度大,所以可用酒精将碘水中的碘萃取出来 | |
| B. | 水的沸点是100℃,酒精的沸点是78.5℃,所以可用直接加热蒸馏法使含水酒精变为无水酒精 | |
| C. | 苯甲酸中含有少量氯化钠,可用重结晶的方法提纯得到苯甲酸 | |
| D. | 乙炔气体中混有少量硫化氢气体,可以通过足量溴水洗气除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
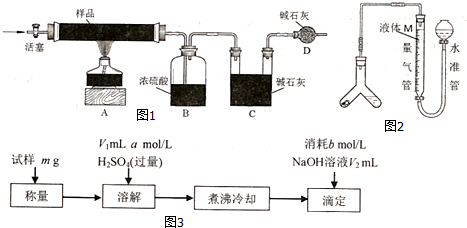
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+ H+ SO42- | B. | H+ Ag+ NO3- | C. | K+ HCO3-Cl- | D. | Na+ NO3- Fe2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com