
【题目】砷化稼(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)基态Ga原子的核外电子排布式为[Ar]_______________。
(2)根据元素周期律,元素的电负性Ga______(填“大于”或“小于”, 下同)As,第一电离能B ____ Ga;BF3和NH3的分子能够通过配位键相结合的原因是_______。
(3)杀虫剂Na3AsO4中阴离子的空问构型为______,As原子采取________杂化。
(4)组成相似的GaF3和GaCl3晶体,前者属于离子晶体,后者属于分子晶体。从F-和Cl-结构的不同分析其原因是____________。
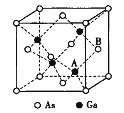
(5)原子晶体GaAs的晶胞参数a=xpm,它的晶胞结构如下图所示。该晶胞内部存在的共价健数为______;A原子距离B原子所在六面体的侧面的最短距离为______ (用x表示)pm ;该晶胞的密度为_____g·cm-3。(阿伏伽德罗常数用NA表示)。
【答案】 3d104s24p1 小于 大于 NH3的N具有孤对电子,BF3中的B核外具有空轨道 正四面体 sp3 Cl-的电子层数比F-的多,原子半径比F-的大 16 0.25x ![]()
【解析】(1)镓是31号元素,核外有31个电子,基态镓(Ga)原子的电子排布式为1s22s22p63s23p63d104s24p1,简写成[Ar] 3d104s24p1;(2)同周期元素,从左到右电负性逐渐增大,同主族元素从下到上,电负性逐渐增大,电负性:Ga小于As;第一电离能与原子核外电子排布有关,当电子在能量相当的轨道上形成全空、半满、全满时,原子的能量较低,第一电离能越大,同一主族,从上到下,原子半径越大,吸电子能力越弱,第一电离能越小,B与Ga在ⅢA族,第一电离能B大于Ga;B原子其价层电子数是4,采取sp3杂化,B原子形成3个σ 键一个配位键,B原子提供空轨道的原子、N原子提供孤电子对,B、N原子之间形成配位键,形成BF3·NH3。(3)AsO43-中含有的孤电子对数是0,中心原子有4个共价键,所以其构型是正四面体形,As原子价层电子对数为4,故杂化方式为 sp3 ;(4) Cl-的电子层数比F-的多,原子半径比F-的大,Ca2+ 与F― 形成离子键,形成离子晶体;(5)如图每个As与4个Ga形成4个共价键,晶胞中共含4×4=16个共价键;A原子距离B原子所在六面体的侧面的最短距离为a/4=0.25xpm;晶胞中拥有的As原子8×1/8+6×1/2=4,Ga也是4个,该晶胞的密度为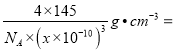
![]() g·cm-3
g·cm-3


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】依照阿伏加德罗定律,下列叙述正确的是
A. 同温同压下两种气体的体积之比等于摩尔质量之比
B. 同温同压下两种气体的物质的量之比等于密度反比
C. 同温同压下两种气体的摩尔质量之比等于密度反比
D. 同温同体积下两种气体的物质的量之比等于压强之比
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备1,2-二溴乙烷的反应原理如下:
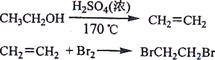
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l 40℃脱水生成乙醚。
用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如下图所示:

有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | 一l30 | 9 | -1l6 |
回答下列问题:
(1)在此制各实验中,要尽可能迅速地把反应温度提高170℃左右,其最主要目的是 ;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入 ,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是 ;
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在 层(填“上”、“下”);
(5)若产物中有少量未反应的Br2,最好用 洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚.可用 的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝基苯可在金属锡、盐酸作用下生成氯化苯铵盐(![]() )、氯化亚锡(SnCl2)和水。
)、氯化亚锡(SnCl2)和水。
(1)己知锡位于第五周期,与C同主族,写出Sn2+的最外层电子排布式_______;Cl-中有___个填充电子的能级。
(2)画出硝基的电子式______,氯化亚锡分子的空间构型是________;氯化苯胺盐(![]() )中N原子的杂化方式为_____,该盐的水溶度较苯胺大的原因是___________。
)中N原子的杂化方式为_____,该盐的水溶度较苯胺大的原因是___________。
(3)在上述反应中的各物质涉及的微粒间作用力有_______。
A、共价键 B、金属键 C、离子键 D、配位键 E、氢键 F、范德华力
(4)Sn的一种同素异形体——灰锡的晶体结构类似金刚石,立方晶胞结构如图所示,则锡的配位数是_______。
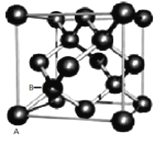
(5)假设锡原子(如图中A、B两原子)在体对角线上外切,晶胞参数为a,计算灰锡的空间利用率约为________。(百分数表示,取两位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值.下列说法正确的是( )
A. l04g苯乙烯(C6H5-CH=CH2)中含有8NA的碳氢键和4NA的碳碳双键
B. 在50g质量分数为46%的乙醇水溶液中,含有氢原子数为3NA
C. lmol有机物CH3-CH=CH-CH2-CH3中最多有9NA个原子在同一平面上
D. 80℃ 时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2SO2+O2![]() 2SO3达到平衡的标志是( )
2SO3达到平衡的标志是( )
①消耗2molSO2的同时生成2molSO3
②SO2、O2与SO3的物质的量之比为2∶1∶2
③反应混合物中,SO3的质量分数不再改变
④恒容条件下压强保持不变
⑤一定体积下气体的密度保持不变
⑥v正(SO2)=2v逆(O2)
A.①②⑤ B.①③④ C.③④ D③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据研究,若把太阳光变成激光用于分解海水制氢,反应可表示为:![]() 。有下列几种说法:① 水分解反应是放热反应;② 氢气是可再生能源;③ 使用氢气作燃料有助于控制温室效应;④ 若用生成的氢气与空气中多余的二氧化碳反应生成甲醇储存起来,可改善生存条件。其中叙述正确的是( )
。有下列几种说法:① 水分解反应是放热反应;② 氢气是可再生能源;③ 使用氢气作燃料有助于控制温室效应;④ 若用生成的氢气与空气中多余的二氧化碳反应生成甲醇储存起来,可改善生存条件。其中叙述正确的是( )
A.①② B.③④ C.②③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)反应3A(g)+B(g) ===2C(g)在三种不同的条件下进行反应,在同一时间内,测得的反应速率用不同的物质表示为①vA=1 mol/(L·min)、②vC=0.5 mol/(L·min)、③vB=0.5 mol/(L·min),三种情况下该反应速率由大到小的关系是 。(用序号表示)
(2)某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
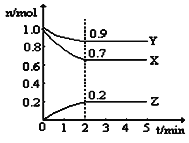
①该反应的化学方程式为____________________________。
②反应开始至2min,以气体Z表示的平均反应速率为 。
③2min反应达平衡容器内混合气体的平均相对分子质量比起 始时 (填“大”,“小”或“相等”下同),混合气体密度比起始时 。
④上述反应,在第2min时,X的转化率为 。
⑤将a mol X与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n (X) = n (Y) = n (Z),则原混合气体中a : b =__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的叙述不正确的是
A.淀粉水解可以制得葡萄糖
B.碘酒可使细菌、病毒的蛋白质变性而死亡
C.氨基酸是两性化合物,能与酸或碱反应生成盐
D. 光导纤维遇盐酸和氢氧化钠溶液都不会被损坏
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com