
【题目】(1)反应3A(g)+B(g) ===2C(g)在三种不同的条件下进行反应,在同一时间内,测得的反应速率用不同的物质表示为①vA=1 mol/(L·min)、②vC=0.5 mol/(L·min)、③vB=0.5 mol/(L·min),三种情况下该反应速率由大到小的关系是 。(用序号表示)
(2)某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
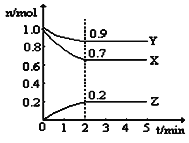
①该反应的化学方程式为____________________________。
②反应开始至2min,以气体Z表示的平均反应速率为 。
③2min反应达平衡容器内混合气体的平均相对分子质量比起 始时 (填“大”,“小”或“相等”下同),混合气体密度比起始时 。
④上述反应,在第2min时,X的转化率为 。
⑤将a mol X与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n (X) = n (Y) = n (Z),则原混合气体中a : b =__________。
【答案】(1)③>①>②(2)①3X+Y![]() 2Z ② 0.02 mol·L-1·min-1 ③大;相等④30% ⑤5:3
2Z ② 0.02 mol·L-1·min-1 ③大;相等④30% ⑤5:3
【解析】
试题分析:(1)比较反应速率时,应用同种物质表示不同条件下的反应速率,再进行比较,比如,可以用反应物B表示反应速率:①vB=![]() mol/(L·min)、②vB=0.25 mol/(L·min)、③vB=0.5 mol/(L·min),因此反应速率由大到小的关系为:③>①>②;
mol/(L·min)、②vB=0.25 mol/(L·min)、③vB=0.5 mol/(L·min),因此反应速率由大到小的关系为:③>①>②;
(2)①化学计量数之比等于各物质的转化量之比,即化学计量数之比为:0.3: 0.1:0.2=3: 1:2,即化学方程式为:3X+Y![]() 2Z;②反应开始至2min,气体Z生成0.2mol,用Z表示的平均反应速率为:
2Z;②反应开始至2min,气体Z生成0.2mol,用Z表示的平均反应速率为: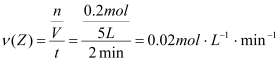 ;③2min反应达平衡容器内混合气体的平均相对分子质量比起开始时大,由于混合气体的质量自始至终不变,而在固体容积中发生反应,因此混合气体的密度比起始时不变;④在第2min时,X的转化率为:
;③2min反应达平衡容器内混合气体的平均相对分子质量比起开始时大,由于混合气体的质量自始至终不变,而在固体容积中发生反应,因此混合气体的密度比起始时不变;④在第2min时,X的转化率为:![]() ;
;
⑤设Y的变化量为x,则:
3X+Y![]() 2Z
2Z
起始(mol) a b 0
转化(mol) 3x x 2x
某时刻(mol) a-3x b-x 2x
由于n (X) = n (Y) = n (Z),则a-3x= b-x=2x,则a=5x,b=3x,故a:b=5:3。


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:
【题目】由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如右图转化关系(部分生成物和反应条件略去)

下列推断不正确的是( )
A. 若X是Na2CO3,C为含极性键的非极性分子,则A一定是氯气,且D和E不反应
B. 若A是单质,B和D的反应是OH-+HCO3-=H2O+CO32-,E一定能还原Fe2O3
C. 若D为CO,C能和E反应,则A一定为Na2O2,其电子式是![]()
D. 若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷化稼(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)基态Ga原子的核外电子排布式为[Ar]_______________。
(2)根据元素周期律,元素的电负性Ga______(填“大于”或“小于”, 下同)As,第一电离能B ____ Ga;BF3和NH3的分子能够通过配位键相结合的原因是_______。
(3)杀虫剂Na3AsO4中阴离子的空问构型为______,As原子采取________杂化。
(4)组成相似的GaF3和GaCl3晶体,前者属于离子晶体,后者属于分子晶体。从F-和Cl-结构的不同分析其原因是____________。
(5)原子晶体GaAs的晶胞参数a=xpm,它的晶胞结构如下图所示。该晶胞内部存在的共价健数为______;A原子距离B原子所在六面体的侧面的最短距离为______ (用x表示)pm ;该晶胞的密度为_____g·cm-3。(阿伏伽德罗常数用NA表示)。
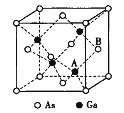
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,PbO2与Cr3+反应,产物是Cr2O72-和Pb2+,则与1.0mol Cr3+反应所需PbO2的物质的量为( )
A. 3.0mol B. 2.5mol C. 1.5mol D. 0.75mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中需要0.2molL﹣1的CuSO4溶液950mL,配制时应选用的容量瓶的规格和称取胆矾晶体(CuSO45H2O式量为250)的质量分别是( )
A.1000mL 50.0g
B.950mL 47.5g
C.950mL 30.4g
D.1000mL 32.0g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去下列物质中的杂质(括号中为杂质),采用的试剂和除杂方法错误的是( )
序号 | 待除杂质 | 试剂 | 除杂方法 |
A | C2H4(SO2) | NaOH溶液 | 洗气 |
B | C6H6(Br2) | Fe粉 | 蒸馏 |
C | C6H5NO2(NO2) | NaOH | 分液 |
D | C2H2(H2S) | CuSO4 | 洗气 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器,800℃时发生如下反应:
2CuO(s)+CO(g)![]() Cu2O(s)+CO2(g),n(CuO)随时间的变化如表:
Cu2O(s)+CO2(g),n(CuO)随时间的变化如表:
时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
n(CuO)(mol) | 0.080 | 0.060 | 0.040 | 0.020 | 0.020 | 0.020 |
(1)写出该反应的平衡常数表达式 。
已知:K(400℃)>K(350℃),则该反应是 热反应。
(2)右图中表示Cu2O的物质的量随时间变化的曲线是 (选填“A”或“B”),800℃时,0~3min内该反应的平均速率v (CO2)= 。
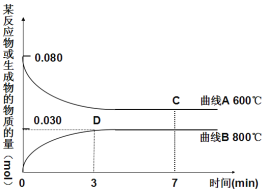
(3) 能说明该反应已达到平衡状态的是 。
a.v(CO)=v(CO2) b.容器内压强保持不变
c.v逆(CO)=v正(CO2) d.容器内气体的密度保持不变
(4)能使该反应的正反应速率增大,且平衡向正反应方向移动的是 。
A.增加CuO的量
B.适当升高温度
C.及时移去CO2
D.增大CO的浓度
E.选择高效催化剂
F.增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应2A(s)+3B(g)![]() C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是( )
C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是( )
①增加A的量,平衡向正反应方向移动; ②升温,平衡向逆反应方向移动,v(正)减小;③压强增大一倍,平衡不移动,v(正)、v(逆)不变; ④增大B的浓度,v(正)>v(逆);⑤加入催化剂,B的转化率提高
A. ①② B. ④ C. ③ D. ④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 发生化学反应时失去电子越多的金属原子,还原能力越强
B. NaCl只有在水溶液中才能电离出Na+、Cl-
C. 能与酸反应的氧化物,不一定是碱性氧化物
D. 电离时能产生H+的化合物是酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com