
【题目】如图所示的转化关系中,已知A是由短周期元素组成的酸式盐.D、Y、H为气体,X为无色液体,G和K均是常见的强酸.H与Na2O2可发生化合反应,生成的盐与Ba2+反应可生成不溶于稀G的白色沉淀,一个D分子中含有10个电子.试回答下列问题: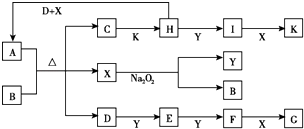
(1)写出D(少量)、H、X反应生成A的离子反应方程式: .
(2)写出D与Y反应生成E的化学方程式: .
(3)写出D与K反应生成的正盐溶液中的离子浓度大小关系: .
(4)已知:2H(g)+Y(g)2I(g)△H=﹣196.6 kJmol﹣1 . 当加入4mol H和2mol Y后,放出345 kJ的热量时,H的转化率最接近于(填字母).
A.40%
B.50%
C.80%
D.90%
【答案】
(1)NH3+SO2+H2O=NH4++HSO3﹣
(2)4NH3+5O2 ![]() 4NO+6H2O
4NO+6H2O
(3)c(NH4+)>c(SO42﹣)>c(H+)>c(OH﹣)
(4)D
【解析】解:X为无色液体,与过氧化钠反应得到B与气体Y,则X是H2O,Y是O2 , B是NaOH.A能与氢氧化钠反应生成气体D,且D为10电子分子,可判断A为铵盐,D为NH3;C与强酸K反应,生成气体H,且H能与Na2O2发生化合反应,可判断H具有还原性,H的氧化产物能与Ba2+生成难溶于酸的沉淀,可知该沉淀是BaSO4 , 据此逐步推出,A为NH4HSO3 , C为Na2SO3 , H为SO2 , I为SO3 , K为硫酸;由D到G的转化过程可判断,E为NO,F为NO2 , G为HNO3 . (1)亚硫酸属于二元酸,NH3少量时生成酸式盐,反应离子方程式为:NH3+SO2+H2O=NH4++HSO3﹣ , 所以答案是:NH3+SO2+H2O=NH4++HSO3﹣;(2)NH3在催化剂存在下可被O2氧化为NO,这是工业生成硝酸的基础,反应方程式为:4NH3+5O2 ![]() 4NO+6H2O,所以答案是:4NH3+5O2
4NO+6H2O,所以答案是:4NH3+5O2 ![]() 4NO+6H2O;(3)NH3与硫酸反应生成(NH4)2SO4 , 铵根离子部分水解使溶液呈酸性,故溶液中的离子浓度关系为:c(NH4+)>c(SO42﹣)>c(H+)>c(OH﹣),所以答案是:c(NH4+)>c(SO42﹣)>c(H+)>c(OH﹣);(4)根据热化学反应方程式可知,4 mol SO2与2 mol O2完全反应放出的热量为:196 kJ×2=392 kJ,实际放出的热量为345 kJ,故SO2的转化率为:345 kJ/392 kJ=0.88,故选:D.
4NO+6H2O;(3)NH3与硫酸反应生成(NH4)2SO4 , 铵根离子部分水解使溶液呈酸性,故溶液中的离子浓度关系为:c(NH4+)>c(SO42﹣)>c(H+)>c(OH﹣),所以答案是:c(NH4+)>c(SO42﹣)>c(H+)>c(OH﹣);(4)根据热化学反应方程式可知,4 mol SO2与2 mol O2完全反应放出的热量为:196 kJ×2=392 kJ,实际放出的热量为345 kJ,故SO2的转化率为:345 kJ/392 kJ=0.88,故选:D.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】已知:Fe2O3(s)+ ![]() C(s)═
C(s)═ ![]() CO2(g)+2Fe(s)△H=+234.1kJ/mol
CO2(g)+2Fe(s)△H=+234.1kJ/mol
C(s)+O2(g)═CO2(g)△H=﹣393.5kJ/mol
则:2Fe(s)+ ![]() O2(g)═Fe2O3(s)的△H是( )
O2(g)═Fe2O3(s)的△H是( )
A.﹣824.4 kJ/mol
B.﹣627.6 kJ/mol
C.﹣744.7 kJ/mol
D.﹣169.4 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 碳酸钙的摩尔质量是100g
B. 摩尔既是微粒数目的单位,也是物质的量的单位
C. 阿伏加德罗常数的符号为NA,约为6.02×1023mol-1
D. 标准状况下,1mol任何物质的体积均为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石墨烯[如图(a)所示]是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯[如图(b)所示]. 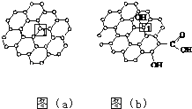
(1)图(a)中,1号C与相邻C形成σ键的个数为 .
(2)图(b)中,1号C的杂化方式是 , 该C与相邻C形成的键角(填“>”“<”或“=”)图(a)中1号C与相邻C形成的键角.
(3)若将图(b)所示的氧化石墨烯分散在H2O中,则氧化石墨烯中可与H2O形成氢键的原子有(填元素符号).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3.6g碳在一定量的氧气中燃烧,反应后生成的混合气体相对氢气的密度是16,则生成的一氧化碳的质量是(相对密度指在相同的温度和压强下物质的密度之比)
A. 3.3 g B. 6.3 g C. 8.4 g D. 13.2 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度时,将1mol A和2mol B放入容积为5L的某密闭容器中发生如下反应:A(s)+2B(g)C(g)+2D(g),经5min后,测得容器内B物质的浓度减少了0.2molL﹣1 . 下列叙述不正确的是( )
A.在5min内该反应用C的浓度变化表示的反应速率为0.02molL﹣1min﹣1
B.在5min时,容器内D的浓度为0.2molL﹣1
C.该反应随着反应的进行,容器内压强逐渐增大
D.5min时容器内气体总的物质的量为3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,在溶液中能大量共存,加入H2SO4溶液后既有气体放出又有沉淀生成的一组是( )
A.Ba2+、NO ![]() 、NH
、NH ![]() 、Cl﹣
、Cl﹣
B.Ba2+、HCO ![]() 、NH
、NH ![]() 、NO
、NO ![]()
C.K+、Cu2+、Cl﹣、OH﹣
D.Na+、CO ![]() 、SO
、SO ![]() 、K+
、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种常见的短周期元素其原子半径随原子序数的变化如下图。
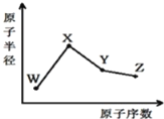
已知W一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期中最强。下列说法正确的是 ( )
A. 对应的气态氢化物的稳定性:Y>Z
B. X的非金属性是同周期中最强的
C. 对应简单离子的半径:X>W
D. Y的氧化物能与X的最高价氧化物对应的水化物反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学方程式或离子方程式正确的是( )
A. H2S在过量的O2中燃烧:2H2S+O2 ![]() 2H2O+2S
2H2O+2S
B. 向稀HNO3中加入过量的铁:Fe + 4H+ + NO3— == Fe3+ + NO↑ + 2H2O
C. 向氯化铝溶液滴加过量的氨水:Al3+ + 3NH3·H2O == Al(OH) 3↓+ 3NH4+
D. 向稀NH4HSO3溶液中滴加少量的稀NaOH溶液:NH4+ + OH-= NH3·H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com