
【题目】下列分子中,各分子的立体构型和中心原子的杂化方式均正确的是( )
A. NH3 平面三角形 sp3杂化 B. CCl4 正四面体 sp3杂化
C. H2O V形 sp2杂化 D. CO32﹣ 三角锥形 sp3杂化
【答案】B
【解析】
根据价层电子对互斥理论确定分子空间构型及中心原子杂化方式,价层电子对数=配原子个数+孤电子对数。
A、NH3中心原子的价层电子对数=3+![]() (5-3×1)=4,N的杂化方式为sp3,含有一对孤电子对,分子的立体构型为三角锥形,选项A错误;
(5-3×1)=4,N的杂化方式为sp3,含有一对孤电子对,分子的立体构型为三角锥形,选项A错误;
B、CCl4中心原子的价层电子对数=4+![]() (4-4×1)=4,C的杂化方式为sp3,没有孤电子对,分子的立体构型为正四面体,选项B正确;
(4-4×1)=4,C的杂化方式为sp3,没有孤电子对,分子的立体构型为正四面体,选项B正确;
C、H2O中心原子的价层电子对数=2+![]() (6-2×1)=4,O的杂化方式为sp3,含有两对孤电子对,分子的立体构型为V形,选项C错误;
(6-2×1)=4,O的杂化方式为sp3,含有两对孤电子对,分子的立体构型为V形,选项C错误;
D、CO32- 中心原子的价层电子对数=3+![]() (4+2-3×2)=3,C的杂化方式为sp2,没有孤电子对,分子的立体构型为平面三角形,选项D错误;
(4+2-3×2)=3,C的杂化方式为sp2,没有孤电子对,分子的立体构型为平面三角形,选项D错误;
答案选B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】过氧化氢H2O2(氧的化合价为﹣1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列A~D涉及H2O2的反应,填写空白:
A.Na2O2+2HCl===2NaCl+H2O2
B.Ag2O+H2O2===2Ag+O2+H2O
C.2H2O2===2H2O+O2
D.3H2O2+Cr2(SO4)3+10KOH===2K2CrO4+3K2SO4+8H2O
(1)H2O2仅体现氧化性的反应是_________(填代号)。
(2)H2O2既体现氧化性又体现还原性的反应是_________(填代号)。
(3)在稀硫酸中,KMnO4和H2O2能发生氧化还原反应。
氧化反应:H2O2﹣2e﹣===2H++O2↑
还原反应:MnO![]() +5e﹣+8H+===Mn2++4H2O
+5e﹣+8H+===Mn2++4H2O
写出该氧化还原反应的离子方程式:___________________。
(4)在K2Cr2O7+14HCl===2KCl+3Cl2↑+7H2O+2CrCl3的反应中,有0.3 mol电子转移时生成Cl2的体积为______(标准状况),被氧化的HCl的物质的量为____。
(5)除去镁粉中混入的铝粉杂质用溶解、_______方法,化学反应方程式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物的同分异构体数目判断正确的是( )
A. C5H10共有6种单烯烃同分异构体B. 1-甲基环己烷(![]() )共有4种一氯代物
)共有4种一氯代物
C. C6H14共有5种同分异构体D. CH2Cl2共有两种同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备1,2-二溴乙烷的实验流程如下:
![]()
已知:①主要副反应:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。
②有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
溶解性 | 易溶于水 | 难溶于水 | 难溶于水 |
沸点/℃ | 78.5 | 132 | 34.6 |
试回答下列问题:
(1)乙醇与浓硫酸l70℃发生反应的化学方程式:______________________。
(2)乙醇与浓硫酸反应装置中放入几片碎瓷片,目的是_________________________。
(3)反应得到的混合气体中含有SO2、CO2等气体,检验其中的SO2气体可选用的试剂是_______________________________。
(4)吸收步骤中,应适当降低吸收液的温度,其主要目的是______________。
(5)实验制得的1,2-二溴乙烷粗产品中含有少量未反应的Br2和少量副产品乙醚,某同学进一步提纯如下:
序号 | 实验方案 | 实验目的或结论 |
① | 除去粗产品中少量未反应的Br2,实验方法是_________________ | 除去溴杂质 |
② | 除去粗产品中的乙醚的实验方法是将①实验后的有机混合物进行________________________ | 除去乙醚杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A(C2H4)是基本的有机化工原料。用A和常见的有机物可合成一种醚类香料和一种缩醛类香料。具体合成路线如图所示(部分反应条件略去):
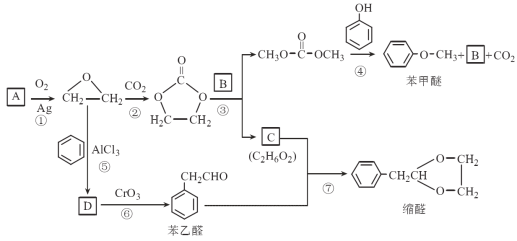
已知以下信息:
①![]()
②D为单取代芳香族化合物且能与金属钠反应;每个D分子中只含有1个氧原子,D中氧元素的质量分数约为13.1%。
回答下列问题:
(1)A的名称是______,图中苯甲醚的分子式是________。
(2)B的结构简式为____________________,D中含有的官能团名称是________。
(3)②的反应类型是____________________。
(4)⑦的化学方程式为__________________________________________________。
(5)请写出满足下列条件的苯乙醛的所有同分异构体的结构简式:含有苯环和![]() 结构,核磁共振氢谱有4组峰,峰面积之比为3∶2∶2∶1。____________
结构,核磁共振氢谱有4组峰,峰面积之比为3∶2∶2∶1。____________
(6)参照 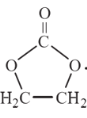 的合成路线,设计一条由2-氯丙烷和必要的无机试剂制备
的合成路线,设计一条由2-氯丙烷和必要的无机试剂制备 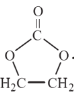 的合成路线____________(注明必要的反应条件)。合成路线流程图示例如下:CH3CH2OH
的合成路线____________(注明必要的反应条件)。合成路线流程图示例如下:CH3CH2OH![]() CH2=CH2
CH2=CH2![]() BrCH2-CH2Br
BrCH2-CH2Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对有机物 说法正确的是
说法正确的是
A. 1mol该物质所含原子数为![]()
B. 该物质系统命名为2,3-二甲基-5-乙基己烷
C. 该物质一个分子中最多10个碳原子共平面
D. 该物质为某炔烃加氢后的产物,则可能的炔烃的结构只有一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应![]() ,在容积固定的密闭容器中达到平衡状态的标志是( )
,在容积固定的密闭容器中达到平衡状态的标志是( )
①单位时间内生成![]() 的同时生成
的同时生成![]()
②单位时间内生成![]() 的同时生成
的同时生成![]()
③用![]() 表示的反应速率之比为
表示的反应速率之比为![]() 的状态
的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的物质的量不再改变的状态
A.①④⑥⑦B.②③⑤⑦C.①③④⑤D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2O、NO和NO2等氮氧化物是空气污染物含有氮氧化物的尾气需处理后才能排放。
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为___。
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为__。
①下列措施不能提高尾气中NO和NO2去除率的有____ (填字母代号)
A.采用气、液逆流的方式吸收尾气
B.加快通入尾气的速率
C.吸收尾气过程中定补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是____(填化学式),吸收后排放的尾气中含量较高的氮氧化物是____(填化学式)。
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同, NO的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
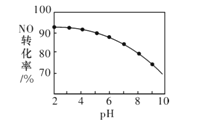
①在酸NaClO性溶液中,HC1O氧化NO生成Cl和NO3-,其离子方程式为3HClO+2NO+H2O=3C1-+2NO3-+5H+
②NaClO溶液的初始pH越小,NO转化率越高,其原因是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组欲开展一次以化学为主题的活动,确定的课题是“研究浓硫酸与木炭粉在加热条件下反应的产物”。根据小组成员的推测,浓硫酸与木炭粉在加热条件下反应的产物可能有CO2、SO2,为了验证推测,小组讨论用以下装置进行实验:
编号 | a | b | c |
装置 |
品红 酸性KMnO4 品红 溶液 溶液 溶液 A B C |
|
|
请回答:
⑴ 实验时可观察装置a中A瓶溶液褪色,C瓶溶液不褪色。则A瓶溶液的作用___,C瓶溶液的作用_____;
⑵ 装置b中所加的液体是________,装置b可验证的产物是________;
⑶ 甲、乙两位同学分别设计了两套不同装置。甲的装置顺序:c→b→a,乙的装置顺序:c→a→b。你认为合理的是(填“甲”或“乙”)__;
⑷写出装置c中发生的化学方程式: __________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com