
【题目】I、三氧化二镍(Ni2O3)是一种灰黑色无气味有光泽的块状物,易碎成细粉末,常用于制造高能电池。工业上以金属镍废料生产NiCl2,继而生产Ni2O3的工艺流程如下:

下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Ni(OH)2 |
开始沉淀的pH | 1.1 | 6.5 | 3.5 | 7.1 |
沉淀完全的pH | 3.2 | 9.7 | 4.7 | 9.2 |
(1)①为了提高金属镍废料浸出的速率,在“酸浸”时可采取的措施有:适当升高温度,搅拌,______等。
②酸浸后的酸性溶液中含有Ni2+、Cl-,另含有少量Fe2+、Fe3+、Al3+等。在沉镍前,需加Na2CO3控制溶液pH范围为______。
(2)“氧化”生成Ni2O3的离子方程式为______。
(3)工业上用镍为阳极,电解0.05 ~ 0.1 mol·L-1 NiCl2 溶液与一定量NH4Cl组成的混合溶液,可得到高纯度、球形的超细镍粉。当其它条件一定时,NH4Cl的浓度对阴极电流效率及镍的成粉率的影响如下图所示,则NH4Cl的浓度最好控制为______。

II、煤制天然气的工艺流程简图如下:

(4)已知反应I:C(s)+H2O(g)![]() CO(g)+H2(g) ΔH=+135 kJ·mol-1,通入的氧气会与部分碳发生燃烧反应。请利用能量转化及平衡移动原理说明通入氧气的作用:______。
CO(g)+H2(g) ΔH=+135 kJ·mol-1,通入的氧气会与部分碳发生燃烧反应。请利用能量转化及平衡移动原理说明通入氧气的作用:______。
(5)①甲烷化反应IV发生之前需要进行脱酸反应III。煤经反应I和II后的气体中含有两种酸性气体,分别是H2S和_____。
②工业上常用热碳酸钾溶液脱除H2S气体得到两种酸式盐,该反应的离子方程式是____。
(6)一定条件下,向体积为2L的恒容密闭容器中充入1.2 mol CH4(g)和4.8 mol CO2(g),发生反应:CH4 (g)+3CO2 (g)![]() 2H2O(g)+4CO(g) ΔH>0。实验测得,反应吸收的能量和甲烷的体积分数随时间变化的曲线图像如右图。计算该条件下,此反应的
2H2O(g)+4CO(g) ΔH>0。实验测得,反应吸收的能量和甲烷的体积分数随时间变化的曲线图像如右图。计算该条件下,此反应的![]() H=______。
H=______。

【答案】 增大盐酸的浓度(或将镍废料研成粉末等) 4.7≤pH<7.1 2Ni2++ClO-+4OH-=== Ni2O3↓+Cl-+2H2O 10 g·L-1 氧气与碳发生燃烧反应放热,放出的热被可逆反应吸收利用,促进反应正向移动 CO2 CO32-+H2S![]() HS-+HCO3- +330 kJ·mol-
HS-+HCO3- +330 kJ·mol-
【解析】试题分析:I、(1)①根据影响反应速率的因素回答;②根据相关金属离子开始生成氢氧化物沉淀和完全生成沉淀的pH,要让Fe2+、Fe3+、Al3+等沉淀而Ni2+不生成沉淀,需要将Fe2+氧化为Fe3+,再调节PH。(2)根据得失电子守恒配平次氯酸钠氧化Ni2+的离子方程式;(3)NH4Cl的浓度最好控制在镍的成粉率最高点;II、(4)C(s)+H2O(g)![]() CO(g)+H2(g)反应吸热,氧气会与部分碳发生燃烧反应放热;(5)①根据元素守恒,煤经反应I和II后的气体中含有两种酸性气体,分别是H2S和CO2;②热碳酸钾溶液与H2S气体得到两种酸式盐是碳酸氢钠和硫氢化钠;(6)根据图像可知,吸收118.8 kJ能量时CH4的体积分数为
CO(g)+H2(g)反应吸热,氧气会与部分碳发生燃烧反应放热;(5)①根据元素守恒,煤经反应I和II后的气体中含有两种酸性气体,分别是H2S和CO2;②热碳酸钾溶液与H2S气体得到两种酸式盐是碳酸氢钠和硫氢化钠;(6)根据图像可知,吸收118.8 kJ能量时CH4的体积分数为![]() ,利用“三段式”计算消耗甲烷的物质的量。
,利用“三段式”计算消耗甲烷的物质的量。
解析:I、(1)(1)①为了提高金属镍废料浸出的速率,可采取的措施有:适当升高温度,搅拌,增大盐酸的浓度等;②要让Fe2+、Fe3+、Al3+等沉淀而Ni2+不生成沉淀,需要将Fe2+氧化为Fe3+,再调节PH,使Fe3+、Al3+等完全沉淀PH≥4.7,Ni2+不生成沉淀PH<7.1,所以控制PH的范围是4.7≤pH<7.1。(2)根据得失电子守恒配平次氯酸钠氧化Ni2+的离子方程式是2Ni2++ClO-+4OH-=== Ni2O3↓+Cl-+2H2O;(3)NH4Cl的浓度最好控制在镍的成粉率最高点,所以NH4Cl的浓度最好控制在10 g·L-1;II、(4)C(s)+H2O(g)![]() CO(g)+H2(g)反应吸热,氧气会与部分碳发生燃烧反应放热,氧气与碳发生燃烧放出的热被C(s)+H2O(g)
CO(g)+H2(g)反应吸热,氧气会与部分碳发生燃烧反应放热,氧气与碳发生燃烧放出的热被C(s)+H2O(g)![]() CO(g)+H2(g)吸收利用,促进反应正向移动;(5)①根据元素守恒,煤经反应I和II后的气体中含有两种酸性气体,分别是H2S和CO2;②热碳酸钾溶液与H2S气体得到两种酸式盐是碳酸氢钠和硫氢化钠,反应离子方程式是CO32-+H2S
CO(g)+H2(g)吸收利用,促进反应正向移动;(5)①根据元素守恒,煤经反应I和II后的气体中含有两种酸性气体,分别是H2S和CO2;②热碳酸钾溶液与H2S气体得到两种酸式盐是碳酸氢钠和硫氢化钠,反应离子方程式是CO32-+H2S![]() HS-+HCO3-;
HS-+HCO3-;
(6)设参加反应的甲烷的物质的量为xmol;
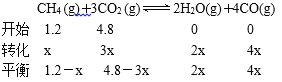
![]()
x=0.36mol
根据图像可知,0.36mol甲烷参加反应吸收118.8 kJ能量,则1mol甲烷反应吸收热量118.8 kJ÷0.36=330 kJ,所以此反应的![]() H=+330 kJ·mol-1。
H=+330 kJ·mol-1。


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是 ( )

A. 正极反应中有CO2生成
B. 微生物促进了反应中电子的转移
C. 质子通过交换膜从负极区移向正极区
D. 电池总反应为C6H12O6+6O2===6CO2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在溶液中能大量共存的是
A. Mg2+、K+、OH- B. Ba2+、Na+、SO42-
C. K+、HCO3-、OH- D. K+、Cu2+、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下表中烃的分子式排列规律,判断空格中的烃的同分异构体数目( )
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
CH4 | C2H4 | C3H8 | C4H8 | C6H12 | C7H16 | C8H16 |
A.2
B.3
C.4
D.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据氧化还原反应:2Ag+(aq)+Cu(s)===Cu2+(aq)+2Ag(s)设计的原电池如图所示。

请回答下列问题:
(1)电极X的材料是_____________;电解质溶液Y是_______________。
(2)银电极为电池的______极,发生的电极反应式为_______________________;X电极上发生的电极反应为_______________________________________。
(3)盐桥中______(选填“阳离子”或“阴离子”)向硫酸铜溶液方向移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能被视为21世纪最具发展潜力的清洁能源,其开发利用是科学家们研究的重要课题。试回答下列问题:
(1)与化石燃料相比,氢气作为燃料的优点是______(答出两点)。
(2)与氢气直接燃烧相比较,设计成镍氢电池可以大大提高能量的转换率,在镍氢电池充电过程中储氢合金(M)吸氢转化为MH2,总反应为:xNi(OH)2+M![]() xNiOOH+MHx,试写出放电过程中负极反应式______。
xNiOOH+MHx,试写出放电过程中负极反应式______。
(3)施莱辛(Sehlesinger)等人提出可用NaBH4与水反应制氢气:BH4-+2H2O == BO2-+4H2↑,已知NaBH4与水反应后所得溶液显碱性,溶液中各离子浓度大小关系为______,用离子方程式表示溶液显碱性的原因______。
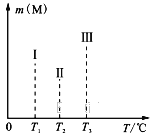
(4)在容积均为V L的Ⅰ、Ⅱ、Ⅲ三个相同密闭容器中,分别放入a g的储氢合金(M)和b mol H2发生如下反应:2M(s)+xH2(g)![]() 2MHx(s) ΔH<0。三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下,实验测得反应均进行到1min时M的质量如下图所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是______。当三个容器反应都达到化学平衡时,H2转化率最大的反应温度是____。
2MHx(s) ΔH<0。三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下,实验测得反应均进行到1min时M的质量如下图所示,此时Ⅰ、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是______。当三个容器反应都达到化学平衡时,H2转化率最大的反应温度是____。
(5)储氢还可以借助有机物,如利用乙苯与苯乙烯之间的可逆反应来实现脱氢和加氢:![]() 。维持体系总压恒定,在温度T时,物质的量为n、体积为V的乙苯蒸气发生催化脱氢。已知乙苯的平衡转化率为α,则在该温度下反应的平衡常数K=_____(用α等符号表示)。
。维持体系总压恒定,在温度T时,物质的量为n、体积为V的乙苯蒸气发生催化脱氢。已知乙苯的平衡转化率为α,则在该温度下反应的平衡常数K=_____(用α等符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列九种物质:①H2 ②铝 ③CuO ④CO2⑤H2SO4 ⑥Ba(OH)2固体⑦氨水 ⑧稀硝酸 ⑨熔融Al2(SO4)3
(1)上述状态下可导电的是;
属于电解质的是;
属于非电解质的是 .
(2)上述九种物质中有两种物质之间可发生离子反应:H++OH﹣═H2O,该离子反应对应的化学方程式为 .
(3)⑨在水中的电离方程式为 , 34.2g ⑨溶于水配成250mL溶液,SO42﹣的物质的量浓度为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为除去括号内杂质,下列有关试剂和操作方法不正确的是( )
A.苯(苯酚):稀NaOH溶液,分液
B.乙醇(乙酸):KOH溶液,分液
C.乙烷(乙烯):溴水,洗气
D.苯(溴):稀NaOH溶液,分液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com