
【题目】下列离子方程式不正确的是
A.硫酸铝溶液中加入氢氧化钡溶液:Ba2++![]() == BaSO4↓
== BaSO4↓
B.硫酸亚铁溶液中加入过氧化氢溶液:2Fe2+ + H2O2 + 2H+ == 2Fe3+ + 2H2O
C.向NaHCO3 溶液中加入NaOH溶液:![]() + OH-==
+ OH-==![]() + H2O
+ H2O
D.向AgCl悬浊液中加入Na2S溶液:2AgCl + S2-== Ag2S + 2Cl-
【答案】A
【解析】
A.硫酸铝溶液中加入氢氧化钡溶液时,除生成BaSO4沉淀,Al3+与OH-也能发生离子反应,其中滴加适量氢氧化钡溶液至SO42-恰好完全沉淀时发生的离子反应方程式为3Ba2++6OH-+2Al3++3SO42-=3BaSO4↓+2Al(OH)3↓,故A错误;
B.硫酸亚铁溶液中加入过氧化氢溶液时发生的离子反应方程式为2Fe2+ + H2O2 + 2H+ == 2Fe3+ + 2H2O,故B正确;
C.向NaHCO3 溶液中加入NaOH溶液时发生的离子反应方程式为![]() + OH-==
+ OH-==![]() + H2O,故C正确;
+ H2O,故C正确;
D.向AgCl悬浊液中加入Na2S溶液发生沉淀转化时的离子反应方程式为2AgCl + S2-== Ag2S + 2Cl-,故D正确;
故答案为A。


科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
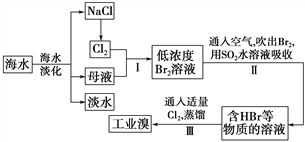
(1)请列举海水淡化的两种方法:________、________。
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是_________。
(3)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为_______,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是_______。
(4)某化学研究性学习小组为了了解从工业溴中提纯溴的方法,查阅了有关资料知:Br2的沸点为59 ℃,微溶于水,有毒并有强腐蚀性。他们参观生产过程后,画了如下装置简图:
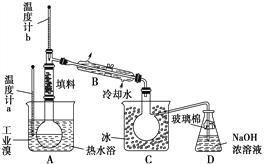
请你参与分析讨论:
①图中仪器B的名称是____________。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是__________。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件?___________。
④C中液体颜色为________________。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油加氢精制和天然气净化等过程产生有毒的H2S,直接排放会污染空气。
(1)工业上用克劳斯工艺处理含H2S的尾气获得硫黄,流程如下:
![]()
①反应炉中的反应:2H2S(g)+3O2(g) =2SO2(g)+2H2O(g) H=-1035.6 kJ·mol1
催化转化器中的反应:2H2S(g)+SO2(g) = 3S(g)+2H2O(g) H=-92.8 kJ·mol1
克劳斯工艺中获得气态硫黄的总反应的热化学方程式:______。
②为了提高H2S转化为S的比例,理论上应控制反应炉中H2S的转化率为______。
(2)科研工作者利用微波法处理尾气中的H2S并回收H2和S,反应为:H2S![]() H2+S,一定条件下,H2S的转化率随温度变化的曲线如图。
H2+S,一定条件下,H2S的转化率随温度变化的曲线如图。
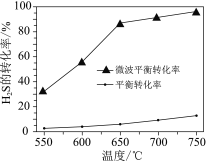
①H2S分解生成H2和S的反应为______反应(填“吸热”或“放热”)。
②微波的作用是______。
(3)某科研小组将微电池技术用于去除天然气中的H2S,装置示意图如下,主要反应:2Fe+2H2S+O2= 2FeS+2H2O(FeS难溶于水),室温时,pH=7的条件下,研究反应时间对H2S的去除率的影响。

①装置中微电池负极的电极反应式:______。
②一段时间后,单位时间内H2S的去除率降低,可能的原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将10 mL充满NO2和O2的混合气体的试管,倒置在水槽中,反应停止后试管内剩余2 mL的无色气体,求原混合气体中NO2和O2各多少毫升____________?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的数值,下列叙述正确的是
A. 78g苯中含有的碳碳双键的数目为3NA
B. 16gCu2S和CuO组成的混合物中含有的阳离子数为0.2NA
C. 将1mol H2与 1 mol I2充入一密闭容器中充分反应后,转移的电子书为2NA
D. 1 mol Fe 与足量的浓硫酸共热反应,生成SO2的分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,适合进行现场酒精检测,下列说法不正确的是
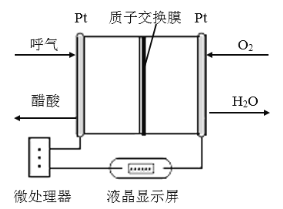
A.电流由O2所在的铂电极经外电路流向另一电极
B.该电池的正极反应式为:O2 + 4e- + 4H+=2H2O
C.该电池的负极反应式为:CH3CH2OH + 3H2O-12e-=2CO2↑ + 12H+
D.微处理器通过检测电流大小而计算出被测气体中酒精的含量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中浓度关系正确的是
A.小苏打溶液中:c(Na+)+c(H+)=c(![]() )+c(
)+c(![]() )+c(OH-)
)+c(OH-)
B.CH3COONa溶液中:c(CH3COO-) > c(Na+) > c(OH-) > c(H+)
C.0.1 mol/L的NaHA溶液,其pH=4,则c(HA-)>c(H+)>c(H2A)>c(A2-)
D.物质的量浓度相等的CH3COOH溶液和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中相关物质的信息都正确的一项是( )
选项 | 化学式 | 电子式或含有的化学键类型 | 物质的性质 | 与性质相对应的用途 |
A |
|
| 不稳定,易分解 | 医用消毒剂 |
B |
| 离子键、共价键 | 强氧化性 | 消毒液 |
C |
| 共价键 | 水溶液呈弱碱性 | 工业制硝酸 |
D |
| 离子键 | 受热易分解 | 泡沫灭火器 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂对工业生产钛白粉产生的废液进行综合利用,废液中含有大量FeSO4、H2SO4和少量Fe2(SO4)3,可用于生产颜料铁红和补血剂乳酸亚铁。其生产工艺流程如图:
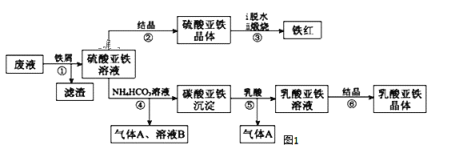
已知:乳酸可以和碳酸根生成二氧化碳气体。请回答:
(1)步骤④需控制反应温度低于35℃,其目的是___。
(2)步骤④反应的离子方程式是___。
(3)已知:FeCO3(s) Fe2+(aq)+CO32-(aq),试用平衡移动原理解释步骤⑤生成乳酸亚铁的原因___。
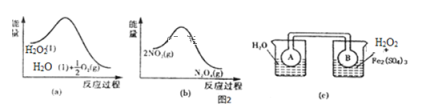
(4)Fe3+对H2O2的分解具有催化作用。利用如图(a)和(b)中的信息,按图(c)装置(连通的A、B瓶中已充有NO2气体)进行实验。可观察到B瓶中气体颜色比A瓶中的___(填“深”或“浅”),其原因是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com