
【题目】下列溶液中浓度关系正确的是
A.小苏打溶液中:c(Na+)+c(H+)=c(![]() )+c(
)+c(![]() )+c(OH-)
)+c(OH-)
B.CH3COONa溶液中:c(CH3COO-) > c(Na+) > c(OH-) > c(H+)
C.0.1 mol/L的NaHA溶液,其pH=4,则c(HA-)>c(H+)>c(H2A)>c(A2-)
D.物质的量浓度相等的CH3COOH溶液和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH)
【答案】D
【解析】
A.小苏打溶液中存在的电荷守恒式为c(Na+)+c(H+)=c(![]() )+2c(
)+2c(![]() )+c(OH-),故A错误;
)+c(OH-),故A错误;
B.CH3COONa溶液显碱性,则c(OH-) > c(H+),溶液中存在的电荷守恒式为c(CH3COO-) +c(OH-) = c(Na+) + c(H+),则c(Na+) > c(CH3COO-),即溶液中:c(Na+) >c(CH3COO-) > c(OH-) > c(H+),故B错误;
C.0.1 mol/L的NaHA溶液,其pH=4,说明HA-的电离程度大于HA-的水解程度,则c(A2-) > c(H2A),即c(HA-)>c(H+) >c(A2-)>c(H2A),故C错误;
D.物质的量浓度相等的CH3COOH溶液和CH3COONa溶液等体积混合后,溶液中存在的电荷守恒式为c(CH3COO-)+c(OH-)=c(H+)+c(Na+),物料守恒式为2c(Na+)= c(CH3COO-)+c(CH3COOH),则c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH),故D正确;
故答案为D。


科目:高中化学 来源: 题型:
【题目】据《科技日报》报道,我国科学家研制成功一系列石墨烯限域的3d过渡金属中心(Mn、Fe、Co、Ni、Cu)催化剂。请回答下列问题:
(1)基态Ni原子价层电子的轨道表达式为__________________。
(2)铜的焰色反应呈绿色,在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为_____。
(3)![]() 因具有良好的结构稳定性而成为新一代锂离子电池正极材料,这与
因具有良好的结构稳定性而成为新一代锂离子电池正极材料,这与![]() 的结构密切相关,
的结构密切相关,![]() 的立体构型为________,P、O、S的电负性从大到小的顺序为_____,
的立体构型为________,P、O、S的电负性从大到小的顺序为_____,![]() 过度脱出易导致锂电池结构坍塌产生O2而爆炸,实验证实O2因具有单电子而成为顺磁性分子,下列结构式(黑点代表电子)中最有可能代表O2分子结构的是_____(填标号)。
过度脱出易导致锂电池结构坍塌产生O2而爆炸,实验证实O2因具有单电子而成为顺磁性分子,下列结构式(黑点代表电子)中最有可能代表O2分子结构的是_____(填标号)。
A. B.
B.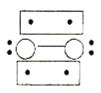 C.
C.![]() D.
D.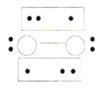
(4)![]() 易与
易与![]() 结合形成
结合形成![]() ,
,![]() 与
与![]() 间的化学键类型为________,若将配离子
间的化学键类型为________,若将配离子![]() 中的2个
中的2个![]() 换为
换为![]() ,2种结构,则
,2种结构,则![]() 是否为
是否为![]() 杂化________(填“是”或“否”),理由为_________________。
杂化________(填“是”或“否”),理由为_________________。
(5)金属锰有多种晶型,其中![]() 的结构为体心立方堆积,晶胞参数为apm。
的结构为体心立方堆积,晶胞参数为apm。![]() 中锰的原子半径为________pm。已知阿伏加德罗常数的值为
中锰的原子半径为________pm。已知阿伏加德罗常数的值为![]() ,
,![]() 的理论密度
的理论密度![]() ________
________![]() 。(列出计算式)
。(列出计算式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肉桂皮是肉桂树的树皮,常被用作药物和食用香料,有效成分为肉桂醛。从肉桂皮中提取肉桂醛的主要流程如下:

下列说法不正确的是
A.肉桂醛可用作食品添加剂且不应过量
B.肉桂醛可溶于乙醇
C.红外光谱可检测出肉桂醛分子中含有碳碳双键和醛基
D.肉桂醛长期置于空气中容易发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式不正确的是
A.硫酸铝溶液中加入氢氧化钡溶液:Ba2++![]() == BaSO4↓
== BaSO4↓
B.硫酸亚铁溶液中加入过氧化氢溶液:2Fe2+ + H2O2 + 2H+ == 2Fe3+ + 2H2O
C.向NaHCO3 溶液中加入NaOH溶液:![]() + OH-==
+ OH-==![]() + H2O
+ H2O
D.向AgCl悬浊液中加入Na2S溶液:2AgCl + S2-== Ag2S + 2Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象预测正确的是
A | B | C | D |
|
|
|
|
烧杯中产生白色沉淀,一段时间后沉淀无明显变化 | 加盐酸出现白色浑浊,加热变澄清 | KMnO4 酸性溶液在苯和甲苯中均褪色 | 液体分层,下层呈 无色 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种天然化合物X的结构简式如图所示。下列有关该化合物的说法中正确的是

A.化合物X分子中所有原子可能在同一平面上
B.化合物X能使酸性高锰酸钾溶液褪色
C.化合物X存在顺反异构和手性异构
D.X能与NaHCO3溶液反应生成CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国具有丰富的铜矿资源,请回答下列有关铜及其化合物的问题:
(1)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。Cu和Zn在元素周期表中位于_____区,请写出基态Cu原子的价电子排布式_______________。第一电离能Il(Zn)_______Il(Cu)(填“大于”或“小于”),原因是________。
(2)新型农药松脂酸铜具有低残留的特点,下图是松脂酸铜的结构简式,请分析1个松脂酸铜中π键的个数是______,加“*”碳原子的杂化方式为________。
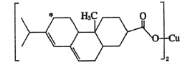
(3)硫酸铜溶于氨水形成[Cu(NH3)4]SO4深蓝色溶液。
①在[Cu(NH3)4]2+中Cu2+、NH3之间形成的化学键为____,提供孤电子对的成键原子是______。
②![]() 立体构型是_____________。
立体构型是_____________。
③NH3的沸点 _________(填“高于”或“低于”)PH3;
(4)一种铜镍合金(俗称白铜)的晶胞如下图所示,铜、镍原子个数比为__________。
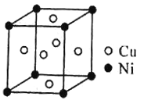
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上合成氨反应的能量变化如图所示,该反应的热化学方程式是
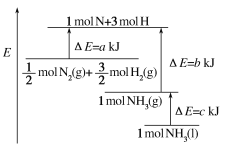
A. N2(g)+3H2(g)=2NH3(l) ΔH=2(a-b-c)kJ·mol-1
B. N2(g)+3H2(g)=2NH3(g) ΔH=2(b-a)kJ·mol-1
C. ![]() N2(g)+
N2(g)+![]() H2(g)=NH3(l) ΔH=(b+c-a)kJ·mol-1
H2(g)=NH3(l) ΔH=(b+c-a)kJ·mol-1
D. ![]() N2(g)+
N2(g)+![]() H2(g)=NH3(g) ΔH=(a+b)kJ·mol-1
H2(g)=NH3(g) ΔH=(a+b)kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A由碳、氢、氧三种元素组成。现取2.3 g A与2.8 L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余)。将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重2.7 g,碱石灰增重2.2 g。回答下列问题:
(1)2.3 g A中所含氢原子、碳原子的物质的量分别是n(H)=______mol;n(C)=_______mol
(2)该有机物的分子式_____________,写出所有可能结构简式____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com