
A、中子数为16的硫离子:
| ||
B、COS的电子式是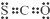 | ||
C、氧的原子结构示意图: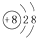 | ||
| D、HClO的结构式:H-O-Cl |
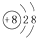 中核外电子总数大于核电荷数,为氧离子,氧原子的核电荷数=核外电子总数=8,最外层为6个电子;
中核外电子总数大于核电荷数,为氧离子,氧原子的核电荷数=核外电子总数=8,最外层为6个电子;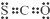 ,故B正确;
,故B正确;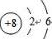 ,故C错误;
,故C错误;

 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
| A、1L 该溶液中含硝酸钾 202g |
| B、100mL 该溶液中含硝酸钾0.02mol |
| C、从 1L该溶液中取出500 mL 后,剩余溶液的浓度为0.1mol/L |
| D、1L水中溶解0.2mol硝酸钾,即可配得 0.2mol/L硝酸钾溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,22.4LCO2中含有NA个CO2分子 |
| B、室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA |
| C、标准状况下,11.2L氦气中约含有NA个氦原子 |
| D、1L0.1mol?L-1Na2SO3溶液中含有0.1NA个SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳、硅都是较活泼的非金属,它们只能以化合态存在于自然界中 |
| B、等质量的Na2CO3、NaHCO3分别与足量盐酸反应,前者产生的CO2多 |
| C、一定条件下CO2、SiO2都能与NaOH、Na2CO3(或CaCO3)发生反应 |
| D、热稳定性:CH4<SiH4;酸性H2CO3>H2SiO3(H4SiO4) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、+3 | B、+4 | C、+5 | D、+6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、过量二氧化碳通人偏铝酸钠溶液中:CO2+3H2O+2AlO2-=2Al(OH)3↓+CO32- | ||||
| B、氯化铝溶液中加入过量氨水:Al3++4OH-=AlO2-+2H2O | ||||
| C、在碳酸氢镁溶液中加入过量石灰水:Mg2++2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+MgCO3↓ | ||||
D、碳酸氢铵溶液与过量的NaOH溶液混合:NH4++HCO3-+2OH-
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钙是人体内含量最丰富的元素之一 |
| B、在人体内钙构成骨骼和牙齿 |
| C、缺钙的人可以多喝牛奶、豆奶等乳制品补钙 |
| D、钙是人体内公认的“智慧元素” |
查看答案和解析>>
科目:高中化学 来源: 题型:

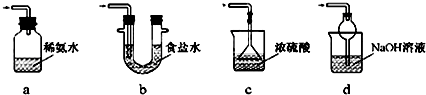
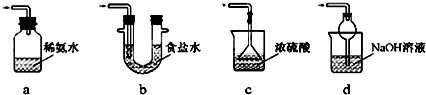
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(N2)=0.01mol/(L?s),v(H2)=0.02mol/(L?s) |
| B、v(H2)=0.02mol/(L?s),v(NH3)=1.2mol/(L?min) |
| C、v(N2)=0.01mol/(L?s),v(NH3)=1.2mol/(L?min) |
| D、v(H2)=0.06mol/(L?s),v(NH3)=0.4mol/(L?min) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com