
下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:





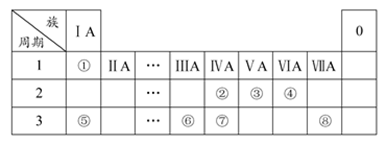
(1) ②③⑦的最高价含氧酸的酸性由弱到强的顺序是(用化学式表示) 。
(2) 写出由④⑤两种元素组成的既含离子键、又含非极性共价键的化合物的电子式 。
(3) ①、④两种元素按原子个数之比为1∶1组成的常见液态化合物,在酸性溶液中能将
Fe2+氧化,写出该反应的离子方程式 。
(4) ①③⑧可组成一种化合物,其原子个数之比为4︰1︰1。该化合物的化学式为_________,该化合物的水溶液显酸性,用离子方程式表示其显酸性的原因 。
科目:高中化学 来源: 题型:
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
下列叙述正确的是( )
A.X、Y元素的金属性 X<Y
B.一定条件下,Z单质与W的常见单质直接生成ZW2
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.一定条件下,W单质可以将Z单质从其氢化物中置换出来
查看答案和解析>>
科目:高中化学 来源: 题型:
下列共有十二种化学符号:
①O2 ②614C ③238U ④1123Na ⑤O3 ⑥714N ⑦1224Mg ⑧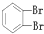
⑨235U ⑩ (11)
(11)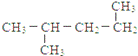 (12)
(12)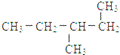
其中:
(1)表示核素的符号共有___种.
(2)互为同位素的是___(填序号,以下相同).
(3)质量数相等,但不能互称同位素的是___.
(4)中子数相等,但质子数不相等的是___.
(5)互为同素异形体的是___.
(6)互为同分异构体的是___.
查看答案和解析>>
科目:高中化学 来源: 题型:
N2O俗称“笑气”,医疗上曾用作可吸入性麻醉剂,下列反应能产生N2O:3 CO+2NO2=3CO2 +N2O。下列关于N2O的说法一定正确的是( )
CO+2NO2=3CO2 +N2O。下列关于N2O的说法一定正确的是( )
A.上述反应中,每消耗2mol NO2,就会生成22.4L N2O
B. 等质量的N2O和CO2含有相等的电子数
C. N2O有氧化性,且为HNO2的酸酐
D.N2O的氧化性强于NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:(NH4)2CO3(s)=NH4HCO3(s)+NH3(g) △H=+74.9 kJ·mol-1,下列说法中正确的是( )
A.该反应中熵变、焓变皆大于0
B.该反应是吸热反应,因此一定不能自发进行
C.碳酸盐分解反应中熵增加,因此任何条件下所有碳酸盐分解一定自发进行
D.能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
[化学——选修2:化学与技术](14分)
纯碱(化学式为Na2CO3)是一种重要的化工原料。现代化工生产有三种工艺:
(一)布兰制碱法。以食盐为原料制碱,该法分三步:
①用氯化钠与硫酸反应制硫酸钠:2NaCl+H2SO4=Na2SO4+2HCl;
②用焦炭还原硫酸钠得硫化钠:Na2SO4+4C=Na2S+4CO↑
③用硫化钠与石灰石反应制碳酸钠:Na2S+CaCO3=Na2CO3+CaS
(二)氨碱法即索尔维制碱法。以食盐、氨、二氧化碳为原料,其反应也分三步进行:
①NH3+CO2+H2O=NH4HCO3
②NH4HCO3+NaCl=NaHCO3+NH4Cl
③2NaHCO3=Na2CO3+CO2↑+H2O
(三)候氏制碱法。低温下先向饱和食盐水中通入氨气,再通入二氧化碳可析出碳酸氢钠,再加入细盐末,因同离子效应,低温氯化铵溶解度突然降低,而食盐的溶解度变化不大,所以氯化铵析出而食盐不析出;再用氨饱和后通二氧化碳,结果往返析出NaHCO3和NH4Cl。该法生产的纯碱质量优良,纯白如雪。
(1)相比另外两种方法,布兰制碱法工艺的缺点除了成本较高,生成CO和CaS等污染物外还有__________________________和_____________________________(写两点)。
(2)氨碱法工艺的中循环利用的物质是_________(填化学式);产品的副产物NH4Cl既可以做氮肥又可以重新生成氨气。写出NH4Cl与生石灰反应的化学方程式 。
(3)候氏制碱法反应的方程式为____________________________________________。
(4)为什么候氏制碱法工艺中先向饱和食盐水中通入氨气,再通入二氧化碳。理由是__________________________________________________(写一点)。
(5)候氏制碱法产品纯碱中含有碳酸氢钠。如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,用m1表示加热前纯碱样品的质量,m2表示加热后固体的质量。则纯碱中碳酸氢钠的质量分数可表示为:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据原子结构及元素周期律的知识,下列推断正确的是
A.同主族元素含氧酸的酸性随核电荷数的增加而减弱
B.核外电子排布相同的微粒化学性质也相同
C.Cl‾、S2‾、Ca2+、K+半径逐渐减小
D. 与
与 得电子能力相同
得电子能力相同
查看答案和解析>>
科目:高中化学 来源: 题型:
有下列物质:①CO2 ②N2 ③H2O2 ④NH3 ⑤Ca(OH)2 ⑥Na2O2 ⑦NH4Cl,试用以上物质的序号填空:
(1)既有极性键,又有非极性键的是______________;
(2)既有离子键,又有非极性键的是______________;
(3)属于共价化合物的是______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com