
【题目】下列关于苯的说法正确的是( )
A.苯的分子式是C6H6,不能使酸性高锰酸钾溶液褪色,苯属于饱和烃
B.从苯的凯库勒式来看,分子中含有双键,所以苯是乙烯的同系物
C.在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应
D.苯分子为平面正六边形结构,6个碳原子之间的化学键完全相同
科目:高中化学 来源: 题型:
【题目】以钙为例,用化学方程式表示钙及其化合物之间的转化关系。

(1)①______________________________________________。
②______________________________________________。
③______________________________________________。
④______________________________________________。
⑤______________________________________________。
⑥______________________________________________。
(2)上述反应中,属于化合反应的是______(填序号,下同),属于复分解反应的是_____。
(3)上述反应①~⑥中属于氧化还原反应的是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别由短周期元素m、n、p、q组成的单质依次为甲、乙、丙、丁,有关反应关系如图所示(部分产物省略)。其中甲为黄绿色气体,M、N均为10电子分子且M的水溶液呈碱性,Q为离子化合物,下列说法中正确的是

A. 原子半径的大小m>q>n>p
B. 元素非金属性q>n>p
C. Q的溶液可以保存在细口玻璃试剂瓶
D. n的氧化物的水化物一定为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.分子式符合CnH2n+2的不同物质一定互为同系物
B.分子式符合CnH2n的烃不一定是烯烃
C.烷烃、烯烃和炔烃都属于链状烃
D.芳香族化合物均具有香味
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列叙述不正确的是( )
A. pH=5的硫酸溶液稀释到原来的500倍,稀释后c(SO42-)与c(H+)之比约为1:10
B. Na2CO3、NaHCO3两种盐溶液中,离子种类相同
C. CH3COONa溶液中滴加少量浓盐酸后c(CH3COO-)增大
D. 滴入酚酞,NaNO2溶液显红色,证明HNO2是弱电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M是一种食品香料可以C4H10为原料通过如图所示路线合成:
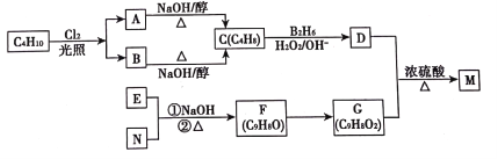
已知:①R—CH==CH2 ![]() R—CH2CH2OH
R—CH2CH2OH
②RCH2CHO+R′CH2CHO ![]()

③C、F分子中的碳链上C有支链,F没有支链;E为芳香族化合物且E、N都能发生银镜反应。请回答下列问题:
(1)A、B均为一氯代烃,写出其中一种的名称(系统命名)___________;M中的含氧官能团名称为___________。
(2)写出下列反应的反应类型:D+G→M___________。
(3)F与新制Cu(OH)2/NaOH(aq)反应的化学方程式为_______________________________。
(4)M的结构简式为___________________。
(5)与G具有相同官能团的G的芳香类同分异构体有___________种。
(6)参照上述合成路线,以苯乙烯( )和乙醛为原料(无机试剂任选),设计制备
)和乙醛为原料(无机试剂任选),设计制备![]() —C H2CH== CHCHO的合成路线:____________________________________________。
—C H2CH== CHCHO的合成路线:____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下表中烃的分子式排列规律,判断空格中的烃的同分异构体数目( )
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
CH4 | C2H4 | C3H8 | C4H8 | C6H12 | C7H16 | C8H16 |
A. 2B. 3C. 4D. 5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究碳氧化合物、氮氧化合物、硫氧化合物等大气污染物的处理对缓解环境污染、能源危机具有重要意义。工业上处理氮的氧化物途径有多种:
Ⅰ.碱吸法。
(1)利用纯碱溶液吸收NO、NO2,发生的反应共生成两种盐,请写出有关氧化还原方程式:______________________________________、NO+NO2+Na2CO3=2NaNO2+CO2
Ⅱ.催化氧化法:城市中NOx和CO污染主要来源于汽车尾气,可以利用化学方法将其转化为无毒无害的物质。
(2)已知:N2(g)+O2(g)![]() 2NO(g) ΔH=+180 kJ·mol-1
2NO(g) ΔH=+180 kJ·mol-1
2CO(g)+O2(g)![]() 2CO2(g) ΔH=-564 kJ·mol-1
2CO2(g) ΔH=-564 kJ·mol-1
请写出把汽车尾气转化为无毒无害的物质的热化学方程式:__________________________
(3)为研究汽车尾气转化为无毒无害的物质有关反应,在密闭容器中充入10molCO和8molNO,发生反应,如图为平衡时NO的体积分数与温度、压强的关系。

①该反应达到平衡后,为在提高反应速率同时提高NO的转化率,可采取的措施有__________(填字母序号)。
a.改用高效催化剂 b.缩小容器的体积 c.升高温度 d.增加CO的浓度
②压强为10 MPa、温度为T1下,若反应进行到20 min达到平衡状态,容器的体积为4 L,用CO2的浓度变化表示的平均反应速率v(CO2)=_______,该温度下平衡常数Kp=______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数;保留两位有效数字)。
③若在D点对反应容器降温的同时缩小体积至体系压强增大,重新达到的平衡状态可能是图中A~G点中的______点。
Ⅲ. 电解硝酸工业的尾气NO可制备NH4NO3,其工作原理如图。

(4)N极的电极反应式为________。
(5)在25℃时,将a mol·L-1的氨水与0.1mol·L-1的硝酸等体积混合后溶液显中性,用含a的代数式表示NH4NO3的水解常数Kh=_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com